第三节 生物大分子
C是组成生物体的主要成分之一,它的最外层的4个电子能与其他4个原子形成共价键,这些原子主要是C、H、O、N、S等。其中,碳氢化合物是碳化合物的最基本形式。不同数量的C原子能构成不同长度的碳氢化合物,有些是直链的,有些是分支的,也可以结合成环状。C与C之间可形成单键、双键和三键,这些结构称为有机化合物的碳骨架。碳氢化合物中的H原子若被其他基团代替则形成多种多样的碳化物,这是生物多样性的物质基础。而这些基团常以一定的结构出现,赋予化合物一定的性质,称为功能基团(functional group)(或官能团)。生物体中的有机化合物含有的功能基团主要有羟基、羰基、羧基、氨基等(如图2-6)。
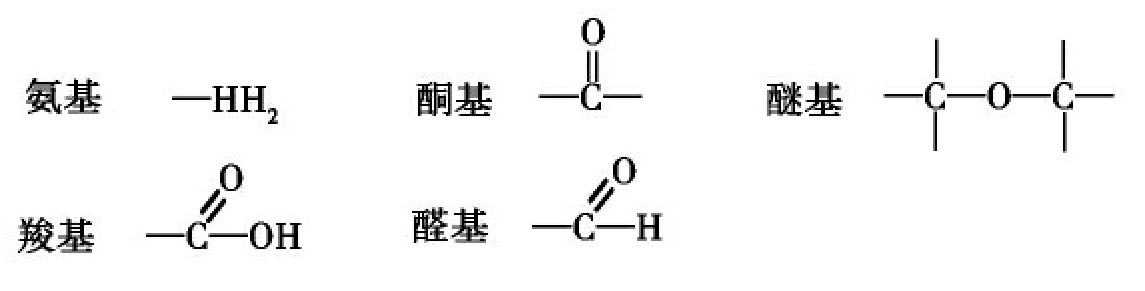
图2-6 几种主要的功能基团
氨基是氨基酸的代表基团,羧基是羧酸的代表基团,也是氨基酸中的重要原子团。醛基及酮基是糖的主要组成部分。除此之外还有甲基、磷酸基、巯基等功能基团。
蛋白质、核酸、脂类和糖类是组成生物体最重要的生物分子,其中,蛋白质、核酸和多糖类是由含有彼此相同或相近功能基团的单体作为单位聚合而成的大分子。聚合反应是脱水反应称脱水缩合反应(dehydration-condensation reaction)。形成的大分子也能不同程度地被水解,形成短链甚至单体。
一、糖类
糖类(carbohydrate)是多羟醛或多羟酮及其缩合物和某些衍生物的总称。糖类是自然界中含量最多的有机化合物,广泛分布于生物体中。存在于植物中的糖类以干物质计,其质量可高达80%以上。如谷类和薯类中的淀粉,木材、稻草、棉麻中的纤维素和半纤维素、甘蔗和甜菜中的蔗糖,水果中的葡萄糖和果糖等。糖类是有机体能量的主要来源之一,是生物代谢过程的重要中间代谢物,有些糖是构成生物大分子,如核糖和糖蛋白的成分。除此之外有些糖类物质在生物体内可充当结构物质,如细菌多糖、壳多糖、纤维素等。根据糖类的水解情况和水解后形成的物质,可分为单糖(monosaccharide)、二糖(disaccharide)和多糖(polysaccharide)三大类。单糖是不能水解的糖,如葡萄糖(glucose)、半乳糖(galactose)、果糖(fructose)以及核糖(ribose)、脱氧核糖(deoxyribose)等。二糖由两分子单糖结合而成,水解后产生单糖。如蔗糖(sucrose)、乳糖(lactose)、麦芽糖(maltose)等。多糖是能够水解成许多分子单糖及其衍生物的糖,如淀粉(starch)、纤维素(cellulose)、糖原(glycogen)等。
1.单糖
单糖(monosaccharide)是构成糖的最小单体。由3~7个碳原子构成单糖的主要骨架,主要组成元素是C、H、O,分子式为(CH2O)n。重要的单糖有甘油醛、二羟丙酮、葡萄糖、果糖、半乳糖、核糖、脱氧核糖等(如图2-7)。单糖的每个碳原子上都含有羟基(-OH),因此都具有极性,易溶于水。构成糖的碳链可以有不同的长度,对多数碳水化合物来说,六碳糖是最重要的单体分子,例如葡萄糖是构成淀粉、糖原和纤维素的单体分子。
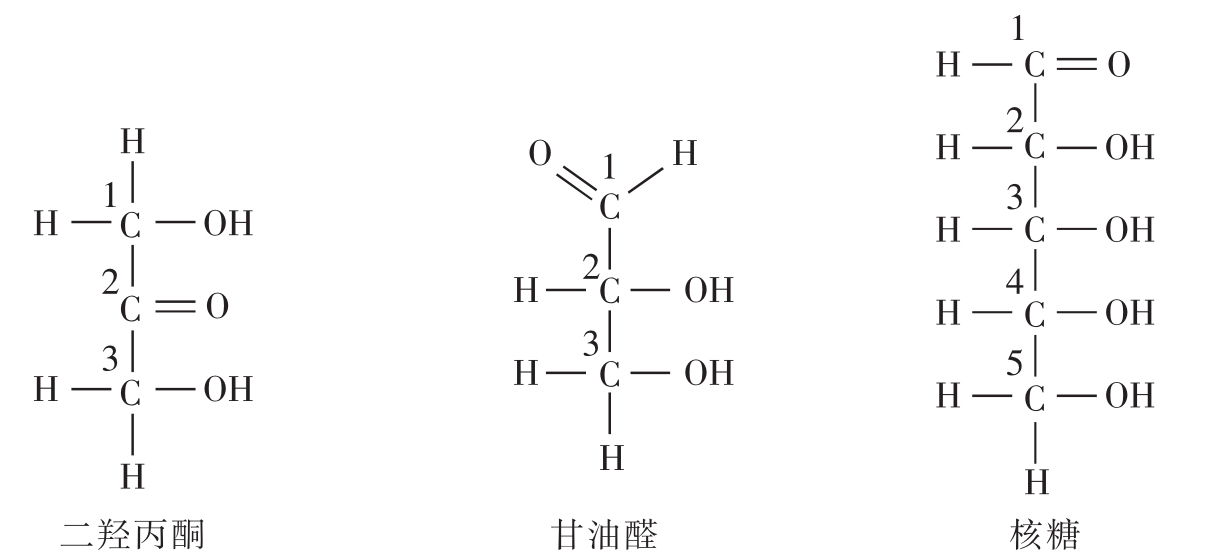
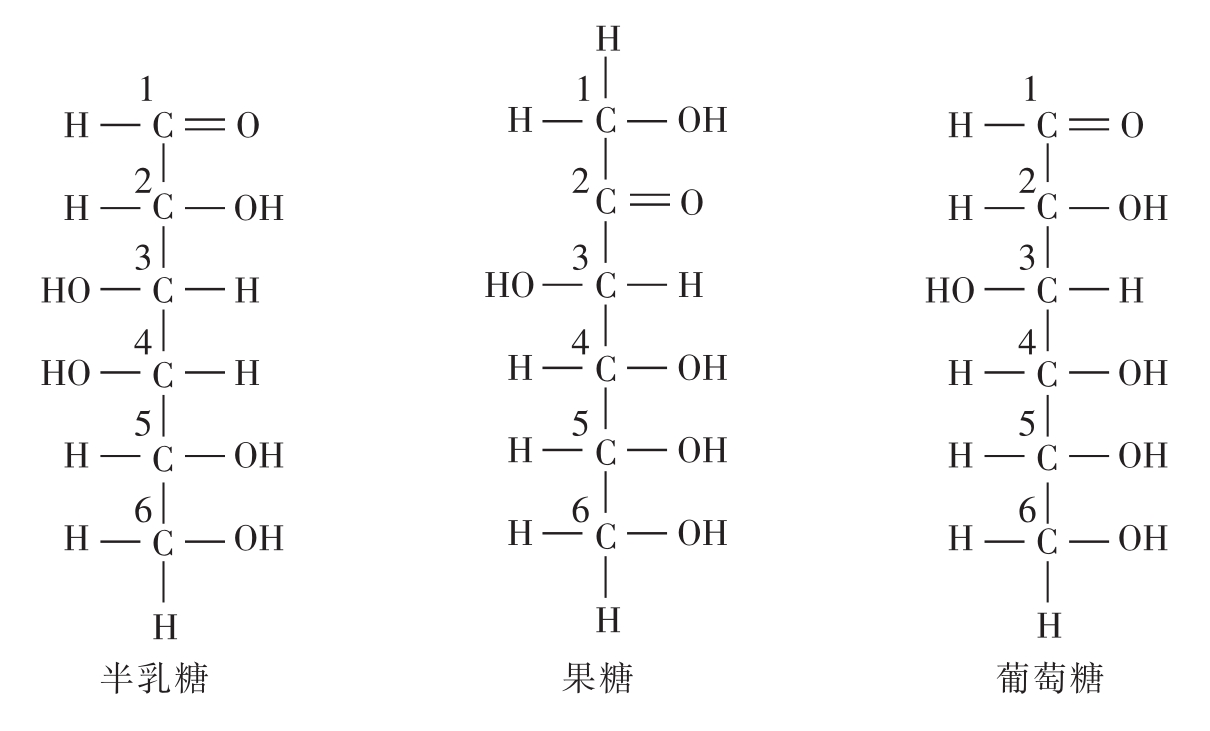
图2-7 几种重要的单糖的链式结构
甘油醛是最小的单糖,核糖是五碳糖,核糖脱去C2上的O原子就成为脱氧核糖。葡萄糖、果糖和半乳糖为六碳糖,它们互为同分异构体。
葡萄糖是自然界存在最广泛的单糖,分子式为C6 H12 O6,与半乳糖和果糖的分子式相同但结构式不相同,称为同分异构体(isomer)。两个异构体的构象关系如同物体与其在镜子中所成的像的关系,两者不能叠合,即为镜像异构体,分别称为D型和L型。天然存在的葡萄糖都是D型的。葡萄糖是有机体的主要供能物质,也是光合作用最先形成的糖。葡萄糖在溶液中往往以环状结构存在。成环是由糖分子中的羰基与倒数第二位碳原子上的羟基相互反应形成半缩醛或半缩酮而成。在环状结构中,C1的羟基写在环平面下面的为α型,写在环平面之上则为β型。溶液中葡萄糖是以α型和β型葡萄糖的混合液存在的(如图2-8)。
果糖大量存在于水果的浆汁和蜂蜜中,是最甜的单糖。纯净的果糖为无色晶体,由于不易结晶,通常为黏稠的液体状态。果糖易溶于水、乙醇和乙醚,不易产生脂肪堆积,不易引起高血压,不会产生龋齿,是目前世界上已知的最安全最健康的糖之一。

图2-8 α和β型葡萄糖的分子结构式
半乳糖存在于奶类产品、甜菜和常青藤的浆果中,是哺乳动物的乳汁中乳糖的组成成分。因此,用双歧杆菌发酵乳糖能产生半乳糖。在大脑和神经组织中常以D-半乳糖苷的形式存在,是构成脑神经系统中脑苷脂的成分,与婴儿出生后脑的迅速生长有密切关系。半乳糖也常被用作营养增甜剂。
2.二糖
两分子的单糖脱水缩合能形成以糖苷键(glycosidic bond)相连接的二糖,又称双糖(disaccharide)。例如麦芽糖是由两分子葡萄糖缩合而成,蔗糖由一分子葡萄糖与一分子果糖缩合而成,乳糖由一分子葡萄糖与一分子半乳糖缩合而成。二糖可水解为两分子单糖。
蔗糖是常用食糖,由甘蔗或甜菜中提取而来。1分子蔗糖由1分子α-D-葡萄糖C1位上的半缩醛羟基与β-果糖的C2位上的半缩酮羟基缩合形成α,β-1,2-糖苷键连接而成(如图2-9)。蔗糖是在人体肠道内经蔗糖酶水解成果糖和葡萄糖而被吸收。
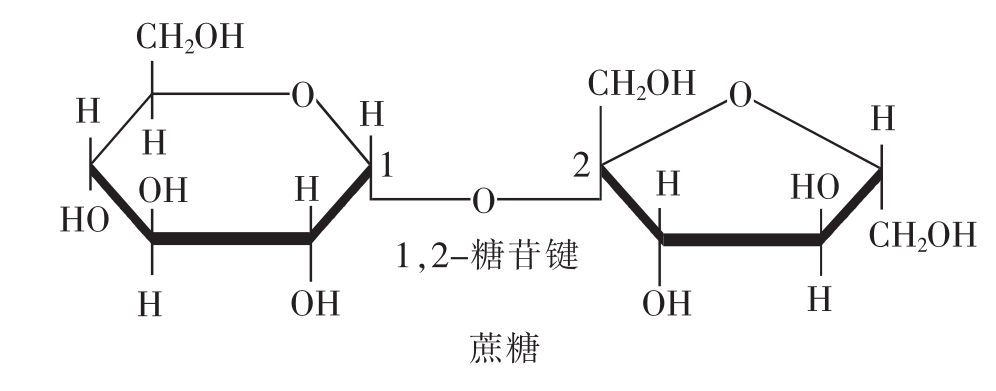
图2-9 蔗糖的分子结构式
蔗糖由1分子α-D-葡萄糖C1位上的半缩醛羟基与β-果糖的C2位上的半缩酮羟基缩合形成α,β-1,2-糖苷键连接而成。
麦芽糖又称饴糖,大量存在于发芽的各类种子中,由淀粉酶水解淀粉而成。人体的唾液淀粉酶和胰淀粉酶也可使食物中淀粉水解生成麦芽糖,麦芽糖再经肠液中麦芽糖酶水解成两分子葡萄糖。麦芽糖由2分子α-D-葡萄糖通过α-1,4糖苷键相连(图2-10)。
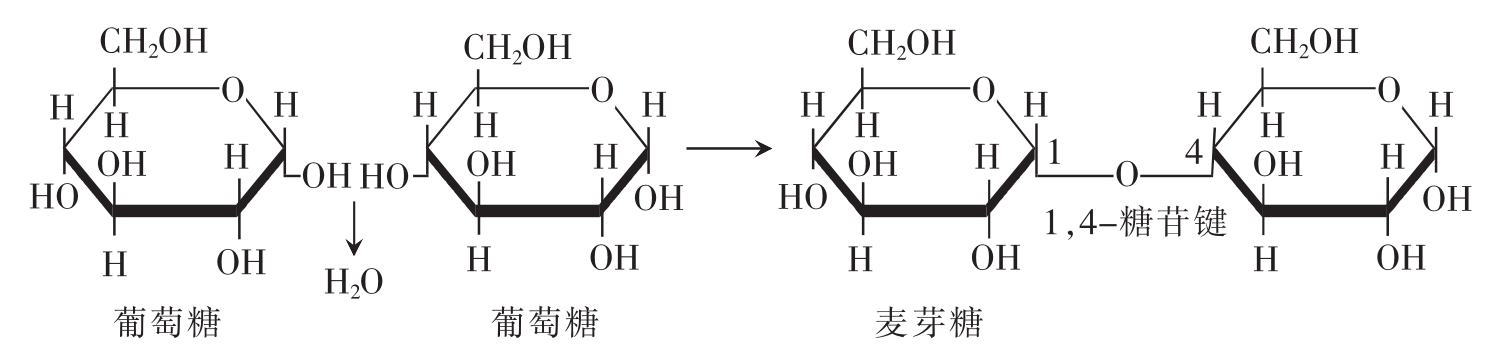
图2-10 麦芽糖的分子结构式
麦芽糖由1分子α-D-葡萄糖的C1上的羟基和1分子α-D-葡萄糖C4上的羟基脱去1分子水,形成α-1,4糖苷键。
在人和动物乳汁中还存在乳糖。牛奶中乳糖的比例为4%,人乳中乳糖的比例为5%~7%。乳糖是由1分子β-D-半乳糖和1分子α-D-葡萄糖缩合而成,2个单糖之间通过β-1,4-糖苷键连接。在人体中,乳糖又可被肠液乳糖酶水解生成半乳糖和葡萄糖,被人体所吸收。
3.多糖
多糖(polysaccharides)是自然界数量最多的糖类。多糖分子是由很多单糖分子(通常是葡萄糖分子)脱水缩合而成的分支或不分支的长链分子。多糖是大分子化合物,分子量从几万到几百万不等,分子通式为(C6 H12 O5)n。常见的多糖有淀粉(starch)、纤维素(cellulose)和糖原(glycogen)等。
淀粉是植物细胞中以贮藏状态存在的糖,是贮存能量的多糖,可以水解先形成糊精,再生成麦芽糖,最后水解成葡萄糖,以维持相关代谢的进行。淀粉广泛分布于块根、块茎和谷类种子中,如大米中约含淀粉80%,面粉中淀粉含量约70%,土豆中约含20%。淀粉是由数百至数千个α-D-葡萄糖分子脱水形成α-1,4-糖苷键连接而成的链状分子。淀粉包括直链淀粉和支链淀粉(如图2-11)。链不分支的淀粉称为直链淀粉(amylose),通常卷曲成螺旋形。链分支的称为支链淀粉(amylopectin)。支链淀粉一般每隔24~30个葡萄糖就有一个分支。在分支处葡萄糖之间形成的是α-1,6-糖苷键。马铃薯淀粉中22%是直链的,78%是支链的。豆类种子所含淀粉全为直链淀粉,糯米淀粉全为支链淀粉。直链淀粉能溶于热水而不成糊状,而支链淀粉不溶于热水,与热水作用后膨胀成糊状。这也是糯米口感黏性较大,与豆类差别很大的原因。直链淀粉遇碘变成深蓝色,支链淀粉遇碘显棕红色。这是鉴定淀粉的简便方法。
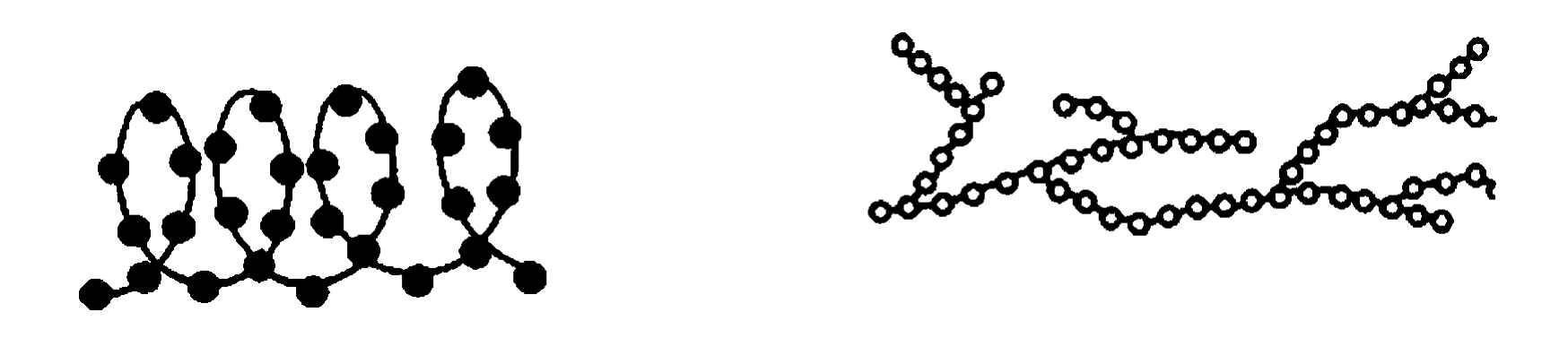
图2-11 直链淀粉和支链淀粉的结构
链不分支的淀粉称为直链淀粉,链分支的称为支链淀粉。
地球上含量最丰富的糖类是纤维素。高等植物细胞壁的主要成分是纤维素,木质部中纤维素含量达50%以上,而棉花纤维中90%以上都是纤维素。纤维素分子由10000~15000个β-D-葡萄糖形成β-1,4-糖苷键连接而成,不分支。纤维素分子的链与链之间拧在一起,像麻绳一样。纤维素在纤维素酶作用下水解产生纤维二糖,再进一步水解而成葡萄糖。人没有纤维素酶,不能水解β-1,4-糖苷键,因此不能消化纤维素。但食物中纤维素成分能刺激肠道蠕动,有通便作用,可改善便秘。而马、牛、羊等动物肠道内的微生物能产生水解β-1,4-糖苷键的酶,所以这些动物能消化纤维素。
糖原是动物细胞中贮存的多糖,又称动物淀粉,在肌肉和肝脏中含量较高,以颗粒状贮存,需要时可以水解释放出葡萄糖。糖原分子结构与支链淀粉相似,也是由α-D-葡萄糖分子脱水形成1,4-糖苷键连接而成的链状分子,但糖原的分支比支链淀粉多,分支长度比支链淀粉短,主链每隔8~12个葡萄糖就有一个分支点,每个分支约有12~18个葡萄糖分子。糖原在水中的溶解度大于淀粉,与碘溶液作用呈红褐色。
除了上述多糖外,生物界还存在一些重要的其他类型的多糖,如几丁质(chitin)、粘多糖(mucopolysaccharide)、果胶(pectin)等。几丁质是昆虫和甲壳类外骨骼的主要成分,在真菌的细胞壁中也存在。它和纤维素相似,但它是由N-乙酰葡萄糖胺以β-1,4-糖苷键连接而成。如果将乙酰基去掉,则成为聚D-氨基葡萄糖,叫做壳糖胺(chitosan)。实验证明壳糖胺具有增强人体免疫功能等保健作用。粘多糖是组成人体细胞间质的主要成分,由氨基己糖、己糖醛酸及其他己糖所组成。果胶是半乳糖醛酸及其衍生物的多聚化合物。果实中的果胶含量很高,植物细胞壁之间的胞间层的主要成分也是果胶。细胞中糖类还和其他物质结合形成复杂的化合物,如糖蛋白、糖脂等。粘多糖在机体内也常与蛋白质结合成粘蛋白。这些物质都是细胞的重要成分。
二、脂类
脂类(lipid)包括的范围很广,这些物质在化学结构上差异很大,但是它们都有共同的特征,即常温常压下不溶于水,而易溶于乙醚、氯仿、四氯化碳、苯等有机溶剂中。脂类也是由C、H、O组成,有的还含有N、P,但其O含量比糖类中O的比例要小很多。脂类完全氧化时产生的能量远高于糖类,因此脂肪成为细胞中储存能量的物质。脂类是生物膜结构的主要成分,增加膜的柔软性、半透性;可构成生物表面的保护层,起防水和润滑的作用,如皮肤和羽毛以及果实外表的蜡质;是良好的绝缘体,能减缓热量散失,如动物皮下脂肪有保持正常体温的作用。还有些重要的生物活性物质如维生素D、睾丸酮、肾上腺皮质激素、前列腺素等都属于脂类。
1.中性脂肪、油和蜡
中性脂肪(fat)和油(oil)都是由甘油(glycerol)和脂肪酸(fatty acid)结合而成的脂类,在植物中称为油,在动物中称为脂肪。甘油分子有3个-OH,脂肪酸的碳氢链末端有一个-COOH,甘油的每个-OH和一个脂肪酸的-COOH缩合,形成酯键,就形成了一个脂肪分子(图2-12)。由于脂肪分子没有极性基团,所以称为中性脂肪,中性脂肪是高度疏水的。
脂肪酸的种类很多,如组成动物脂肪的脂肪酸就约有30种。中性脂肪或油的3个脂肪酸大多是不相同的。脂肪酸的碳氢链上没有双键的称为饱和脂肪酸,例如硬脂肪酸;至少有一个双键的是不饱和脂肪酸,例如油酸和亚油酸。不同脂肪酸之间的差别主要在于碳氢链的长短和双键的数目、位置。饱和脂肪酸分子可以伸直,紧密并列如晶体状,需较多热能才能使之散开,故熔点高,在室温下为固态。不饱和脂肪酸的双键部分扭曲成小弯,分子不能紧密排列,易于散开,因而熔点低,在室温下为液态。动物脂肪大多数富含饱和脂肪酸,例如猪的脂肪中油酸只占50%左右,其余均为饱和脂肪酸,故在室温下为固态。而植物油含有大量油酸和亚油酸,故在常温下为液态。动物脂肪由于含饱和脂肪酸多,对心血管有不利影响,以少食为宜。对于哺乳动物和人,亚油酸和亚麻酸是必需的营养要素,哺乳动物和人不能自己合成,只能从外界摄取。脂肪的主要功能是供应能量,保持体温,减少内部器官间的摩擦和压力,协助脂溶性维生素的吸收等。因此,生吃或水煮富含维生素A、D、E、K和胡萝卜素的食物,不利于这些维生素的吸收。
蜡(wax)和脂肪相似,也是由脂肪酸和醇化合而成的酯。但蜡的脂肪酸和醇都是长链,并且只有一个-OH。皮肤表面、毛、羽、植物叶及果实表面以及昆虫体表都有蜡覆盖,使细胞与外界严密隔离,防止细胞失水。
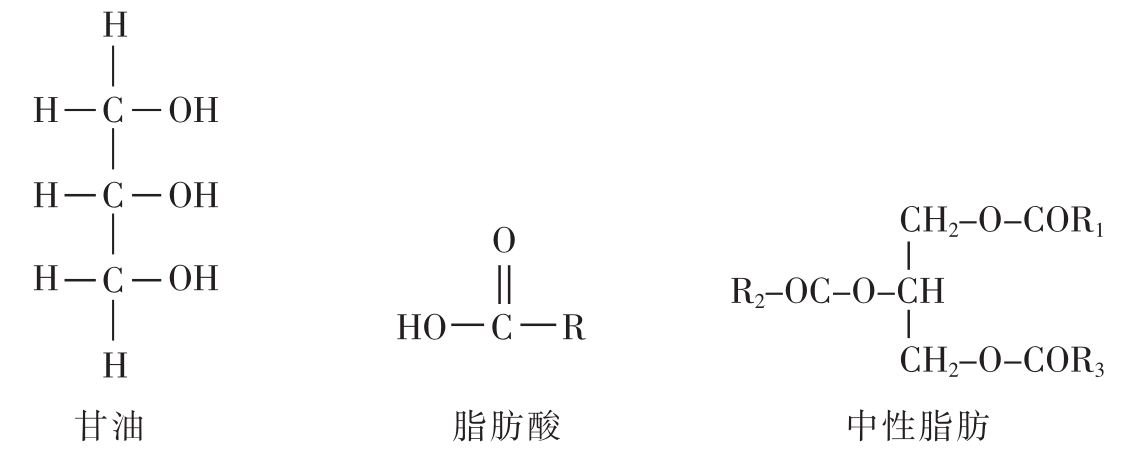
图2-12 甘油、脂肪酸、中性脂肪的结构式
甘油的每个-OH和一个脂肪酸的-COOH缩合,形成酯键。
2.磷脂类
磷脂(phospholipid)又称磷酸甘油酯(phosphoglyceride),绝大部分存在于细胞的膜系统中,在脑、肾、心、骨髓、卵及大豆细胞中含量最高。其组成和脂肪相似,不同之处在于:甘油的C3上的-OH不是和脂肪酸而是和磷酸基团结合成酯,形成最简单的磷脂——磷脂酸(phosphatidic acid)。磷脂酸在细胞中含量低,但它是其他磷脂合成的中间产物。细胞中的磷脂大多比磷脂酸复杂,即磷脂酸分子中的磷酸基团末端还带有其他含氮有机碱,所以是由甘油、脂肪酸、磷酸和含氮有机碱组成的。例如卵磷脂(lecithin)含氮碱为胆碱,脑磷脂(cephalin)中的含氮碱为胆胺。卵磷脂为白色蜡状物质,易溶于乙醚、乙醇等有机溶剂,是生物膜的主要成分,主要存在于脑、神经组织、红细胞、肾上腺中。蛋黄中含量达8%~10%。脑磷脂与血液凝集有关,血小板内的凝血激酶就是脑磷脂与蛋白质所组成的。脑磷脂也是动物膜结构中的主要成分。通常磷脂分子中的2个脂肪酸总有一个是不饱和的,因此2个脂肪酸不是平行并列的,其中一个不饱和脂肪酸总是折弯的。磷脂分子含磷酸和与之相连接的含氨基的化合物,所以是极性分子。但其分子两端在理化性质上差别很大。其2条脂肪酸链是非极性的尾,疏水性强,不溶于水。但甘油和磷酸基团一端处于电离状态,易溶于水,是亲水的(图2-13)。例如在水中,磷脂分子呈现规则排列,疏水端向内,亲水端向外,与水接触,形成单分子微团。将磷脂放在水面上,磷脂分子都将以亲水的头和水面相接,而倒立在水面上,形成一个单分子层。细胞膜的双层磷脂分子就是亲水的头部向外,疏水的脂肪酸链向内,位于两层中间。
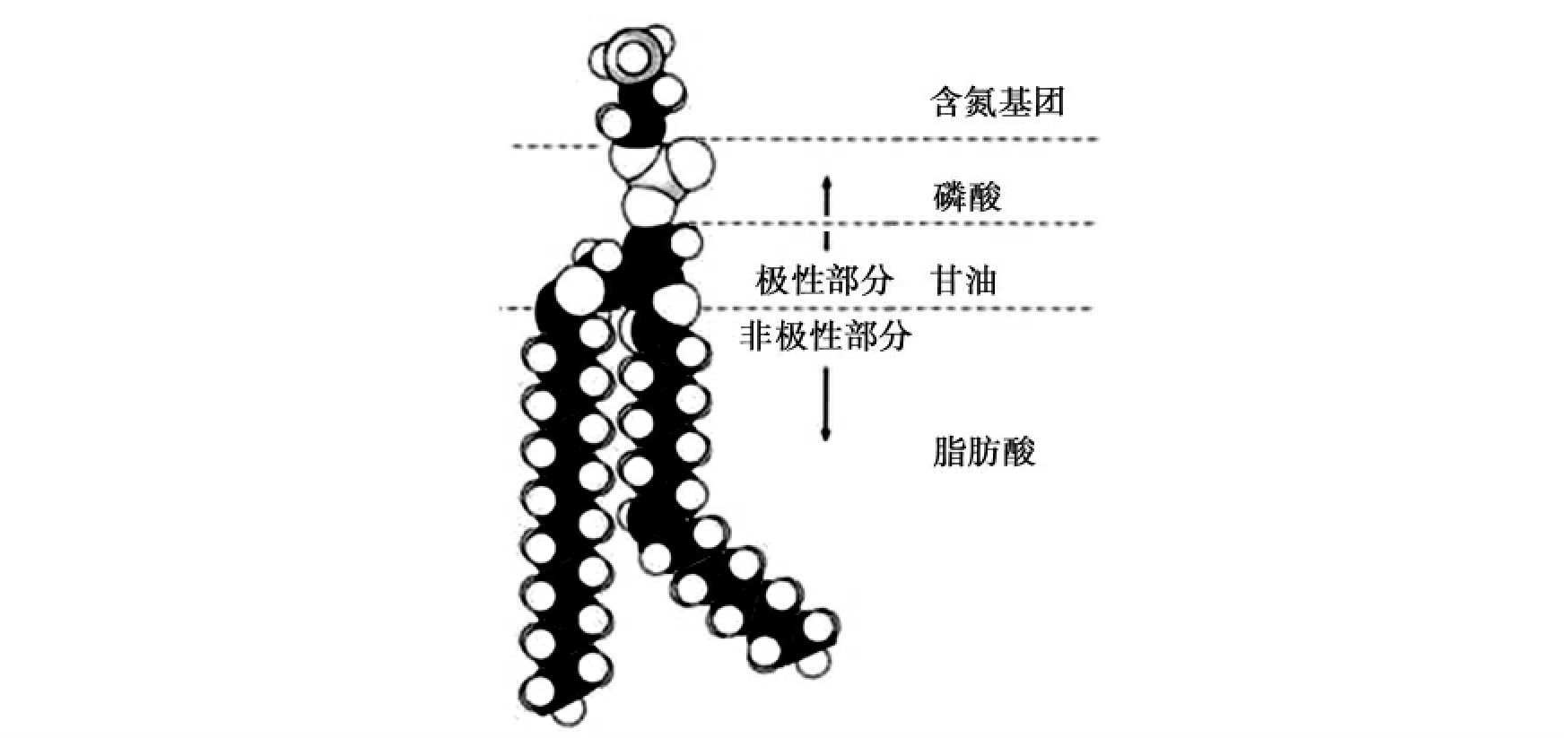
图2-13 磷脂的分子结构
磷脂分子是由甘油、脂肪酸、磷酸和含氮有机碱组成的。通常磷脂分子中的2个脂肪酸总有一个是不饱和的,因此2个脂肪酸不是平行并列的,其中一个不饱和脂肪酸总是折弯的。磷脂分子含磷酸和与之相连接的含氨基的化合物,所以是极性分子。但其分子两端亲水性相差很大。其2条脂肪酸链是非极性的尾,是疏水的。甘油和磷酸基团一端是极性亲水的。
3.类固醇和萜类
类固醇(steroid)又称甾类化合物,是一类具有特殊芳香族结构的物质。它们的理化性质与脂肪相近。不溶于水,而易溶于非极性的有机溶剂,所以习惯上将它们和脂类归在一起。但与脂肪不同的是它们不含脂肪酸。类固醇分子中碳原子排列成4个相关联的环,环上连有一侧链,侧链的长度和结构各不相同。最熟知的类固醇是在环戊烷多氢菲上连有一条碳氢链的胆固醇(图2-14)。胆固醇(cholesterol)是动物细胞膜和神经髓鞘的重要成分,与膜的透性有关。动物细胞线粒体和内质网膜中也有少量胆固醇。胆固醇是人体必需的化合物,在体内合成的量比从食物中吸收的多。胆固醇在体内可以转变成肾上腺皮质激素(corticoid)、性激素等重要物质,具有重要的生理功能。植物细胞不含胆固醇,但含有其他类固醇物质,称为植物固醇(phytosterol)。一些重要的生物活性物质,例如性激素、维生素D和肾上腺皮质激素等都属于类固醇。从结构上看,萜类和类固醇很相似。萜类也不含脂肪酸,是由不同数目的异戊二烯连接而成的分子。因不溶于水,所以也被列入脂类。植物细胞中的类胡萝卜素(carotenoid)属于萜类(terpene),由8个异戊二烯(isoprene)构成,是一种植物色素,辅助捕获光能,与植物的向光性有关。如β-胡萝卜素就是一种重要的类胡萝卜素(图2-15),1分子β-胡萝卜素可裂解生成2分子的维生素A,是维生素A的主要来源。另一萜类物质视黄醛,是维生素A的氧化物,也是视网膜细胞中所含的感光色素,对动物的感光活动有非常重要的作用。此外,维生素E和维生素K也都是萜类。
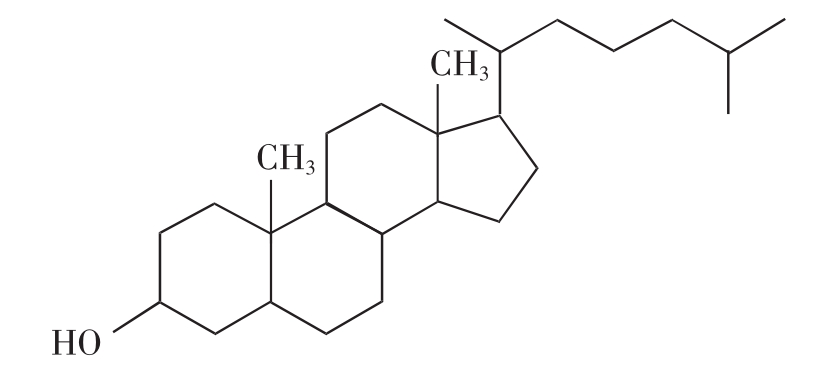
图2-14 胆固醇分子结构
胆固醇分子中不含脂肪酸,四个环成为环戊烷多氢菲。
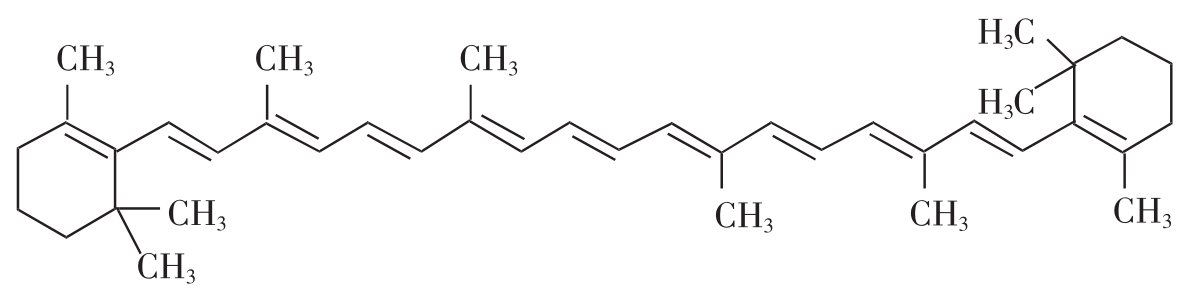
图2-15 β-胡萝卜素分子结构
β-胡萝卜素是光合作用的一种辅助色素,也是维生素的来源。
三、蛋白质
蛋白质(protein)是生物体中最重要的组成物质之一,自然界中几乎一切生物都含有大量蛋白质。如蛋白质占人体干重的45%,肌肉、皮肤、血液、毛发的主要成分都是蛋白质,微生物中蛋白质一般含50%~80%,而病毒中除核酸外其余均为蛋白质。蛋白质是生命物质的结构与功能的基础。有机体细胞的许多重要结构组分主要是蛋白质,绝大多数的酶以及某些激素也都是蛋白质。蛋白质种类繁多,人体中含有的蛋白质就达10万种以上。蛋白质比糖类和脂类更为复杂,除C、H、O外,还含有N,大多数蛋白质都含有S。
1.构成蛋白质的结构单元——氨基酸
组成蛋白质的氨基酸(amino acid)有20种,每种氨基酸都含有一个氨基(-NH2)、一个羧基(-COOH)和一个以字母R表示的化学基团,R基是连接着其他功能基团的侧链。氨基、羧基和R基都连接在同一个碳原子上,这个碳原子称为α-碳原子。此外该碳原子上还连有一个氢原子。因此,除了甘氨酸以外,所有氨基酸的α-碳原子都连接了4个不同的基团,所以氨基酸的α-碳原子为手性碳原子。根据旋光性的不同,左旋的氨基酸命名为L-α-氨基酸,右旋的命名为D-α-氨基酸,两者互为镜像(图2-17)。自然界中构成蛋白质的氨基酸几乎都是L-氨基酸。氨基酸之间的差异在于R基团的不同,R基团可以只是一个氢原子,如甘氨酸;也可以含有一个或多个氨基或羧基,如精氨酸和赖氨酸。根据R基团的极性不同可将氨基酸分成两类,一类是非极性疏水的,一类是极性亲水的;根据R基团化学性质的不同,可以将氨基酸分为脂肪族氨基酸、芳香族氨基酸、含硫氨基酸、醇类氨基酸、酸性氨基酸、碱性氨基酸和酰胺类氨基酸(图2-18)。R基团的结构决定了不同氨基酸在特性上的区别。同一氨基酸分子中含有碱性的氨基和酸性的羧基,它的羧基能解离释放出H+,形成-COO-,释放出的H+与氨基结合,形成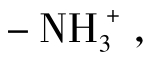 使得同一分子上带有正、负两种电荷,因此氨基酸是两性化合物,它是呈酸性还是呈碱性取决于所处的环境中的pH值。氨基酸不游离或游离成正、负离子的趋势相等时所处的环境的pH值称为该氨基酸的等电点,此时氨基酸在电场中不移动。在小于等电点的酸性环境中,氨基酸的羧基结合质子使其带正电荷,呈碱性。而在大于等电点的碱性环境中,氨基酸的氨基解离使其带负电荷,呈酸性。20种氨基酸中,有8种是人体不能制造的,非得从食物中补充,称为必需氨基酸(essential amino acid)。必需氨基酸对人体的生命活动来说,是重要的生活物质。
使得同一分子上带有正、负两种电荷,因此氨基酸是两性化合物,它是呈酸性还是呈碱性取决于所处的环境中的pH值。氨基酸不游离或游离成正、负离子的趋势相等时所处的环境的pH值称为该氨基酸的等电点,此时氨基酸在电场中不移动。在小于等电点的酸性环境中,氨基酸的羧基结合质子使其带正电荷,呈碱性。而在大于等电点的碱性环境中,氨基酸的氨基解离使其带负电荷,呈酸性。20种氨基酸中,有8种是人体不能制造的,非得从食物中补充,称为必需氨基酸(essential amino acid)。必需氨基酸对人体的生命活动来说,是重要的生活物质。
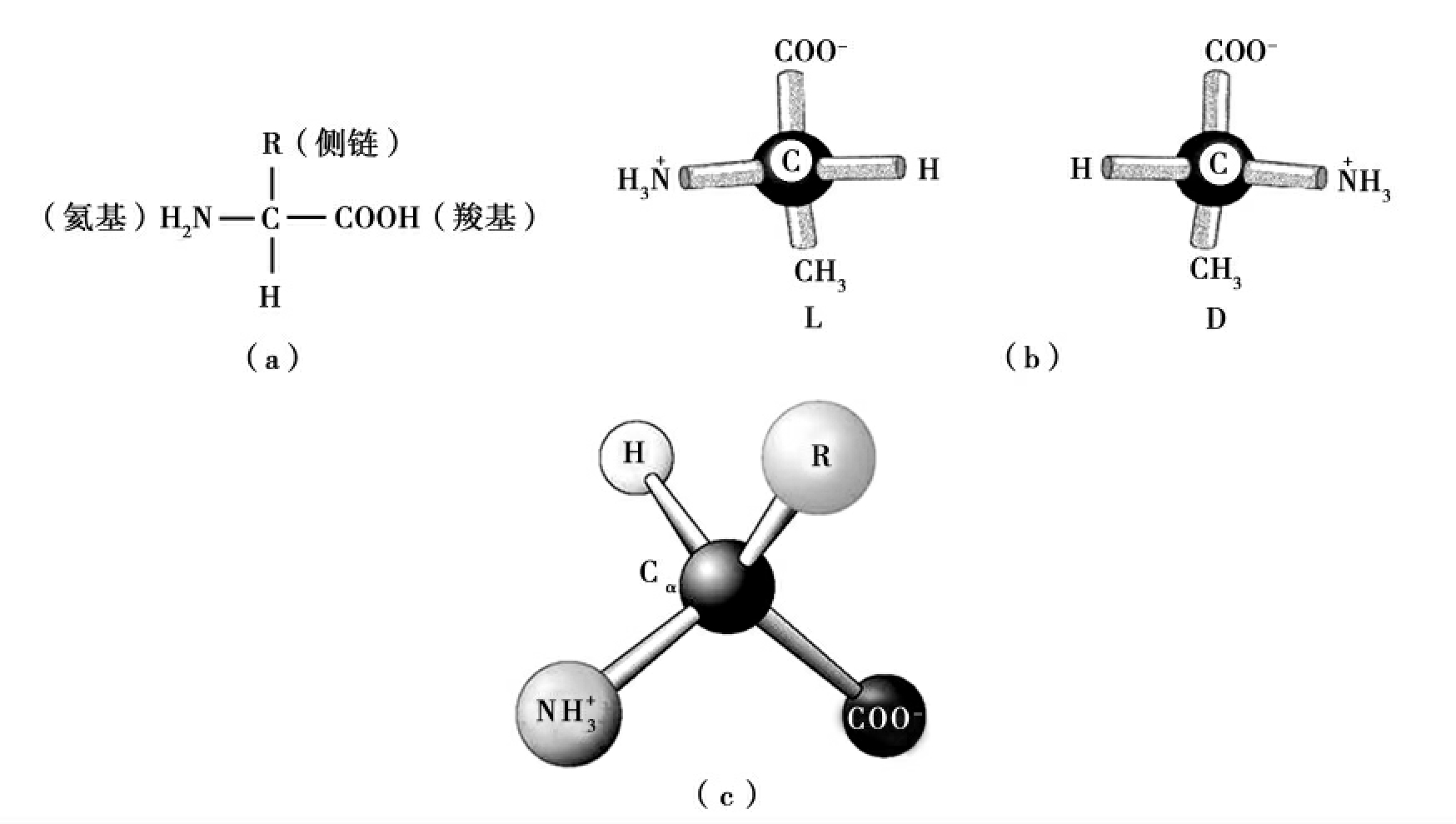
图2-17 氨基酸的基本结构
(a)各种氨基酸的α碳原子都连着一个羟基、一个羧基、一个氢原子和一个R基,因此,氨基酸的α碳为手性碳原子。(b)根据旋光性不同,氨基酸分为左旋(L)和右旋(D)两种,互为镜像。自然界构成蛋白质的氨基酸几乎都是L型的。(c)氨基酸是两性的。
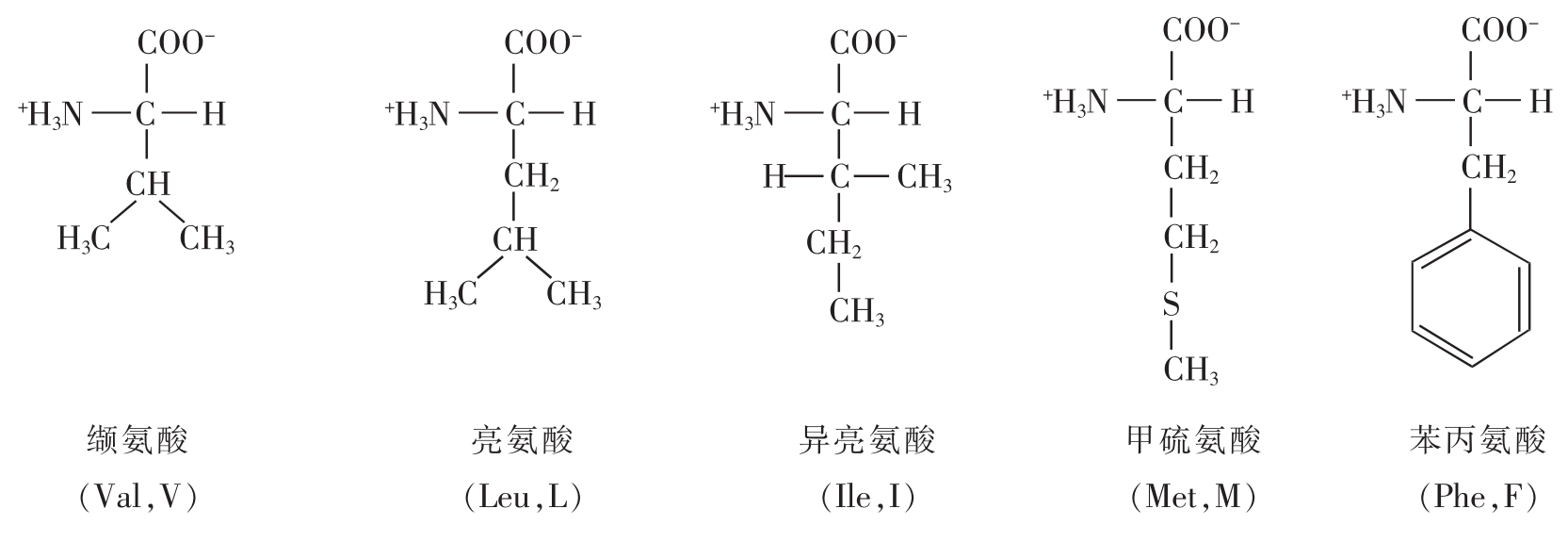
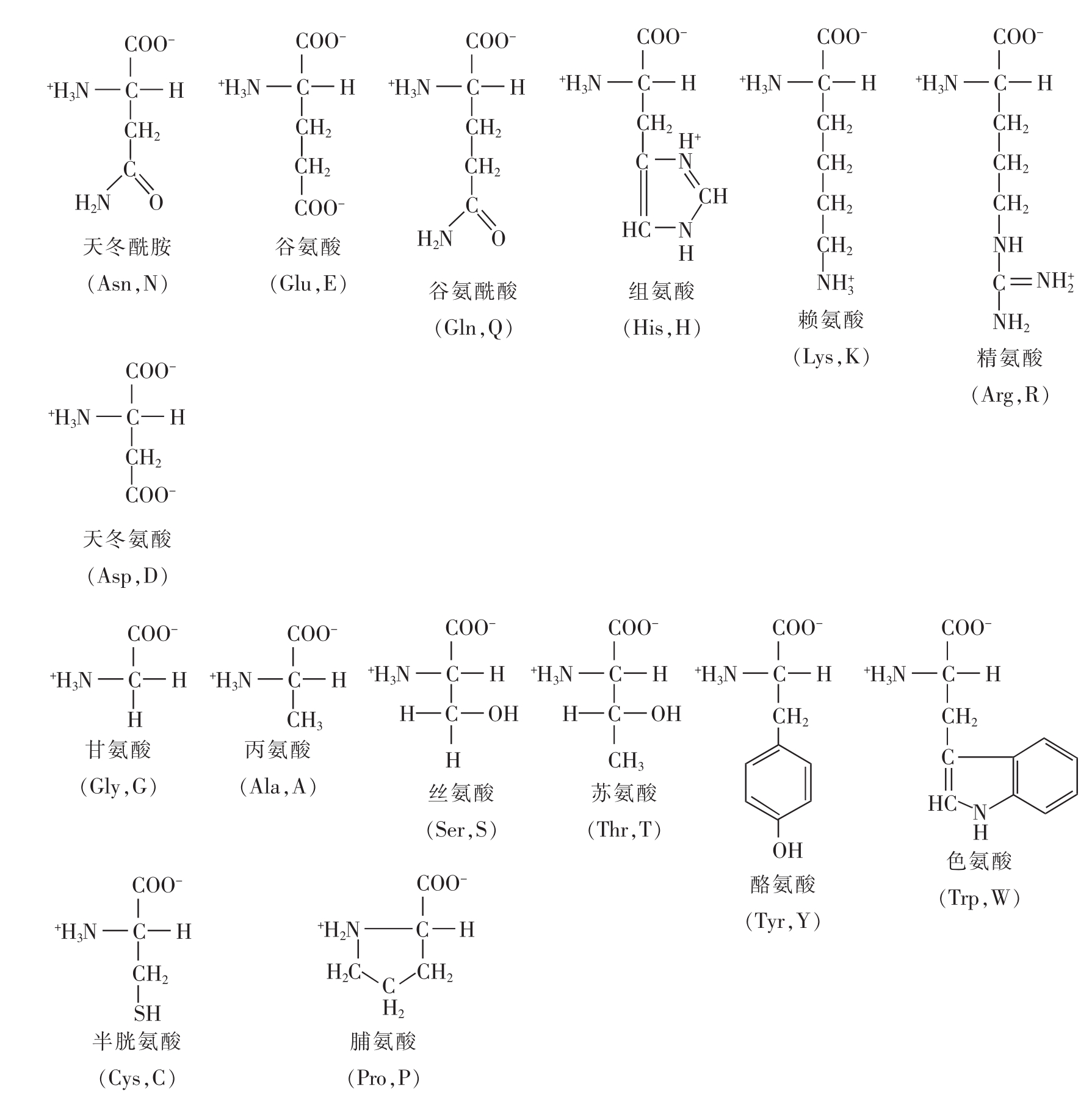
图2-18 生物体中的20种氨基酸
结构式下方为氨基酸的中文名,括号中为该氨基酸名称的3字母英文缩写和大写单字母。根据R基的化学性质,可以将氨基酸分为脂肪族氨基酸:甘氨酸(Gly,G)、丙氨酸(Ala,A)、缬氨酸(Val,V)、亮氨酸(Leu,L)、异亮氨酸(Ile,I)、脯氨酸(Pro,P);芳香族氨基酸:苯丙氨酸(Phe,F)、酪氨酸(Tyr,Y)、色氨酸(Trp,W);含硫氨基酸:甲硫氨酸(Met,M)、半胱氨酸(Cys,C);醇类氨基酸:丝氨酸(Ser,S)、苏氨酸(Thr,T);酸性氨基酸:天冬氨酸(Asp,D)、谷氨酸(Glu,E);碱性氨基酸:组氨酸(His,H)、赖氨酸(Lys,K)、精氨酸(Arg,R);酰胺类氨基酸:天冬酰胺(Asn,N)、谷氨酰胺(Gln,Q)。
2.蛋白质的分子结构
一个氨基酸分子中的α-氨基与另一个氨基酸分子中的α-羧基脱水缩合形成肽键(peptide bond),生成的化合物称为二肽(dipeptide)(图2-19)。不同数目的氨基酸以肽键顺序相连,这样形成的链状分子称为多肽(polypeptide)。组成肽链的氨基酸数目可以从几个到成千上万个不等,所以肽链的长短差异很大。多肽链的一端有一个氨基,另一端有一个羧基,一般写多肽链分子式时,将带有一个氨基(N末端)的那一端写在左侧,带有一个羧基(C末端)的那一端写在右侧。有些蛋白质分子只是一条多肽链,有些则是由几条多肽链组成,如胰岛素(insulin)由2条多肽链组成,血红蛋白(hemoglobin)由4条多肽链组成,细胞色素氧化酶由7条多肽链组成。决定功能的蛋白质空间结构可包括四个连续不同的结构水平,每一级决定了其更高一级的结构特点。
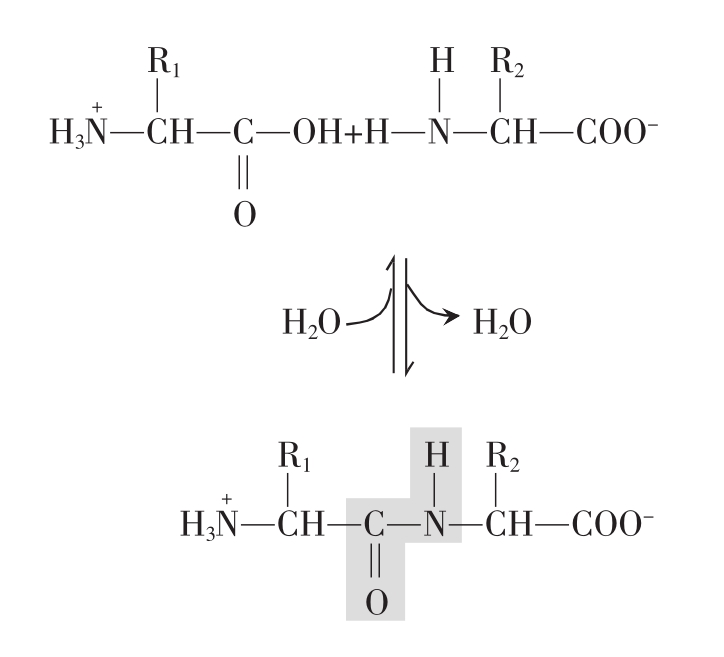
图2-19 氨基酸脱水缩合为二肽
一个氨基酸分子中的α-氨基与另一个氨基酸分子中的α-羧基脱水缩合形成肽键,生成的化合物称为二肽。
蛋白质的一级结构(primary structure)指组成某一多肽链的氨基酸的种类、数量和排列顺序。它是由基因决定的蛋白质的最基本结构,因此同源蛋白质一级结构的差别可反映出生物间的种属特异性和进化关系。如哺乳动物牛、猪、羊、鲸、人的胰岛素的A链的第8、9、10位上的3个氨基酸有差异,表现出了种属差异性。一般来说,一级结构中氨基酸序列的差别越小,它们的亲缘关系就越近。例如人和黑猩猩的细胞色素c的氨基酸序列相同,与兔的相差9个氨基酸,与鸡的相差13个氨基酸,与金枪鱼的相差21个氨基酸,与小麦的相差35个氨基酸,与酵母的相差44个氨基酸。蛋白质的一级结构决定了其二、三级和四级结构,改变一级结构可使二级结构和蛋白质功能发生变化。如镰刀形细胞贫血症病人的血红蛋白分子与正常人血红蛋白分子的主要差异在β链上第6位氨基酸残基,正常人为谷氨酸,病人则为缬氨酸。缬氨酸侧链与谷氨酸侧链的性质和在蛋白质分子结构形成中的作用完全不同,所以导致病人的血红蛋白结构异常,红细胞呈镰刀状,当红细胞脱氧时,这种镰刀状细胞明显增加。这种病人的血红蛋白使运输氧的能力减弱,引起贫血症状(图2-20)。另外,在生物体内的某些生化过程中,蛋白质分子的部分肽链要按特定方式先断裂,然后才能表现出生物活性。如凝血因子以无活性的前体或酶原的形式存在,一旦动物受到创伤而流血时,这些前体就在凝血因子作用下被激活,这个过程中就包含着氨基酸序列断裂使一系列酶原被激活,酶促激活的级联放大使血凝块迅速形成。又如人的胰岛素最初合成的是前胰岛素原,含有86个氨基酸残基,分为A、B、C三段,经胰蛋白酶作用后切去约30个氨基酸残基组成的C肽而转变为活性胰岛素。
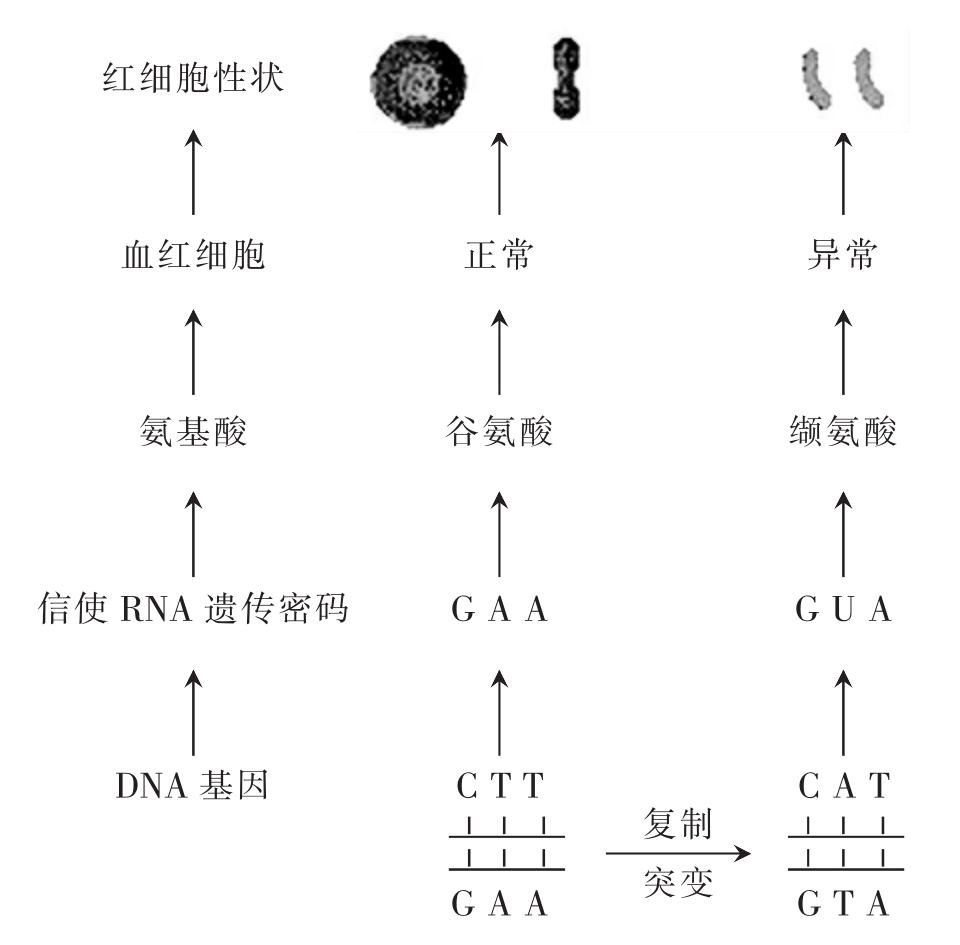
图2-20 镰刀形细胞贫血症血红蛋白异常
蛋白质的二级结构(secondary structure)是指多肽链主链折叠产生的由主链内和主链间周期性氢键维系的有规则的构象。常见的二级结构有α-螺旋(α-helix)和β-折叠(β-pleated sheet)(图2-21)。α-螺旋是蛋白质中最常见最典型、含量最丰富的二级结构,它的结构特点是主肽链围绕一个中心轴螺旋上升,每3.6个氨基酸残基上升一圈,沿螺旋轴方向上升0.54nm,大多为右手螺旋,氨基酸残基的R基在螺旋的外侧,每个氨基酸残基的N-H与前面第4个氨基酸残基的羰基间形成相邻螺旋圈之间的链内氢键。氢键的取向几乎与螺旋中心轴平行,是维系α-螺旋的主要作用力,若无法形成氢键则不能形成α-螺旋。如多聚赖氨酸在pH 7.0时R基带正电荷,彼此间由于静电排斥不能形成氢键,因此以无规则卷曲形式存在。又如脯氨酸所含的亚氨基参与了肽键的形成,无酰胺H原子形成链内氢键,从而使α-螺旋在脯氨酸处产生“结节”,螺旋被中断或拐弯。指甲、毛发以及动物的蹄、角、羊毛等中的纤维蛋白普遍呈α-螺旋。α-螺旋可被弯曲和回折而不断,拉伸后可以恢复原状,所以毛发等具有很好的弹性。β-折叠的结构特征是肽链几乎是完全伸展的重复性结构,肽链主链呈锯齿状,按层平行排列,形状如折叠的条状纸片侧向并排而成,肽平面并排成折叠形式,α-碳原子位于折叠线上,称为折叠片。相邻肽链肽键上的-CO-与-NH-形成链间氢键,以维持片层间结构的稳定。肽链的侧链基团都垂直于折叠片的平面,并交替地从平面上下两侧伸出,在平行(parallel)β-折叠片中,相邻肽链是同向的,在反平行(antiparallel)β-折叠片中,相邻肽链是反向的。平行β-折叠片比反平行β-折叠片更规则,反平行式结构更稳定。蚕丝中的丝心蛋白以β-折叠为主,所以蚕丝的弹性较差。另外,二级结构还有β-转角(β-turn)和无规则卷曲等。在β-转角中第一个氨基酸残基的C=O与第四个氨基酸残基的N-H氢键键合,形成一个紧密的环,目前发现的β-转角多数都处在蛋白质分子表面,在球状蛋白中的含量高。无规则卷曲存在少数柔性的无序区段,但这些区段也像其他二级结构一样是明确而稳定的结构,并非完全无规则,这类有序的非重复性结构经常构成酶活性部位和其他蛋白质特异的功能部位。蛋白质的二级结构还可组合成超二级结构(super-secondary structure),称为基序(motif)。最常见的组合形式是αα、βαβ、ββ。许多蛋白质都利用αα结构来直接与DNA双螺旋相结合,调控基因的功能。
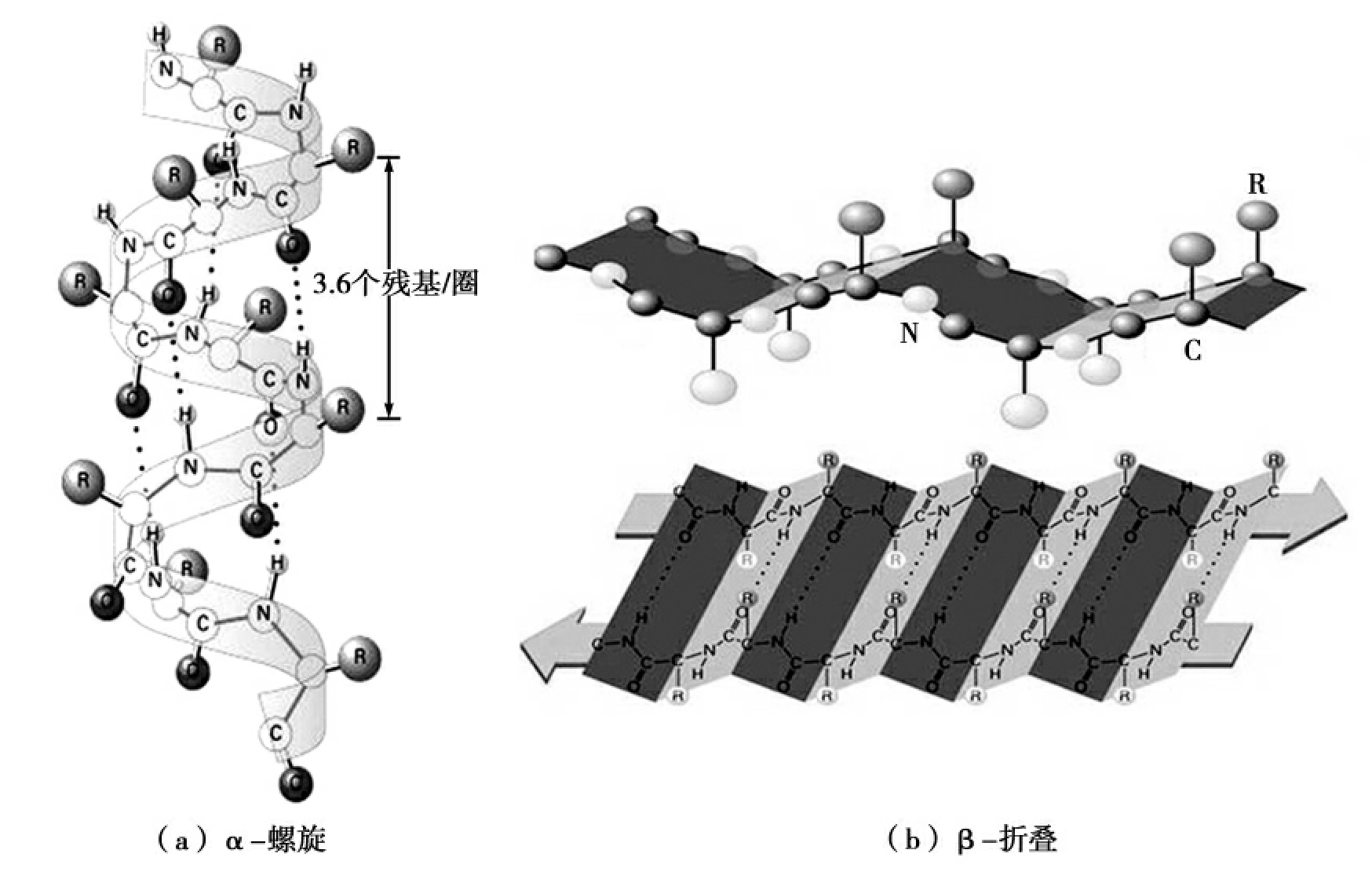
图2-21 蛋白质的二级结构
蛋白质的三级结构(tertiary structure)是指多肽链在二级结构基础上借助各种次级键(主要为疏水作用)构建成的盘绕或折叠的三维结构,包括一级结构中相距远的肽段之间的几何相互关系和侧链在三维空间中彼此间的相互关系。一般情况下呈球状或纤维状。三级结构中常常会有分立的、独立折叠的结构称为结构域(domain),结构域通常由在三级结构中相邻的基元组成。不同的蛋白质包括的结构域的数量并不相同。
许多蛋白质含有两个或更多的肽链,每一个或两个肽链都可组成蛋白质的一个亚基。蛋白质的四级结构(quaternary structure)是指寡聚蛋白质中以非共价键彼此缔合在一起的各亚基形成聚集体的方式。每一个亚基都有它的一级、二级和三级结构(图2-22)。组成四级结构时,各亚基可以是相同的肽链,也可以是不同的肽链。如血红蛋白是由四个亚基组成,包括两个相同的α-亚基和两个相同的β-亚基。胶原蛋白是有三条螺旋肽链缠绕形成的超螺旋。稳定蛋白质四级结构的作用力主要是一些弱的相互作用力,或称非共价键或次级键,包括氢键、范德华力、疏水作用和离子键。这些弱的相互作用力也是稳定核酸构象、生物膜结构的作用力。此外共价二硫键在稳定某些蛋白质构象方面也有重要作用。蛋白质空间结构的变化也必然影响到蛋白质的功能。如血红蛋白是执行运输氧的功能时发生的空间结构的变化称为变构作用(allosteric effect),使得血红蛋白的氧亲和力发生改变,从而完成氧的结合和释放。又如蛋白质在一些物理或化学因素作用下解开多肽链的盘绕和折叠,使其空间结构发生改变,从而使蛋白质丧失生物活性的过程称为蛋白质变性过程(denaturation)。引起变性的因素有很多,包括加热、紫外线、超声波、强酸、强碱等,其中加热是最常用的处理方式。
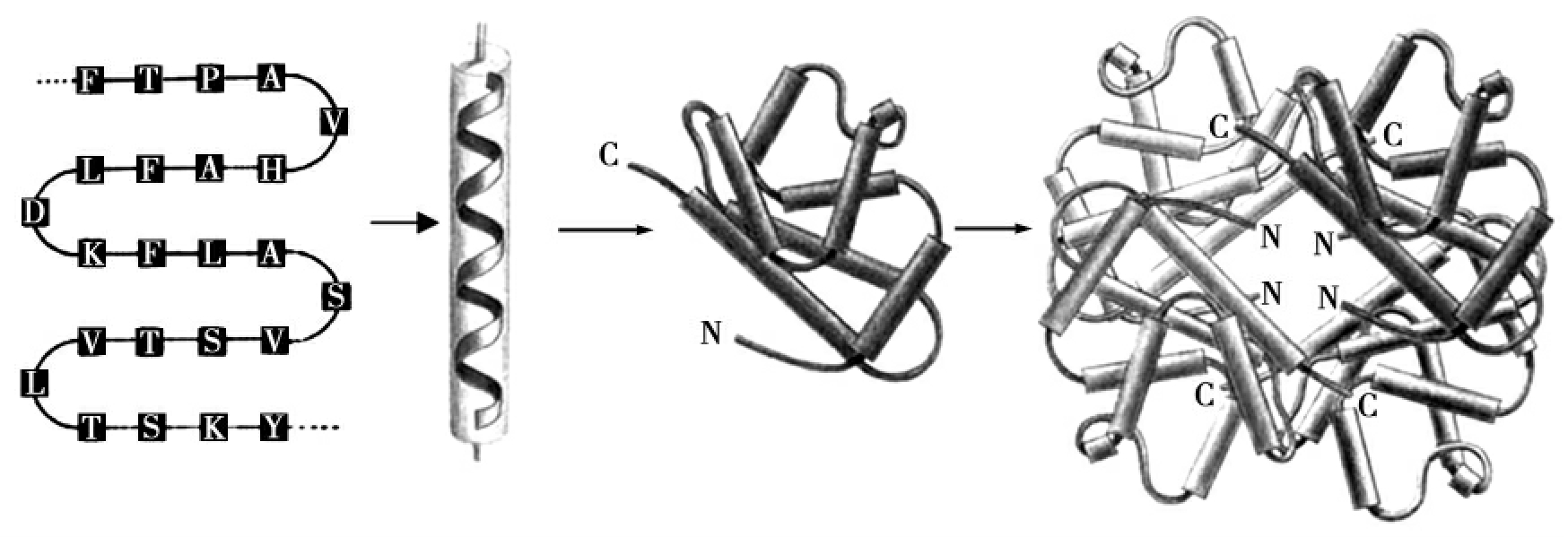
图2-22 蛋白质的四级结构模型
蛋白质的一级结构指组成某一多肽链的氨基酸的种类、数量和排列顺序。二级结构指主链的构象,主要有α-螺旋和β-折叠。已具有二级结构的多肽链进一步折叠成三级结构。如果蛋白质是由二条或多条肽链组成,这些肽链不是通过共价键而是次级键结合在一起的,这样的蛋白质具有四级结构。
3.蛋白质的种类和功能
由于蛋白质的结构非常复杂,很多蛋白质的化学结构尚未阐明,目前还很难根据其结构加以分类,一般是依照它们的组成成分分为单纯蛋白(如清蛋白、球蛋白、组蛋白等)和结合蛋白。单纯蛋白指那些只含有氨基酸组成成分的蛋白质;结合蛋白是其蛋白质分子中除了含有氨基酸这一成分外,还有辅基。辅基可以是糖类、脂类、磷酸、核酸等。相应这些结合蛋白分别称为糖蛋白、脂蛋白、磷蛋白和核蛋白。生物体中的蛋白质大都属于结合蛋白,其中核蛋白最为重要,细胞核内含量最多。在生物体生命活动中起着极其重要的作用。
蛋白质是重要的生命活性物质,按功能主要分为结构蛋白、贮存蛋白、保护蛋白、运输蛋白、伸缩蛋白、信号蛋白等。还有可以催化生物体内各种复杂化学反应的酶是特化了的蛋白质。如人体和哺乳动物骨骼和皮肤之所以具有高抗张强度,也是由一种胶原纤维蛋白的作用产生的结果,属于结构蛋白。动物和人体抵御外界致病微生物入侵的重要免疫保护物质——抗体,也是一些高度专一性的蛋白质,属于保护蛋白;人体血液中的红细胞的血红蛋白和肌肉中的肌红蛋白都是运输氧的蛋白质,属于运输蛋白;肌动蛋白和肌球蛋白的相互协调滑动才出现肌肉的收缩,属于伸缩蛋白;感受光刺激和神经冲动的受体也是一些专一的蛋白质,调节机体生长、发育和代谢的一些激素也是蛋白质,这些属于信号蛋白;除此之外,人们也常根据蛋白质分子的形状,将蛋白质分为球蛋白(globulin)和纤维蛋白(fibrin)。球蛋白分子似球形,较易溶解,如血液的血红蛋白,豆类球蛋白等。纤维蛋白形状似纤维,不溶于水,如指甲、羽毛中的角蛋白,蚕丝的丝蛋白和胶原蛋白等。
四、核酸
核酸(nucleic acid)是生物体内一类含有磷酸基团的重要生物大分子,其主要作用是遗传信息的储存和传递。C、H、O、N、P是组成核酸的主要元素。核酸中P的含量较恒定,质量分数约为9%~10%,因此可以用定P法来测核酸的含量。核酸包括脱氧核糖核酸(DNA)和核糖核酸(RNA)两类。贮存遗传信息的特殊DNA片段称为基因(gene),它主要编码蛋白质的氨基酸序列,从而决定蛋白质的功能。通过蛋白质的作用,DNA实际上控制着细胞和生物体的生命过程。DNA控制蛋白质的合成是通过RNA来实现的,即遗传信息由DNA转录到RNA,后者决定蛋白质的氨基酸序列。
1.构成核酸的结构单元——核苷酸
核酸是多聚核苷酸,它的基本结构单位是核苷酸(nucleotide)。每一个核苷酸单体由一个戊糖分子、一个磷酸和一个含氮碱基三部分组成。含氮碱基分为两类:一类是嘌呤,为双环分子,包括腺嘌呤(A)和鸟嘌呤(G)2种;一类是嘧啶(pyrimidine),为单环分子,包括胸腺嘧啶(T)、胞嘧啶(C)和尿嘧啶(U)3种(如图2-23)。DNA的碱基是A、T、G、C,RNA的碱基是A、U、G、C。戊糖分子上第1位碳原子上的羧基与嘌呤第9位氮原子上的氢或嘧啶第1位氮原子上的氢缩合,失去1分子水,就成为核苷。如果戊糖是β-D-2-脱氧核糖,形成的核苷就是脱氧核苷;如果戊糖是β-D-核糖,形成的核苷就是核糖核苷。一个核苷或一个脱氧核苷与一个磷酸分子结合,就成为一个核苷酸或脱氧核苷酸,也可称为一磷酸核苷,如一磷酸腺苷(AMP)和一磷酸脱氧腺苷(dAMP),这里的“d”表示脱氧之意。若在一磷酸腺苷(AMP)的磷酸一侧以高能磷酸键再连接1个磷酸,就成了二磷酸腺苷(ADP),如连接2个磷酸就成了三磷酸腺苷(ATP)。ATP是细胞中的能量分子。每一种核苷酸都可在环化酶的作用下生成环式的一磷酸核苷。例如,ATP在腺苷酸环化酶的催化下生成cAMP,对于介导激素及调节细胞生命活动的许多方面起到重要的作用。磷酸与核糖或脱氧核糖结合的部位通常是核糖或脱氧核糖的第3位碳原子。多个核苷酸以磷酸顺序相连而成长链的多核苷酸分子,即成核酸的基本结构。细胞中重要的二核苷酸有烟酰胺腺嘌呤二核苷酸(NAD+)、烟酰胺腺嘌呤二核苷酸磷酸(NADP)、黄素腺嘌呤二核苷酸(FAD)等。
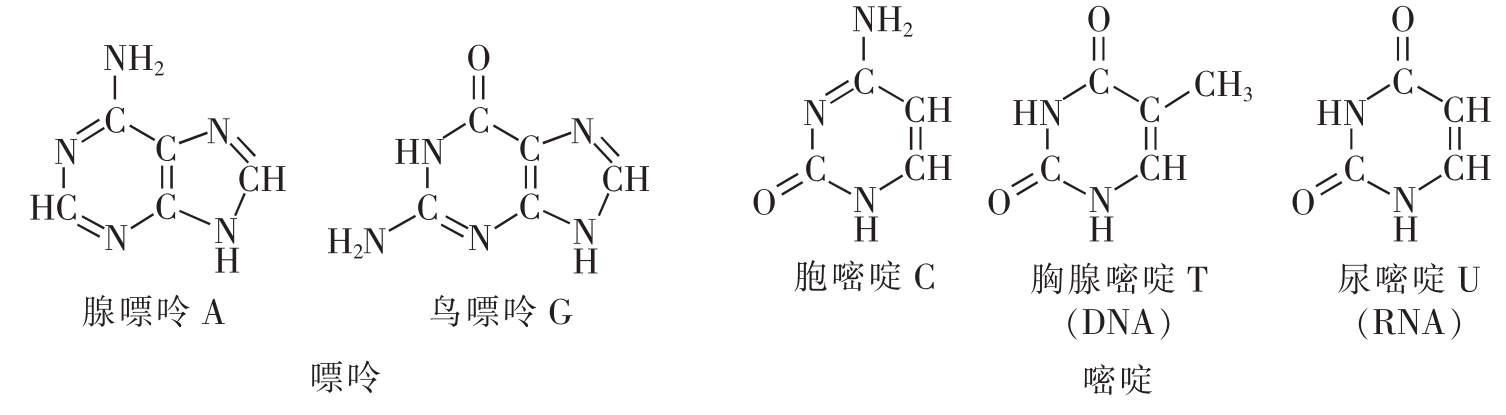
图2-23 核苷酸中的碱基
含氮碱基分为两类:一类是嘌呤,为双环分子;一类是嘧啶,为单环分子。嘌呤包括腺嘌呤(A)和鸟嘌呤(G)2种,嘧啶有胸腺嘧啶(T)、胞嘧啶(C)和尿嘧啶(U)3种
2.DNA的双螺旋结构
DNA在原核细胞中集中在核区。真核细胞中的分布在核内,组成染色体(染色质)。线粒体、叶绿体等细胞器也含有DNA。病毒或含有DNA,或含有RNA,尚未发现两者兼有的病毒。美国分子生物学家沃森(J.D.Watson)和英国分子生物学家克里克(F.H.C.Crick)在前人工作的基础上,提出了DNA双螺旋结构的模型。DNA分子双螺旋结构模型表明:DNA分子是由两条多核苷酸链沿共同的纵轴螺旋平行盘绕,形成双螺旋。螺旋直径2nm,沿纵轴相邻碱基之间相距0.34nm并转角36°。10个碱基组成一个螺旋重复延伸,每个螺旋长3.4nm。两条多核苷酸链的骨架(磷酸及糖)方向相反,核苷酸链带完整磷酸的一端是5'端,带完整羟基的一端是3'端。习惯上以3'到5'为正向。两条多核苷酸链一条是5'到3'方向,另一条则是3'到5'方向。磷酸基团及糖在螺旋表面,碱基位于螺旋内部,碱基的平面与纵轴垂直,糖平面几乎与碱基平面垂直。两条多核苷酸链由彼此碱基间形成氢键而吸引在一起,腺嘌呤与胸腺嘧啶配对,由两个氢键相连,鸟嘌呤与胞嘧啶配对由三个氢键相连,这种碱基之间互相匹配的情形称为碱基互补(complementary)(如图2-23)。在多核苷酸链中碱基的顺序各不相同,具体碱基的顺序即是遗传信息。当一条多核苷酸链的顺序确定以后,根据碱基互补配对原则即可确定另一条互补的多核苷酸链的碱基顺序。DNA的自我复制、转录及反转录的分子基础都是碱基互补。这一模型不仅与前人研究工作所取得的结果相吻合,同时也很好地解释了遗传物质DNA自我复制和信息传递机制。后来的许多实验都证明了这一模型的正确性。
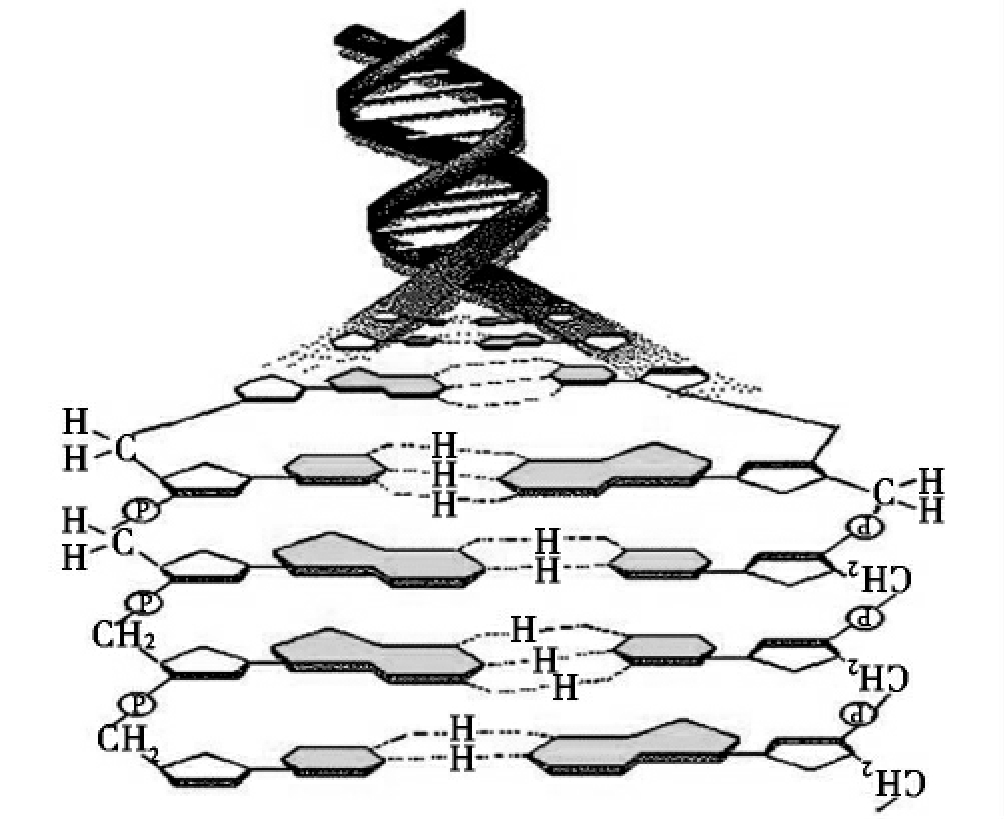
图2-23 DNA双螺旋结构
在DNA双螺旋分子中,一个核苷酸分子中戊糖的C3与相邻的另一个核苷酸分子中戊糖的C5的磷酸之间依次相连接,形成长链。长链中各个核苷酸分子的顺序构成核酸分子的一级结构。在DNA分子中,两条脱氧核糖核酸链反向平行,由彼此碱基间形成氢键而吸引在一起,腺嘌呤与胸腺嘧啶配对,由两个氢键相连,鸟嘌呤与胞嘧啶配对,由三个氢键相连。
3.RNA
RNA有几种类型:信使RNA(messenger RNA)、核糖体RNA(ribosomal RNA)、转运RNA(transfer RNA),它们基本上是单链。每种类型的RNA在蛋白质合成中起着不同的作用:信使RNA作为细胞中DNA指导下蛋白质合成的信息携带者,在肽链合成中决定氨基酸排列顺序,约占细胞RNA总量的5%;核糖体RNA作为核糖体(核糖体是蛋白质合成的场所)的结构组分,约占细胞RNA总量的80%,相对分子质量较大;而转运RNA则将氨基酸转移到核糖体上,以便使其结合成蛋白质(图2-24),约占细胞RNA总量的15%,相对分子质量较小,游离在细胞质中。
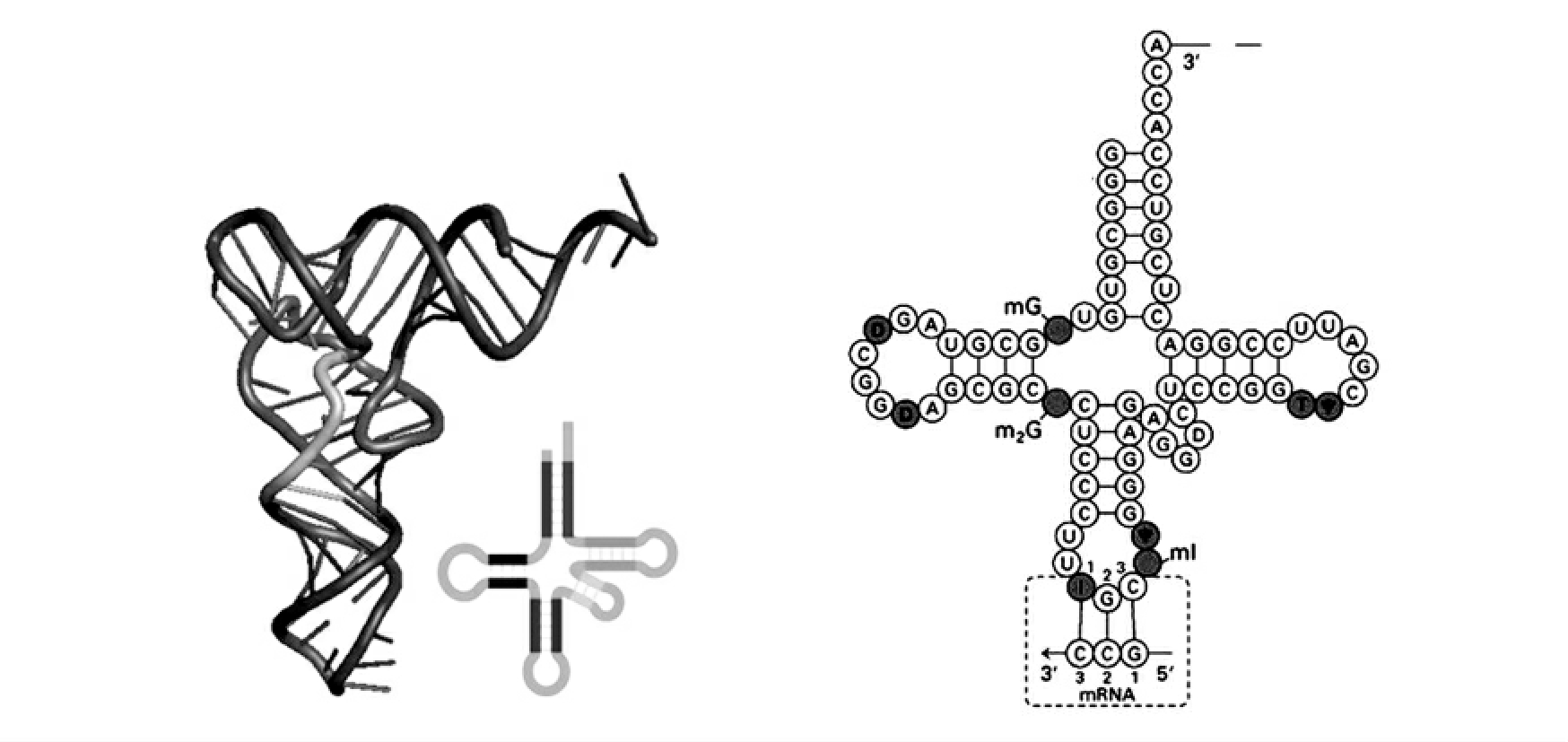
图2-24 tRNA分子结构
左图为空间结构,右图为结构组成。tRNA分子由约75个核苷酸组成,相对分子质量为25000。所有tRNA分子的一级结构经链内互补形成三叶草形的二级结构。
思考题:
1.组成生命的主要元素有哪些?它们有什么特点?
2.生物体中的化学键主要有哪些?它们是怎么形成的?
3.水有哪些主要特征?水分子的结构有什么特点?
4.生物体中的无机盐主要有哪些?无机盐的主要作用是什么?
5.生物大分子有哪些主要种类?
6.何为单糖,它的主要种类有哪些?糖类在有机体中有什么作用?
7.脂类有哪些主要的种类?它们分别有什么作用?
8.蛋白质有几级空间结构?
9.DNA和RNA的主要区别是什么?
10.请叙述DNA分子的右手双螺旋结构。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。













