利用金属膜提取L-缬氨酸工艺研究
徐庆阳1 刘淑云1 陈宁1,2
(1.天津科技大学生物工程学院; 2.天津市工业微生物重点实验室 天津 300222)
摘要:研究了金属膜过滤的各种操作参数对L-缬氨酸过滤效果的影响,综合各方面因素确定了最适工艺条件:进出膜压力分别为4.0MPa和3.0MPa,过滤温度为25℃,过滤液pH为3.0。在此操作条件下,蛋白去除率达到87.36%,色素去除率达48.61%,L-缬氨酸收率达90.2%。
关键词:金属膜;色素去除率;蛋白去除率; L-缬氨酸
L-缬氨酸发酵液中存在着大量的菌体和杂蛋白,这些物质的存在使L-缬氨酸收率和结晶质量下降。因此,在进行L-缬氨酸分离前必须先将其除去。 L-缬氨酸发酵液黏度大,细菌菌体细胞小,难于沉降,离心法能耗大,操作繁杂,速度慢,投资大,综合各方面的因素本实验选择膜过滤方法。
目前经常使用的过滤方法有微滤法、超滤法、中空纤维膜过滤、陶瓷膜过滤和金属膜过滤。用微滤法和中空纤维膜除去细胞碎片,易产生膜阻塞。聚丙烯酰胺絮凝剂中存在少量的单体,存在一定的毒性,不适合用于食品和医药。絮凝剂有很强的吸附作用,在吸附沉降过程中有部分氨基酸被吸附;加入絮凝剂的同时又引入新的杂质。
L-缬氨酸发酵液黏度大,细菌菌体细胞小,难于沉降,离心法能耗大,操作繁杂,速度慢,投资大,综合各方面的因素本实验选择膜过滤方法。
膜分离技术是近年来发展较快的一门新兴高效分离技术。随着膜材料、膜分离装置的不断改进以及应用领域的拓展,膜分离技术已成为重要的化工单元操作,正在引起分离技术的重大变革[1]。金属膜微孔材料是一种孔径小、分布均匀、孔隙度高、厚度薄、表面光滑的过滤分离材料,结构由骨架层和工作层两部分组成,前者有足够的机械强度起支撑作用,后者起过滤分离作用。金属膜在超纯分离、反应催化、生物环保以及电子、核能、医药、食品等领域的超纯气体净化、气相分离、无菌过滤和微(超)滤等方面显示出巨大的发展潜力[2~6]。
1 材料与方法
1.1 材料
金属管式膜分离中试设备:凯能高科技工程(上海)有限公司。
L-缬氨酸发酵液:天津科技大学代谢控制发酵研究室提供。
1.2 分析测定
1.2.1 可溶性蛋白质的测定
将样品溶液在280nm和260nm波长测定其吸收值,求出两者的比值,并从校正因子表求得相应的校正因子[9]。蛋白质含量(mg/ml) =A280*校正因子。因校正因子为一常数,因而去除蛋白的效果可以通过A280反映出来。
1.2.2 色素去除率的测定
L-缬氨酸发酵液一般为黄褐色,于480nm处有最大吸收值,故直接吸取稀释发酵液,于480nm处测透光率即可。
1.2.3 L-缬氨酸的测定
采用纸层析法、比色定量法[7,8]。
1.3 操作方法
金属膜法:将处理好的发酵液装入设备罐体,在一定的操作条件下,过滤得到澄清的发酵液,测定其蛋白去除率和色度去除率。
2 结果与讨论
2.1 不同过滤方法的过滤效果比较
发酵液通过絮凝法、离心法和金属膜过滤法处理后,处理效果见表1。
表1 各种过滤方法的蛋白去除率比较
![]()
从表1可以看出,离心和金属膜的过滤效果较好,但若用离心法,由于菌体细胞很小,尤其细菌比酵母和霉菌都小,更难于沉降,则能耗大,离心法操作繁杂,速度慢,而且投资也比较大,综合各方面的因素选择膜过滤方法较好。
2.2 进出膜压差对金属膜过滤的影响
金属膜过滤的方式是错流过滤,错流过滤能够过滤浑浊度较高的液体,其作用方式是:液体以切线方向流过膜表面,经过膜表面时产生的剪切力可使沉积在膜表面的混浊颗粒扩散回主体流,从而使膜表面污染层保持在一个较薄的稳定水平,防止出现快速堵塞。压力的变化可影响到膜表面污染层的厚度,所以在过滤过程中对过滤的速度等有影响。在研究压力对金属膜过滤结果的影响时,由于主要差别在于进出膜的压差,而金属膜的耐压性特别好,所以在过滤过程中能耐受较大的压力和压差。这套中试设备可耐压70MPa,在发酵液过滤中,为节省能耗选择的压力为4.0 MPa以下;考虑到过滤速率,进出膜压差应保持在0.4 MPa以上。不同压力及压差对缬氨酸过滤效果见表2。
表2 不同压差对缬氨酸的过滤效果
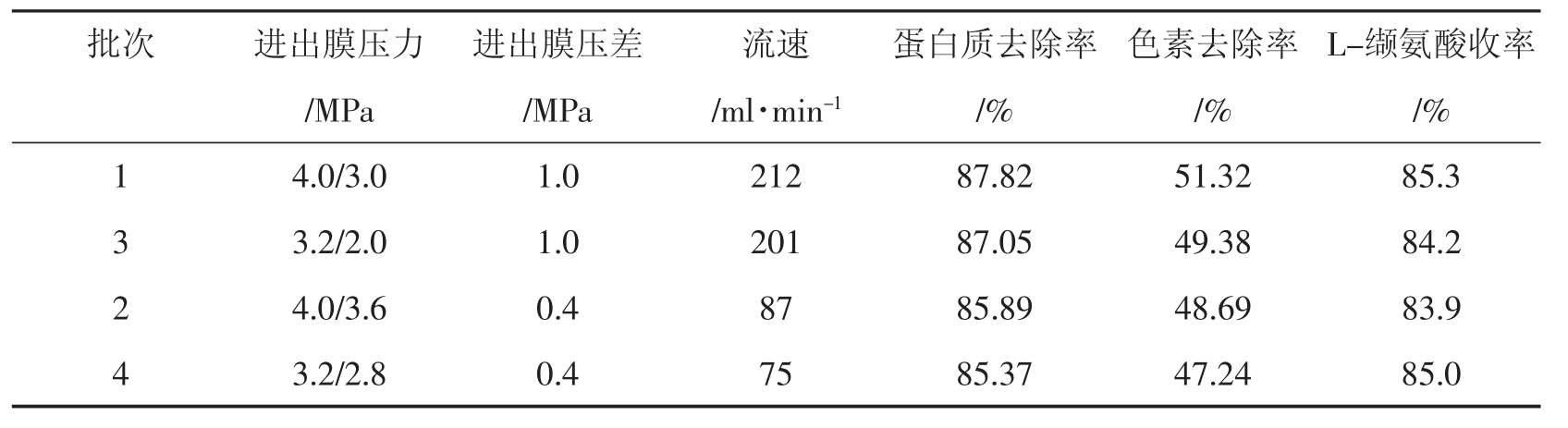
从表2可以看出,过滤压力和压差的高低对蛋白质去除率、色素去除率、L-缬氨酸收率都没有很大的影响,但对流速影响较大,当压力和压差都很低时,过滤速度就小,特别到了后期,过滤速度会变得更小,影响到过滤时间,直接影响到过滤的效率,所以,选择较高的压力和压差,这里选择批次1的操作条件较好。
2.3 温度对金属膜过滤的影响
过滤温度升高时,L-缬氨酸发酵液的粘度降低,发酵液的雷诺系数变大,膜表面流动速率增大,膜表面剪切力增大,使滤层变薄,因而过滤速率增加。本实验研究了不同的过滤温度对L-缬氨酸发酵液的蛋白质去除率和色度去除率影响,并测定了不同温度下的L-缬氨酸收率,结果见表3。
表3 不同的过滤温度对过滤的效果的影响
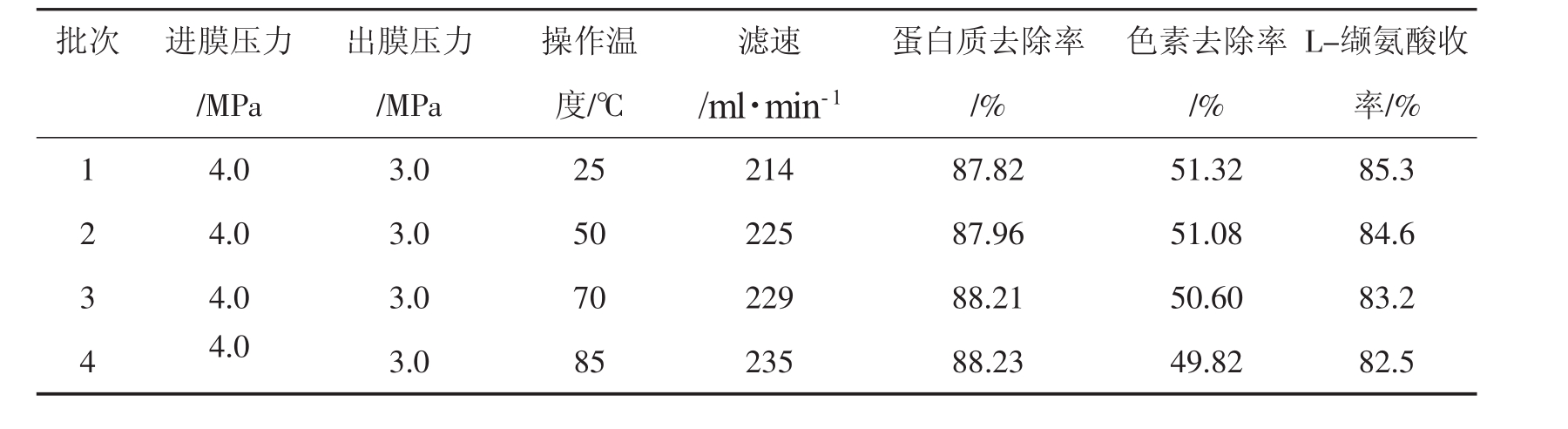
从表3可看出,过滤温度升高,色素去除率、L-缬氨酸收率降低,因为温度越高发酵液中产生的反应就越多,致使色素加深,也使L-缬氨酸收率稍许降低,温度升高对流速也有一定的影响。考虑到高温度的控制需消耗循环水和大量的能源,选择25℃进行分离。
2.4 L-缬氨酸发酵液pH变化与过滤质量的关系
发酵结束后,L-缬氨酸发酵液pH约为7.2。pH的变化对蛋白质有较大的影响,蛋白质在一定的pH条件下可以沉降,而且pH可影响到后面的树脂处理,而在进行树脂处理时,选择pH为3.0。L-缬氨酸发酵液pH变化与过滤效果的关系见表4。
表4 不同pH对L-缬氨酸发酵液过滤效果影响
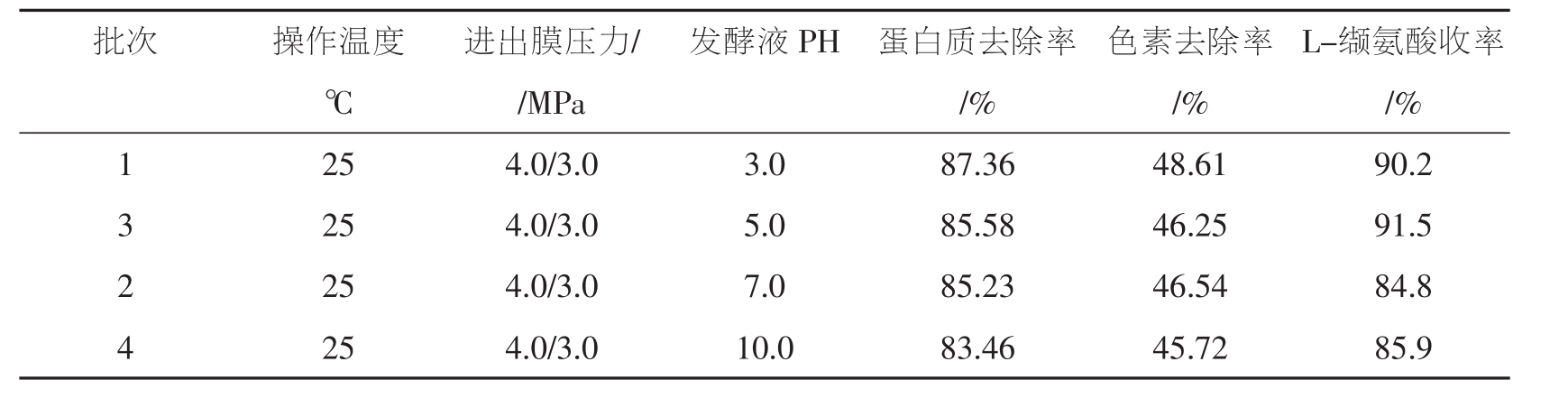
从表4可以看出,pH对发酵液的蛋白去除率、色素去除率和L-缬氨酸收率影响不大,但是滤过液pH为3.0时,所选树脂有最大静态吸附量,因而本实验选择pH为3.0,此时,蛋白去除率为87.36%,色素去除率为48.61%,L-缬氨酸收率为90.2%。 pH为5.0时,L-缬氨酸有最大收率91.5%。
2.5 助滤剂对金属膜过滤的影响
发酵液中加入助滤剂,可以使过滤滤饼疏松,减少过滤的阻力,因而可以提高过滤液的流速,同时助滤剂对发酵液中的蛋白、色素等杂质有吸附作用,但是助滤剂也对L-Val有吸附作用,影响收率。本文以硅藻土为助滤剂,其对金属膜过滤效果的影响如表5所示:
表5 硅藻土对L-缬氨酸发酵液过滤效果影响
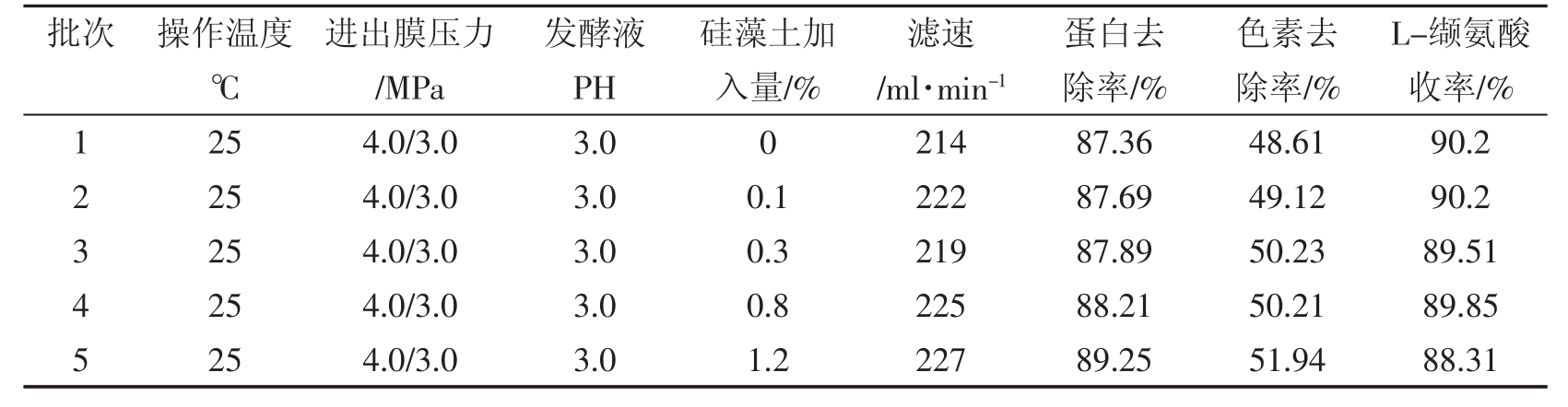
从表5可以看出,加入助滤剂以后,滤速变化不大,影响很小,蛋白去除率和色素去除率随着硅藻土加入量的增加而增大,L-缬氨酸收率则减小,截留液可以作为饲料,加入硅藻土后,影响饲料的质量,综合考虑,不加任何助滤剂。
2.6 金属膜过滤对树脂吸附量的影响
由于发酵液中含有大量的菌体、蛋白等杂质,对后续分离纯化工艺有较大的影响。在此考察了金属膜过滤对树脂吸附量的影响。
L-缬氨酸分离提取应选用强酸性阳离子交换树脂,本实验选用了5种离子交换树脂进行静态吸附实验,取金属膜过滤前后的发酵液作比较,测定各种树脂对L-缬氨酸的静态吸附量。实验结果见表6。
表6 不同树脂对L-缬氨酸的吸附量
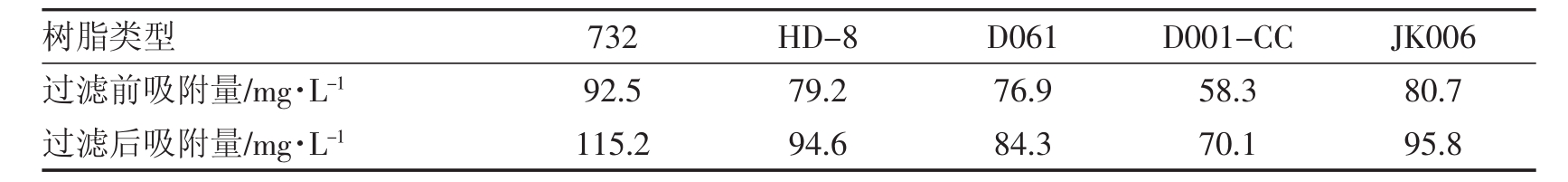
注:料液pH=3;平衡时间10h
从表6可以看出,不论是哪种树脂在经过金属膜处理后的吸附量明显大于过滤前的吸附量,主要是因为过滤前有蛋白质等存在的影响。所以在树脂吸附前应进行膜过滤处理。
3 结论
(1)本实验的最适操作参数:进出压力分别为4.0MPa和3.0MPa,过滤温度为25℃,过滤液为pH3.0。在此条件下,蛋白去除率为87.36%,色度去除率为48.61%,过滤单元收率90.2%,不用加助滤剂,膜两侧压力差是影响过滤速率的主要因素。
(2)本实验过滤单元最高收率为91.5%,主要原因是所用设备死体积较大(5L) ,提供的发酵液量较少,导致发酵液过滤过程中不能浓缩到终点,透析不完全。随着工业化的放大,过滤单元收率会有很大提高。
参考文献:
[1]王学松.腹分离技术及其应用[M].北京:科学出版社,1994
[2]尤新,李红兵.发酵工业面临的问题与采用膜分离技术的前景[J].膜科学与技术,1997,17 (4):8~13
[3]郝彤.赛普特不锈钢膜分离系统及应用.膜科学与技术[J],1998,18 (6):25~27
[4] nEUMANp,RohligR.KohstoβA,et al. Metallic membranes[J]. Filtration Sep.,1998,35 (1) :40~42
[5]汪洪生,陆雍森.国外膜材料及膜工艺进展[J].污染防治技术,1999,12 (2) : 111~113
[6]黄仲涛,曾昭愧,钟邦克,等.无机膜技术及其应用[M].北京:中国石化出版社,1999
[7]张伟国,钱和. L-缬氨酸菌种选育[J].无锡轻工大学学报,1995,14 (3):221~224
[8]赵丽丽,陈宁,熊明勇,等.利用神经网络对L-缬氨酸发酵建模[J].无锡轻工大学学报,2003,22 (2) :44~47
[9]南京药学院主编.分析化学[M].北京:人民卫生出版社,1979
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















