【目的要求】 硝酸还原酶是植物氮素同化的关键酶,也是一种诱导酶,与作物吸收和利用氮肥有关,其活性可反映植物的氮代谢状况。
【实验原理】 硝酸还原酶可催化硝酸盐还为亚硝酸盐:
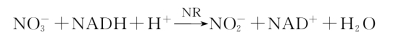
产生的NO-2在酸性条件下可以与对氨基苯磺酸(sulfanilic acid)或磺胺(对-氨基苯磺酰胺,sulfanil-amide)反应生成重氮盐,再与α-萘胺反应生成红色偶氮化合物(对苯磺酸-偶氮-α-萘胺)。
生成的红色偶氮化合物在520nm波长下有最大吸收值,可用分光光度法测定,并计算出亚硝态氮含量。硝酸还原酶活性可以每小时每克鲜重产生的NO-2微克数表示酶活性[μg/(g· h)]。
根据材料处理不同可分为活体法与离体法,根据反应介质的不同则可分为内源基质法和外源基质法。活体法步骤简单,适合快速、多组测定。离体法复杂,但重复性较好。内源基质法测定结果可反映硝酸还原酶在实际生长条件下的还原力,而外源基质法测定结果则可反映硝酸还原酶的潜在或最高还原力。
【实验方法】
1.活体法
(1)实验材料与仪器设备
①实验材料:欲测植物材料(如叶类药用植物,实验材料在实验前一天可用硝态氮肥处理,以增强硝酸还原酶活性)。
②仪器设备:分光光度计、真空泵、真空干燥器、天平(感量0.1mg)、恒温培养箱、三角瓶(50ml)、1ml移液管、5ml移液管烧杯、10ml试管、试管架、直径1cm打孔器。
③试剂:0.1mol/L pH 7.5磷酸缓冲液(Na2HPO4·12H2O取30.090 5g与Na2HPO4· 2H2O取2.496 5g,用蒸馏水定容至1 000ml)、30%的三氯乙酸(30g三氯乙酸,水溶后定容至100ml)、0.2mol/L KNO3(20.22g KNO3用蒸馏水定容于1 000ml)、磺胺试剂(1g磺胺,加25ml浓盐酸,用蒸馏水定容于100ml)、α-萘胺试剂(0.2gα-萘胺,用含1ml浓盐酸的蒸馏水定容于100ml)、5μg/ml NO-2标准液(0.10g NaNO2用蒸馏水定容至100ml,吸取7.5ml,再用蒸馏水定容至1 000ml)。
(2)实验内容与方法
①标准曲线制作:取7支10ml刻度试管,按表3-3顺序加试剂,并处理。
表3-3 制作标准曲线
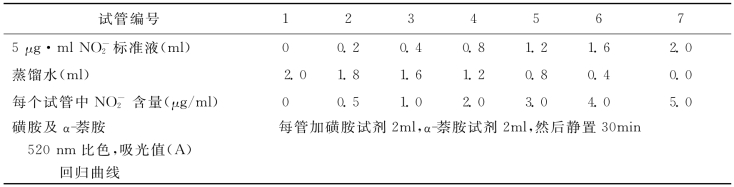
注:可用坐标纸制作标准曲线
②取新鲜植物组织洗净,拭干。如果是叶片可去主脉,打成直径1cm的圆片,若是根、茎可切成0.1cm厚的薄片。
③取上述材料4份,每份50片,称重后分别放入4个50ml三角瓶中,其中1个为空白,3个用于酶活性测定,分别记为重复1、2、3。
④在空白瓶中先加1ml 30%三氯乙酸,然后在每个三角瓶中加入0.1mol/L pH 7.5磷酸缓冲液5ml、蒸馏水5ml(内源基质法)。如果是外源基质法,则将蒸馏水换为5ml 0.2mol/L KNO3。
⑤将三角瓶置于真空干燥器中抽气至样品完全沉入溶液中(约10min)。
⑥取出三角瓶,30℃避光30min;之后在重复中也分别加入1ml 30%的三氯乙酸以终止反应,摇均。
⑦吸取2ml(若反应液浓度太大,可吸取1ml加1ml水)反应液于10ml试管中,加磺胺试剂2ml,α-萘胺试剂2ml,静置30min;比色,记下吸光值(A)(表3-4);
表3-4 吸光值记录表

⑧从标准曲线中检出NO-2含量(μg/ml),以每小时每克鲜重产生的NO-2微克数表示酶活性,计算方法:
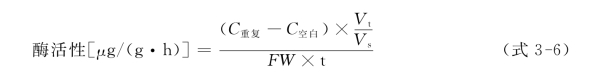
式中:C为根据回归曲线计算的NO-2μg数;Vt为反应液总体积(ml);Vs为测定时取样体积(ml);FW为鲜重(g);t为反应时间(h)。计算时,先分别计算3个重复的结果,再算平均值,为所求结果。
2.离体法
(1)实验材料与仪器设备
①实验材料:欲测植物材料(如叶类药用植物,实验材料在实验前一天可用硝态氮肥处理,以增强硝酸还原酶活性)。
②仪器设备:分光光度计、冷冻离心机、天平(感量0.1mg)、冰箱、恒温培养箱、研钵、剪刀、离心管、15ml具塞试管、移液管、10ml容量瓶、洗耳球。
③试剂:1.5μg/ml Na NO2标准液(1g NaNO2用蒸馏水定容至1 000ml,吸取5ml,再用蒸馏水定容至1 000ml)、0.1mol/L pH 7.5磷酸缓冲液(30.0905g的Na2HPO4·12H2O与2.496 5g的NaH2PO4·2H2O,用蒸馏水定容至1 000ml)、0.025mol/L pH 8.7磷酸缓冲液(8.864 0g的Na2HPO4·12H2O与0.0570g的K2HPO4·3H2O,用蒸馏水定容至1 000ml)、提取液(0.121 1g半胱氨酸、0.0372g EDTA溶于100ml 0.025mol/L pH 8.7磷酸缓冲液)、2mg/ml NADH溶液(2mg溶于1ml水中,临用前配制)、0.1mol/L KNO3(10.11g KNO3用蒸馏水定容于1 000ml)、磺胺试剂(1g磺胺,加25ml浓盐酸,用蒸馏水定容于100ml)、α-萘胺试剂(0.2gα-萘胺,用含1ml浓盐酸的蒸馏水定容于100ml)、30%的三氯乙酸(30g三氯乙酸,水溶后定容至100ml)。
(2)实验内容与方法
①标准曲线制作,同活体法。
②酶的提取,取新鲜植物组织洗净,拭干,剪碎混均,称取1g,放入研钵中冰冻30min,然后加入少许提取液及少量石英砂,研磨匀浆,转移并用提取液定容至10ml,摇均,静置5min,取上清液4ml加入到5ml离心管中,在4℃、4 000r/min下离心15min,得上清液为粗酶液。
③酶活性测定:取4个15ml试管,其中1个为空白管,另外3个为重复1、2、3在空白管中先加入1ml30%的三氯乙酸,然后在每个试管中加入上述酶液0.2ml、0.1mol/L KNO3 0.5ml、2mg/ml NADH溶液0.3ml,在25℃下水浴保温30min。
④保温结束后之后在重复的3个试管中也加入1ml 30%的三氯乙酸,摇均,以终止反应;在4个试管中各加入磺胺试剂2ml、α-萘胺试剂2ml,摇匀,静置15min;520nm比色,记下吸光值(A)。
⑤计算方法同活体法。
【注意事项】
1.亚硝酸的磺胺比色法比较灵敏,显色速度受温度和酸度等因素的影响。因此,标准液与样品的测定应在相同条件下进行,并在时间上保持同步,方可比较。
2.取样宜在晴天进行,以保证积累足够的糖类。同时,可在取样前一天施用一定量硝态氮肥,提高硝酸还原酶活性。
【思考题】
1.比较活体法与离体法的特点。
2.为什么测定前一天材料要施一定量硝态氮肥?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。

















