1.妊娠期母体的药动学特点 妊娠期胃酸分泌减少,胃排空时间延长,肠蠕动减弱减慢,口服药物吸收峰值常偏低;血容量明显扩张,血浆流量增加35%,血液稀释,血药浓度降低;肾血流量增加,肾小球滤过率增加约50%,肾的排出过程可能加快,也会导致血药浓度降低,药物半衰期可能会缩短,故妊娠期的用药量和给药间隔比非妊娠期大而短。妊娠期血浆白蛋白减少,药物蛋白结合率降低,血中游离药物增多,可致药物分布容积增大,肝负担加重,对药物的清除减慢,妊娠晚期仰卧位时肾血流量减少,可使肾排出药物延缓,尤其伴高血压者,肾功能受影响,药物排泄减慢减少。这些特点可能导致药物在体内蓄积。
(1)药物吸收:早孕反应可使口服药物的吸收受到影响,而临产孕妇的胃排空时间显著延长,胃内残存量多而影响吸收。
妊娠期间由于雌、孕激素分泌增多,致使胃酸和胃蛋白酶分泌减少,胃排空延迟,胃肠道平滑肌张力减退,小肠蠕动减慢、减弱,胃肠道对药物的转运时间延长30%~50%,使弱酸性药物,如水杨酸经口服的吸收延缓、减少,血药浓度达峰时间后推,峰浓度下降,同时药物通过小肠的时间延长,肠道黏液形成增加,肠腔内p H升高,这将有利于弱碱性药物,如镇痛药、催眠药等的吸收较非妊娠妇女增多。但如氯丙嗪能在肠壁被代谢,故在小肠停留时间越长,进入体循环的药物越少,其作用越低。
由于孕妇心排血量约增加37%,加上妊娠时生理性肺通气过度,肺潮气量和肺泡交换量的增加,可使吸入性药物,如麻醉药的吸收加快。同时排血出量的增加使孕妇的皮肤黏膜的局部毛细血管开放,血流增加,因此,滴鼻给药易吸收;阴道栓剂、霜剂、软膏、灌洗液等制剂中的药物亦可随阴道等黏液的吸收加快而增多。皮肤尤其是手足部位的血流显著增加,有利于一些皮肤用药,如控释贴片、酊剂、搽剂、油膏及洗剂等的透皮吸收。硬膜外腔在妊娠期有更多血管形成,故妊娠期妇女硬膜外腔可加速吸收,如注入哌替啶后,不但吸收较非妊娠妇女快,且其血药浓度可相当于静脉注射给药。
妊娠晚期由于血流动力学发生改变,尤其是下肢循环不良,会影响皮下或肌内注射药物的吸收,如孕妇站立时,股静脉压力随着妊娠期的增加而升高,下肢血流通过速度减慢,若于股静脉回流区肌内注射药物,则吸收将有所下降。
(2)药物分布:影响药物体内分布的因素较多,诸如血流量、体液p H、药物与血浆蛋白和组织的结合等。但对孕妇来说,主要是由于血浆容量的扩大与血浆蛋白浓度的减低两大因素影响药物的体内分布。
妊娠期妇女血容量增加40%~50%,血浆增加多于红细胞的增加,因此,血液稀释,心排血量增加,同时,随着子宫、乳腺及胎儿体积的增大而体液总量也增多,平均可增加8L之多,尤其是细胞外液显著增加。由于体液容量的扩大导致许多水溶性药物浓度被稀释,因此,在靶器官往往达不到有效浓度,尤其是对于分布容积较小的药物更为显著,换言之,妊娠期妇女的药物应用剂量应大于非妊娠期妇女。
大多数药物在血液中有一部分与血浆蛋白(主要是白蛋白)形成结合型,孕妇血容量的扩张稀释了血浆蛋白,如在妊娠前半期血浆白蛋白浓度每升可下降5~10g,形成生理性血浆白蛋白低下,加之妊娠期很多蛋白结合部位被血浆中内源性的载体激素和肽类激素等物质占据,使妊娠期药物与血浆白蛋白结合量减少,游离型药物增多,而易转运至各房室,如地西泮、苯妥英钠、苯巴比妥、利多卡因、哌替啶、地塞米松、普萘洛尔、水杨酸、磺胺异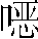 唑等,由于游离型药物增多,药物作用亦可增强,且可增加药物经胎盘向胎儿转运的比率,尤其是高蛋白结合率的药物更为显著。另值得注意的是妊娠晚期妇女脂肪储备可达10kg,使脂溶性药物分布容积显著增大。
唑等,由于游离型药物增多,药物作用亦可增强,且可增加药物经胎盘向胎儿转运的比率,尤其是高蛋白结合率的药物更为显著。另值得注意的是妊娠晚期妇女脂肪储备可达10kg,使脂溶性药物分布容积显著增大。
(3)药物代谢:药物代谢的主要器官为肝,妊娠期肝血流量的变化可能不大,但由于受孕激素的分泌量增加的影响,不但可造成胆汁淤积,使药物的排除减慢,且可诱导或抑制肝微粒体药酶的活性,如妊娠期苯妥英钠等药物羟化代谢的增强,可能与妊娠期胎盘分泌的孕酮相关,而茶碱的代谢则受到明显的抑制,这是肝微粒体药酶活性受到抑制的关系,使肝生物转化功能下降,易产生药物蓄积中毒,故当应用具肝毒性的药物时应持十分慎重态度。
(4)药物排泄:肾脏是药物排泄的主要器官,由于妊娠期妇女心排血量增加而肾血流量亦相应增加约35%,由此肾滤过率增加约50%,肌酐清除率也相应增加,多种药物的清除率随之增加,尤其是主要从肾排泄的药物,如注射用硫酸镁、庆大霉素、氨苄西林、地高辛、碳酸锂的清除明显增加。但在妊娠晚期,由于孕妇长时间腹主动静脉的压迫等,导致肾血流量减少,使药物的清除率也随之降低。若孕妇有妊娠高血压综合征伴有肾功不全时,则药物排泄减慢或减少,从而使药物在体内蓄积,血药浓度增高,半衰期亦相应延长。
有些药物在肝中与葡萄糖醛酸结合后随胆汁排入肠道,而在肠内被水解,游离药物被重吸收而形成肝肠循环,但由于妊娠期葡萄糖醛酸转移酶活性降低,结合型的药物量减少,则在肝肠循环中被重吸收的药量增多,致使药物在血液和组织内的半衰期延长。
2.妊娠期胎儿的药动学特点
(1)胎盘的功能:母体-胎盘-胎儿是一个整体,胎盘的功能主要是药物转运和代谢。
①药物转运:胎盘具有一般生物膜特性,对于药物的透过具有一定的阻抗性,称之为胎盘屏障。母体-胎儿间的物质和药物通过胎盘屏障进行转运。几乎所有的药物都能通过胎盘转运到胎儿体内,但程度与速度有所不同。药物的分子量<500、脂溶性高、解离度低、血浆蛋白结合率低的药物较易通过,分子量>1000时通过的可能性很小,而多数药物的分子量在200~500,易于通过。母体与胎儿血中药物浓度的梯度越大扩散越快,到妊娠中、晚期由于胎盘面积逐渐增大、变薄,亦有利于药物分子的扩散。凡能通过胎盘屏障进入胚胎循环的药物均可对胚胎产生一定影响,其影响大小与用药量、方法,胚胎发育时期以及胎儿基因有关。
②药物代谢:胎盘含有各种参与代谢作用的酶系统,这些酶可分别催化药物的氧化、还原、水解的Ⅰ相和结合的Ⅱ相代谢反应,如对苯并芘等的羟化,对偶氮键和硝基基团等的还原,对哌替啶、乙酰水杨酸等水解及对对氨基苯甲酸等的结合。而且对内源性药物样作用的肾上腺素、去甲肾上腺素、乙酰胆碱等亦可代谢。其代谢能力虽较肝为弱,但至少可起到补偿胎儿肝功能低下的作用。
(2)胎儿的药动学特点:由于胎盘屏障不能完全保护胎儿免受药物的影响,大多数药物可经胎盘进入胎儿体内,且有相当多的药物经代谢可形成有害物质,而致胚胎死亡或畸形。且胎儿各器官功能处于发育和不完善阶段,故药动学特点与成年人有很大差异。
①胎儿的药物吸收:药物经胎盘转运至胎儿体内并经羊膜进入羊水中,但羊水内的蛋白含量仅为母体的1/20~1/10,药物多呈游离型。药物被胎儿皮肤吸收或妊娠12周后的胎儿吞咽入胃肠道,并被吸收入血液循环,其代谢产物由尿排泄,排泄的药物又可被胎儿吞咽羊水致重吸收而形成“羊水肝肠循环”。
②胎儿的药物分布:妊娠12周前胎儿体液含量较高,水溶性药物在细胞外液分布较多,且胎体脂肪含量较少,故脂溶性药物的脂肪分布与蓄积也少,随着胎龄的增长至妊娠晚期,胎儿细胞外液明显减少,脂肪含量增多,使得脂溶性药物分布相应增加。由于胎儿的肝、脑等器官与身体的比例相对较大,血流量多,药物进入脐静脉后,有60%~80%的血流进入肝脏,故肝内药物分布较高,也因胎儿血-脑屏障功能较差,药物容易进入中枢神经系统。胎儿的血浆蛋白含量较母体低,进入组织的游离药物增多。胎儿的血液循环由脐静脉血主要是经肝、肝血窦再经肝门静脉与下腔静脉进入右心房,但亦有进入肝的部分脐静脉血不流入肝血窦,而是经静脉导管直接进入下腔静脉到达右心房,从而减少了肝对药物的代谢,增高了药物直接到达心脏和中枢神经系统的药量,这一特点尤其是母体快速静脉注射给药时应给予足够重视。
③胎儿的药物代谢:药物代谢主要在肝脏进行,胎盘也可限于甾体类、多环碳氢化合物等几类药物的代谢。但是,胎儿肝药酶缺乏,代谢能力低下,因此,往往出现一些药物胎儿血药浓度高于母体,如妊娠期应用乙醚、巴比妥、镁盐、维生素B、维生素C等,胎儿的血药浓度是母体的1倍甚至数倍。多数药物经代谢其活性下降,但有些药物,如苯妥英钠,经Ⅰ相代谢成对羟苯妥英钠,则可竞争核酸合成酶而干扰叶酸代谢,呈现致畸作用,尤其是合并应用苯巴比妥等肝药酶被诱导后,其代谢产物增多,致畸作用增强。
④胎儿药物的排泄:妊娠11~14周开始,胎儿肾脏虽已有排泄功能,但因肾小球滤过率低,药物及其降解产物排泄延缓,即使药物被排泄至羊膜腔后,可被胎儿吞咽形成“羊水肠道循环”,而且胆道的排泄功能也较弱,因此,经代谢形成极性和水溶性的代谢物,较难通过胎盘屏障向母体转运,沙利度胺(反应停)的致畸作用,就是其水溶性代谢物在胎儿体内蓄积所致。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














