(一)AP产生机制与构成
通常神经细胞静息时处于极化状态(polarization),即膜两侧电位保持着内负外正的静息状态。当受到某种刺激使神经细胞膜去极化达到或超过阈电位时,即可在极短的时间内突然变化为膜内为正、膜外为负,然后又回到静息电位,从而出现一个陡峭的峰电位变化,即动作电位(AP)。
AP的构成如下:①膜内电位在短时间内由原来的-70~-90mV变到+20~+40mV,由内负外正变为内正外负,构成了动作电位变化曲线的上升支;②膜内电位由零值变正的数值,称为超射值;③刺激所引起的内外电位倒转是暂时的(神经在0.5~2.0ms内完成),很快膜内电位下降,构成了动作电位曲线的下降支;④短促而尖锐的脉冲样变化称为峰电位;⑤峰电位下降一般要经历微小而较缓慢的波动,称为后电位,一般先持续5~30ms的负后电位,再出现一段延续较长的正后电位(图9-14)。
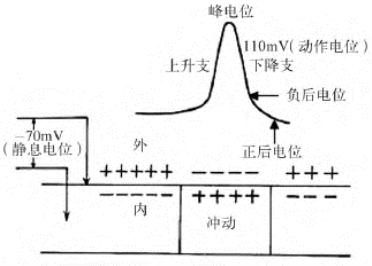
图9-14 动作电位产生的原理(膜电位学说)
Ensin Neher等创造的膜片钳单通道记录技术,为从分子水平了解生物膜离子通道的开放与关闭、动力学、选择性和通透性等膜信息提供了直接的手段。离子通道与神经、肌肉和突触电位呈密切相关。通道的开关过程与产生电信号的神经系统反应相一致,这些微弱电流由神经系统和组织综合加工放大后,形成神经冲动,使生物体作出相应的反应。例如对于钠依赖性动作电位来说,单靠一个钠通道的开放还不足以产生动作电位上升相,它必须、至少有上千个单钠通道开放后才能产生动作电位的上升相。
1.去极相的产生 细胞膜内、外Na+浓度差很大,膜外Na+浓度显著高于膜内。当神经细胞的胞膜受到刺激时,膜上少量Na+通道开放,少量的Na+将顺浓度差内流至胞内。Na+是带正电的离子,它的内流将使得胞内电位轻度去极化。当膜电位减少到阈电位时,大量的电压门控型Na+通道被激活而开放,Na+内流速度急剧增大,在Na+的化学驱动力和静息时膜内原已维持着的负电场对Na+吸引的作用,致使Na+大量通过易化扩散跨膜进入细胞内,以至于超过了K+外流。随着Na+内流增加,膜进一步去极化,而去极化本身又促使更多的Na+通道开放,膜对Na+通透性又进一步增加,形成正反馈,膜内电位迅速由负变正,形成了动作电位的上升支。由于膜外Na+浓度势能较高,Na+在膜内负电位减小到零时,Na+化学梯度可继续驱使Na+内流,直至Na+的平衡电位,形成动作电位中的超射。
2.复极相的产生 细胞膜在去极化过程中,Na+通道开放时间很短,仅万分之几秒,随后Na+通道关闭而失活。使Na+通道开放的膜去极化也使电压门控K+通道开放,膜对K+的通透性增大,膜内K+顺电化学驱动力向膜外扩散,使膜内电位又从正值向负值转变,直至原来的静息电位水平,形成了动作电位的下降支即复极相。快速的上升支和下降支组成了动作电位中的峰电位。
3.后电位的产生 峰电位发生后,产生了微小而持续时间较长的后电位。包括负后电位和正后电位。
(1)负后电位紧接于峰电位下降支后,膜电位比静息电位小,持续5~30ms,幅度为峰电位的5%~6%。一般认为负后电位的产生是在复极时迅速外流的K+蓄积在膜外附近,暂时阻碍K+外流的结果。
(2)正后电位是在负后电位后出现超极化的电位,持续50ms至数秒,幅度为峰电位的0.2%。正后电位的前半部分的形成主要是由于K+通道仍然处于一定的开放状态,对K+的过度通透可持续数毫秒,使较多的K+扩散到膜外,引起膜内正离子的“过多”缺失,后半部分主要由于Na+泵作用,使Na+过度外流的结果。神经纤维每兴奋一次,进入细胞内的Na+浓度增加8万~10万分之一,这种微小的变化,足以激活膜上的Na+泵,使之加速转运,逆浓度差将细胞内多余的Na+排到细胞外,细胞外多余的K+摄入。
4.后电位完结 电位恢复到静息状态,膜内外Na+、K+分布也恢复到静息状态,即指兴奋性恢复正常,可再次接受刺激产生兴奋。
以上过程可以看出,两种离子通过膜结构中电压门控性钾离子通道和钠离子通道进行的异化扩散,是形成神经细胞静息电位和动作电位的直接原因。膜两侧离子浓度梯度及可调控的离子通道是动作电位产生的基础,而动作电位是各种可兴奋细胞(组织)产生兴奋的共同结果。
(二)影响动作电位的因素
正因为生物电的产生是以膜两侧离子浓度梯度及膜离子通道开放和关闭改变离子的通透性为基础,因此改变膜内、外离子浓度或用人工方法调控通道的开关,都将影响生物电的质和量。
在不同神经纤维上动作电位的传导速度不尽相同,因为在有髓纤维动作电位只能在郎飞结处产生,呈跳跃式传导,显然有髓鞘纤维比无髓鞘纤维快。有髓鞘纤维典型的传导速度为10m/s,动作电位的持续时间大约为2ms,因此跨膜距离为2cm。在耳蜗传入神经的动作电位可以通过观察此指标的变化了解神经冲动的同步化程度,从而进一步推测传入神经及突触是否正常。正常情况下影响动作电位传导速度的因素:①髓鞘或膜电阻,有髓鞘存在使传导速度加快;如果脱髓鞘,则传导速度减慢。②与神经纤维的束径有关。因为神经冲动传导速度与膜电阻和膜内电阻有关,膜电阻与纤维的半径成正比,而膜内电阻与半径的平方成反比,所以神经纤维直径越大,传导速度越快。③与膜去极化快慢有关。去极化愈快,达到阈电位所需时间愈短,引起兴奋愈快,传导速度也就愈快。
(三)CAP的来源
当耳蜗毛细胞受机械刺激兴奋后,产生CM的同时,传入神经递质谷氨酸释放入突触,经传入突触与突触后膜的谷氨酸受体结合,激活与谷氨酸受体相耦联的Ca2+通道,引起Ca2+内流,使突触后膜即传入树突去极化产生AP,CAP实际上是数以千计的单个听神经纤维AP之总和。在低频声(0.5,1kHz)刺激时,记录到的CM各波实际上可能是每个正弦波引起一个AP,CM没有潜伏期。从高频到低频CAP的潜伏期从1.76~3.84ms,约相差2ms(图9-15)。
听神经复合动作电位(CAP)在人体ECochG记录中常呈潜伏期为1.5ms左右的一组电位,且始终表现为负性,不随刺激的相位交替而改变,包括N1、N2、N3。在高强度刺激时N2、N3比较明显,N2潜伏期比N1延迟1ms,N3再延长1ms左右。图9-16示N1、N2、N3随刺激强度变化情况。因为CAP实际上是数以千计的单个听神经元放电之总和。因此,有的作者对短声引出的来自基底膜全长的神经活动电位称为“全神经动作电位”(whole-nerve AP,WNAP),而用具有频率特性的刺激引出的称为复合动作电位(compound AP)。通常认为N1来源于有髓鞘的听神经纤维,N2、N3来源于传导速度慢的无髓鞘纤维的放电或重复放电。另外还有实验证明,N2部分来源于耳蜗核,N3部分来源于橄榄核。
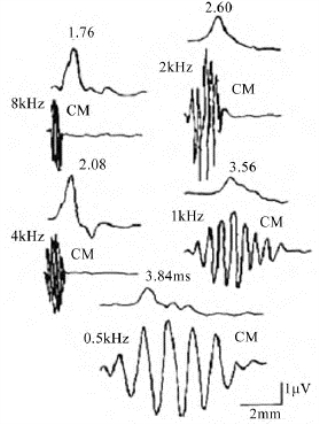
图9-15 用短音8kHz、4kHz、2kHz、1kHz、0.5kHz刺激引导CAP
其CAP的潜伏期从8kHz的1.76ms逐渐延迟到0.5kHz的3.84ms,整个行波延迟2.08ms(刺激强度均为115dB SPL),且可清楚看见CM和SP-AP复合波的关系(从豚鼠圆窗龛记录)
基底膜运动使毛细胞产生耳蜗微音电位,经突触传递使耳蜗神经纤维的传入树突去极化,但一般认为疏相声刺激使基底膜产生向上的运动,是对毛细胞及随后的传入纤维的最有效刺激。听神经纤维对声刺激以两种基本形式发放冲动作出反应。第1种是持续性动作,其发放率在声刺激一开始就达到最大限度;第2种是只对声音有频率锁相(phase-locking)特性的神经纤维发放冲动。每一传入神经纤维单位都有一“特征频率”(characteristic frequency,CF)和对这特征频率最敏感的感受器区。对低强度刺激只有特征频率的感受区有反应。当刺激强度增高时,反应区扩大。这种反应区的扩大主要是向低于CF的一侧延伸,而向高于CF的一侧的延伸则很有限。
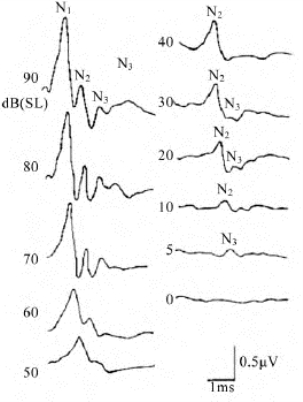
图9-16 人ECochG记录的CAP
示N1、N2、N3随刺激强度减弱而变化过程
在对短促的声刺激作出反应时,耳蜗神经纤维的发放有一潜伏期。这一潜伏期是由行波运行的时间和突触延迟所决定的。在接近蜗尖的神经纤维对短促刺激的反应是一种减幅的迟发放电。观察行波过程,行波从耳蜗底圈至耳蜗顶圈约需2ms的时间延迟图9-15。
CAP的潜伏期随刺激强度增加而缩短,二者呈负相关关系。在反应阈处潜伏期约4 ms~90dB SL时缩短到约1.5ms。CAP的振幅则随声刺激强度增加而增加。但在声强增加到40~50dB SL时振幅达到一稳定平台,而继续增加至60dB SL时,振幅又突然急剧加大(图9-17)。振幅—强度函数曲线可分为“H”(高)、“平台”和“L”(低)段。在高强度时CAP以N1为主;在60dB HL时,CAP呈W形,N1和N2的振幅几乎相等;在低强度(40dB HL)时则以N2为主,在阈值强度(20dB HL)时以N3为主。
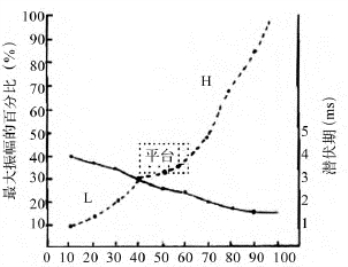
图9-17 20例正常人耳CAP振幅/强度(I/O)及潜伏期/强度(I/O)函数关系
(4kHz短纯音引导)
CAP的波形和输入-输出函数曲线的特性。第1种可以用两群不同的感觉单元的反应来解释。既然认为内毛细胞主要由放射纤维支配,位于基底膜的边缘,距离基底膜的最大振动处远,弱刺激不足以兴奋内毛细胞,强刺激才能激活内毛细胞。因此认为高强度时主要是由内毛细胞及与之相连的神经纤维发出的N1,也就是说“H”段反映了这一群神经单元的活动。N2则为外毛细胞及与之相连的神经纤维产生的冲动,是“L”段的基础。换句话说,OHC对阈值强度灵敏,而IHC对高强度刺激反应。由于神经冲动沿螺旋纤维的非髓鞘树突传递比沿放射纤维传递的时间长,所以N2的潜伏期比N1的长。链霉素、卡那霉素中毒使外毛细胞损害时,“L”段消失而“H”段不受影响。梅尼埃病的CAP输入/输出函数曲线已只剩“H”段(图9-18)。
用两群感觉神经单元解释上述现象并不完善。第2种解释是:从单根神经纤维的频率调谐曲线(frequency tuning curve,FTC)可知各神经纤维对它本身的CF最敏感,刺激强度增加到60dB SL左右时,FTC朝低频侧伸展至最宽程度。FTC的尖峰处即是各纤维的CF的反映。在ECochG中,低强度刺激时,CAP是从相应的FTC的尖峰处的神经单位发生的,这相当于“L”段;刺激强度超过60dB SL,CAP则为由FTC的宽部许多神经单位所发生的,这相当于“H”段。这种解释又无法说明波形的问题。

图9-18 双耳梅尼埃病的CAP输入-输出函数曲线
短音引导,外耳道记录,o…o右耳,×…×左耳
第3种解释认为WNAP的波形是由于各神经单位与行波到达的时间关系不同,阈值不同,可能极性也不同,这些综合起来使耳蜗各段产生的CAP综合组成WNAP的波形。
近年来,Dallos P和Russell PT成功地进行了载体的毛细胞的胞内记录,使之真正认识了耳蜗毛细胞的生理特性。实验证明,内毛细胞比外毛细胞敏感,但它必须依赖于外毛细胞的完整,表现出主动机制的非线性特点,提示在正常情况下,OHC对IHC有驱动作用。当OHC损伤时IHC灵敏度下降,CAP阈值升高,且耳蜗功能表现出被动的线性特征。耳声发射现象的发现以及对外毛细胞能动性和胞内肌动蛋白组织学基础的研究,进一步证明了外毛细胞的主动机制及其与内毛细胞之间的关系,从而补充和修正了上述两群不同感觉单元的假说(详见第15章)。
(四)CAP的特点
1.符合“全或无”定律 即阈下刺激时不引起反应,而对阈上刺激无论强度大小,总产生一定的动作电位,有不应期。
2.CAP的幅度与刺激强度构成特定的非线性关系 根据CAP为同步化反应或瞬态反应之特点,当短声的刺激声强较大时,其强度可在短时间内达到最大值,可使不同阈值、不同潜伏期的纤维在短时间内达到兴奋状态而发放冲动。此时CAP的潜伏期短,幅度大,反之亦然。CAP潜伏期-强度曲线基本上呈负相关的线性关系,而CAP幅度-强度曲线分为“L”、“平台”和“H”3个阶段。其产生的原因如本节的第二段所述,可能是OHC与IHC各自特点及相互关系造成的。
3.CAP具有真正的阈值 可以比较真实地反映耳蜗功能,为耳蜗功能重要的指标,也是临床和科研实验中常用的指标。
4.CAP为听神经的同步化反应 CAP是数根传入神经纤维动作电位的空间总和,因此各根纤维活动的同步化程度是记录CAP的前提,为了获得数根纤维的同步化效应,大量的试验经验得出结论,只有瞬态特性好(即上升/下降时间短)的短声可引出同步化程度高的CAP,所以CAP也叫做瞬态反应。然而短声是宽频带噪声,其能量主要集中在3~4kHz,所以短声诱发的CAP不能反映耳蜗各圈的功能。因此,既要选择瞬态特性好的刺激声使CAP同步化好,又要保证其频率特异性,这几乎是不可实现的。学者们采用了“折中”的办法,即选择频率特异性较好,瞬态特性又较好的滤过短声或短音来诱发CAP。图9-15为用不同频率的短音诱发CAP的例子,但值得注意的是在低频时(0.5,1kHz)CAP波形分化得并不好,会给判断反应阈值带来困难,需要反复测试和谨慎从事。
5.CAP有被掩蔽的特性 无论在临床听力检测或者动物实验中,当我们诱发CAP时,周围有噪声持续一段时间时可见CAP的幅度下降甚至消失,此特点可能是作纯音测听时加掩蔽噪声消除好耳“影子”曲线的生理学基础。在实验或临床检测中,如果需要突出CM也可用宽带噪声来掩蔽CAP的出现。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















