成年人星形细胞瘤(astrocytic tumors)大多发生于大脑,而儿童则多发于小脑。按肿瘤组织学分为6种类型,而根据细胞分化程度的不同可分为以下4个级别。
(1)Ⅰ级星形细胞瘤(毛细胞型星形细胞瘤、室管膜下巨细胞星形细胞瘤)。
(2)Ⅱ级星形细胞瘤(弥漫生长型)。
(3)Ⅲ级星形细胞瘤(间变型星形细胞瘤)
(4)Ⅳ级星形细胞瘤(胶质母细胞瘤)。
其中Ⅰ、Ⅱ级肿瘤边缘较清楚,多表现为瘤内囊腔或囊腔内瘤结节,肿瘤血管较成熟;Ⅲ、Ⅳ级肿瘤呈弥漫浸润生长,肿瘤轮廓不规则,分界不清,易发生坏死、出血和囊变,肿瘤血管丰富且分化不良。
1.Ⅰ级星形细胞瘤(毛细胞型星形细胞瘤、室管膜下巨细胞星形细胞瘤)
【临床表现】
星形细胞瘤好发年龄10-20岁,占全部脑肿瘤的3%~6%,尤其好发于儿童,占儿童胶质瘤第2位,生长缓慢,症状隐匿。好发部位为视交叉、下丘脑、小脑、脑干及第四脑室等;少数病变发生于颞叶、基底节及中脑四叠体,瘤体一般与周围组织无明显的分界,但发生于小脑的毛细胞型星形细胞瘤可见明确的纤维包膜。
临床主要表现为颅内高压、共济失调、视力损害及癫 等,多数患者可行外科全切根治术,预后良好。
等,多数患者可行外科全切根治术,预后良好。
【影像学诊断与鉴别诊断】
(1)影像学表现
1)CT
①肿瘤一般呈低密度,瘤体可伴有钙化,瘤周无水肿。
②发生于小脑者,一般为囊性肿瘤多见,瘤体呈大囊状,可见壁结节,部分呈囊实性,少数呈实体性,增强扫描实性部分、壁结节,囊壁强化明显,常合并幕上明显的梗阻性脑积水。
③发生于下丘脑及视交叉等部位时,肿瘤多为实性,但增强扫描时,肿瘤明显强化,但瘤体内部可见不强化的微囊变区。
2)MRI:形态学改变与CT基本相同,增强扫描与CT亦基本相同,瘤体于T1 WI序列呈低信号,于T 2 WI序列呈高信号,囊变呈T 1 WI低信号,T 2 WI高信号(图2-1)。
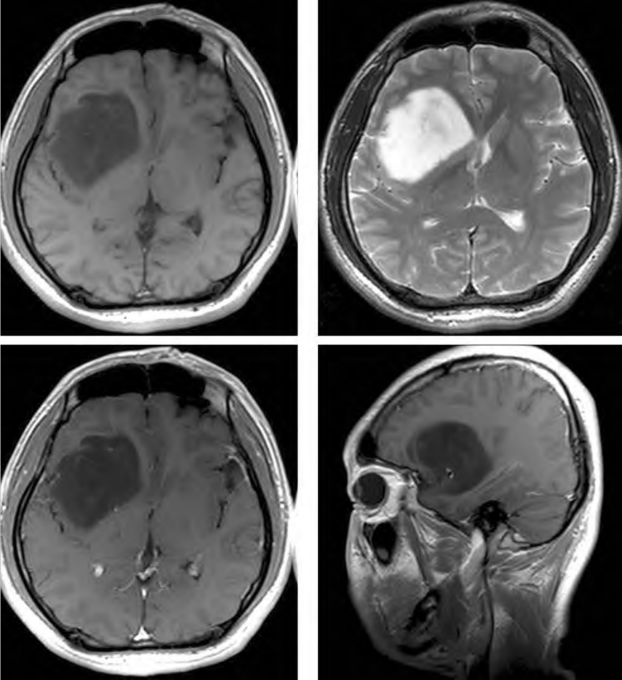
图2-1 右侧额叶Ⅰ级星形细胞瘤
MRI平扫呈长T 1长T2信号,瘤周无水肿,增强扫描无明显强化
(2)鉴别诊断:主要与发生于小脑的血管母细胞瘤(angioblastom)相鉴别,前者多见于青少年,后者多见于中年人,囊性毛细胞型星形细胞瘤的壁结节大而不规则,而良性血管母细胞瘤多表现为大囊小结节。另外MRI的平扫即可见后者丰富的流空血管。
【病理学表现】
(1)大体观察:瘤组织大部分色灰,质软,相当疏松。肿瘤内和周边常见囊肿形成。
(2)组织病理学:瘤细胞密度低,组织双相性,由致密区含Rosenthal纤维的梭形细胞和疏松区多极细胞伴微囊和嗜酸性颗粒小体(granular bodies)形成为特点。核分裂象罕见,偶见染色质浓染的核,可见微血管增生和脑膜浸润,但此非恶性指征。致密区的双极毛状细胞表现为长长的毛发样突起,常与Rosenthal纤维相伴随。毛状细胞核长梭形,淡染,细胞富含纤维, GFAP染色阳性。Rosenthal纤维为胡萝卜形、节段形或串珠状、杆状的嗜伊红透明团块,最常出现在致密的毛细胞区,尤其在细胞涂片中看得更清楚。疏松微囊区的细胞与毛状细胞不同,细胞核圆或卵圆形,胞体小,胞突相对短,GFAP染色弱阳性,细胞核淡染,常与嗜伊红颗粒状透明小体伴随存在。常可在肿瘤中见到明显的血管透明变性、扩张,陈旧性出血、钙化和淋巴细胞浸润等,还可见一些像少突胶质细胞样的细胞和弥漫型星形细胞瘤WHOⅡ级的细胞存在。
尽管毛细胞型星形细胞瘤是良性的,但有些肿瘤显示染色质浓染和细胞多形性(图2-2),罕见病例的核分裂可高达30%。偶尔,小脑的弥漫生长型肿瘤可掩盖致密和微囊生长型的组织学特点,若发现染色质浓染的核,则易与高级别弥漫型星形细胞瘤相混淆。易造成误诊的病变还包括变性所致的不典型和多形性核、灰污的染色质和核内胞质包涵体,这些病变常见于病史较长的患者,尤其在小脑或大脑半球最易发生。透明变性和肾小球样血管是毛细胞型星形细胞瘤的组织学特点,也可见到血管周围淋巴细胞浸润。
(3)鉴别诊断
①少突胶质细胞瘤:少突胶质细胞瘤瘤细胞核较圆,有核周空晕。在毛细胞型星形细胞瘤可以见到少突胶质细胞瘤样细胞,特别在小脑肿瘤中,瘤细胞片状排列或被间质分隔,很像少突胶质细胞瘤。局部区域找到典型的毛细胞型星形细胞瘤结构就能给出正确诊断。
②多形性黄色星形细胞瘤:两者发病年龄相似,易形成囊腔和瘤结。但前者瘤体多表浅,明显累及脑膜,瘤细胞多形性明显,瘤细胞排列紧密。
③纤维型星形细胞瘤:纤维型星形细胞瘤的胶质纤维丰富,很少呈编织样排列。单级或双极细长的瘤细胞不易见到,很少见到Rosenthal纤维和嗜酸性颗粒小体。
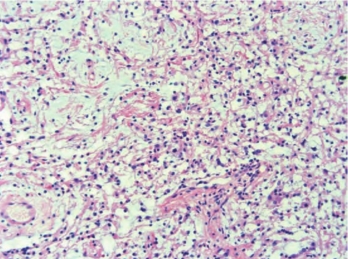
图2-2 毛细胞型星形细胞瘤
瘤细胞密度低,组织双相性,由致密区含Rosenthal纤维的梭形细胞和疏松区的多极细胞构成
④毛细胞型星形细胞反应性增生:Rosenthal纤维并不是毛细胞型星形细胞瘤或肿瘤所特有,也可见于慢性反应性胶质增生中。致密的纤维、少量的细胞、大量的Rosenthal纤维的胶质增生反应很像毛细胞型星形细胞瘤。此情况多见于颅咽管瘤周围或小脑囊性血管母细胞瘤的周围,反应性增生一般不会有囊腔出现。
2.Ⅱ级星形细胞瘤(弥漫生长型)
【临床表现】
弥漫性星形细胞瘤约占全部胶质瘤的1/3,属于Ⅱ级胶质瘤。好发于30-40岁的成年人,病变好发部位为大脑半球白质区,也可发生于基底节、丘脑、脑干及小脑等部位,临床症状以颅内高压以及相应部位压迫症状为主,不具有特征性。
【影像学诊断与鉴别诊断】
(1)影像学表现
1)X线
①颅内生理性钙化移位或出现病理性钙化;
②合并颅内高压时,成年人部分可见鞍背骨质的破坏,儿童可见颅脑脑回间压迹增多及颅缝分离等征象。
2)CT
①平扫肿瘤及肿瘤周边的水肿均呈低密度,一般无钙化;但有15%~20%的病例,肿瘤内可有小的斑点状钙化。
②肿瘤表现有不同程度的占位效应,肿瘤较大或肿瘤周围水肿明显者可有中线结构移位和脑室受压变形、移位、闭塞,小的肿瘤或周围水肿较轻者可仅表现肿瘤区域脑沟、脑裂变窄或闭塞。
③肿瘤内一般无出血。
④增强扫描多数强化不明显,少数呈轻度强化,强化方式为斑片状或团块状(图2-3)。
3)MRI
①在T 1 WI序列上多表现为低信号,也可表现为低等混杂信号,T 2加权图像上一般为高信号,可以瘤体非常均质,也可以见不均质,不均质的肿瘤常见于较大瘤体,不均质的原因是部分瘤体在T 2图像上信号增加不显著,明显低于周围水肿,或因肿瘤内有钙化或囊变。
②T 1 WI序列对于仅有脑沟、脑裂等轻微占位效应显示好于CT图像。
③增强扫描肿瘤多不强化或表现为轻度斑点状强化,极少数可出现明显强化,少数肿瘤可以出现囊变。
④氢质子波谱的典型表现为NAA波显著降低,Cr波中度降低,Cho波显著升高,Cho/Cr比值通常>2,但恶性程度较低的肿瘤波谱改变可以与正常脑组织基本相同,由于髓鞘脱失, Cho波也比正常脑组织低,但Cho/NAA比值高于对侧(图2-4)。
(2)鉴别诊断
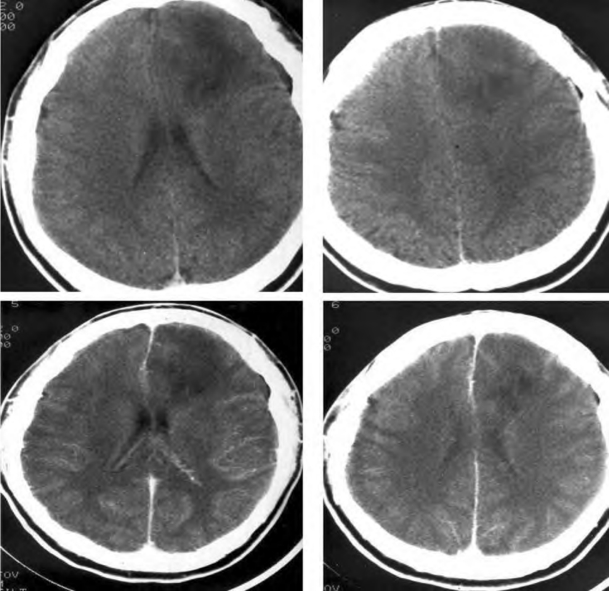
图2-3 左额叶Ⅱ级星形细胞瘤
CT平扫可见左额叶不规则片状低密度影,邻近脑沟裂变浅,无明显钙化,增强扫描未见明显强化
1)脑梗死:①CT扫描均为低密度,MRIT 1图像为低信号,T 2图像为高信号,但脑梗死病变范围与脑血管分布区一致,同时累及灰质和白质;②脑梗死发病突然,老年人常见,数周后占位效应消失,边界清楚,并可局部出现脑萎缩征象;③鉴别有困难者可以行MR氢质子波谱检查,星形细胞瘤NAA波明显降低,Cr波中度降低,Cho波也降低;急性脑梗死NAA波也降低,但急性脑梗死特征性波谱改变为出现明显的Lac波。
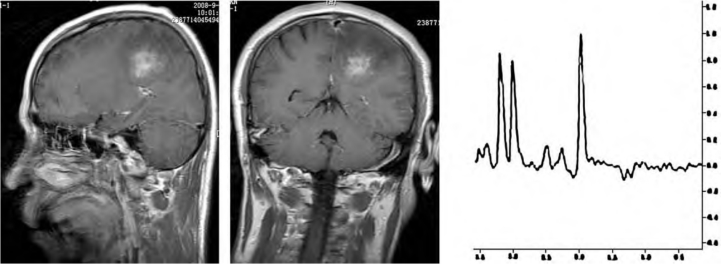
图2-4 左顶叶Ⅱ级星形细胞瘤
MRI扫描可见左顶叶不规则长T1、长T2信号,T 2 WI信号不均匀,周边可见水肿,增强扫描呈斑片样强化, MRS可见NAA峰降低,Cho峰明显升高
2)脑实质内室管膜瘤:弥漫性星形细胞瘤出现大部分囊变或几乎囊变少见。
【病理学表现】
(1)大体观察:瘤体呈灰白色,质地视肿瘤内胶质纤维的多少而异,或硬或软,或呈胶胨状外观,或呈海绵状。灶性钙化也可存在,呈沙砾状。
(2)组织病理学:弥漫生长型星形细胞瘤分为纤维型、原浆型和肥胖细胞型星形胶质细胞瘤三个亚型,由分化好的纤维性、原浆性或肥胖性肿瘤性星形细胞构成,瘤细胞一般较一致,背景疏松,含黏液样微囊。核细胞密度中等,核分裂象少见,一般无出血及坏死。免疫组织化学染色显示GFAP弥漫表达,表达强度可不一致。
1)纤维型星形细胞瘤:瘤细胞与正常脑白质的星形细胞结构相似,比正常白质的星形细胞密度高1~2倍或以上。核轻度增大和不规则,染色质轻度增多,核周少许胞质或胞质不明显,呈裸核状或雪茄烟状或不规则浓染核,胞质胶质纤维丰富,凸起呈细网状。毛细血管稍增多,但无内皮细胞增生。存在黏液微囊是其病变特点(图2-5)。
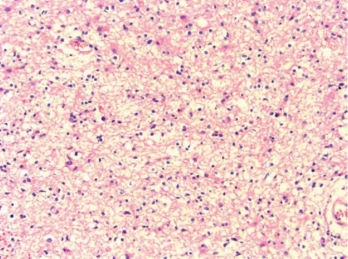
图2-5 纤维型星形胶质细胞瘤
瘤细胞核轻度增大和不规则,染色质轻度增多,核周少许胞质或胞质不明显,胞质胶质纤维丰富,凸起呈细网状
纤维型星形细胞瘤需与以下情况相鉴别。
①反应性胶质细胞增生:正常星形细胞核卵圆形到长梭形,横切面可呈圆形,明显空泡状,染色质中等大小,常有一个清晰的核仁,不见胞质,与网状背景形成对比。反应性星形细胞核增大,胞质明显,与肥胖细胞类似,核偏位,胞质红染,边缘渐淡。结构上很少在同一时间同一区域呈一致性变化,常表现为不同形态的星形细胞混在一起,有的核伸长,有的胞质量增多,残存的细胞如神经元常可陷入其中,核分裂相当少或缺如。弥漫性星形细胞瘤内的细胞数目增多,形态一致,可见微囊形成。
②间变型星形细胞瘤:本型瘤细胞密度不及间变型星形细胞瘤,胶质纤维比后者多,瘤细胞异型性不明显,核分裂象罕见,无坏死灶。
2)原浆型星形细胞瘤:瘤细胞胞体较小,核一致性圆形或卵圆形,其胞质较纤维型星形细胞瘤丰富,并伴有少量纤细短凸起,神经胶质纤维少或缺乏。当瘤细胞发生退变时,可形成海绵状的基质和微囊,此型也常见黏液变性和微囊形成。
原浆型星形细胞瘤需与以下情况鉴别。
①纤维型星形细胞瘤:纤维型星形细胞瘤瘤细胞多呈梭形延伸或三角形,而原浆型星形细胞瘤其胞质较丰富,常见黏液变性和微囊形成。
②毛细胞型星形细胞瘤:两者均易见到微囊形成,而原浆型星形细胞瘤无单级或双极细长的瘤细胞,无Rosenthal纤维和嗜酸性颗粒小体。
③少突胶质细胞瘤:两者瘤细胞核均呈圆形。少突胶质细胞瘤瘤细胞有核周空晕,而本瘤核周为胞质及纤维短突起。前者可见钙化灶,囊腔形成少见。
3)肥胖细胞型星形细胞瘤:以存在大量肥胖型瘤性星形细胞为特点,一般和纤维型星形细胞瘤共存,肥胖细胞比例应>20%。瘤细胞多密集排列,呈多角状或球状,核偏位,核固缩或核仁明显,有丰富的嗜酸性毛玻璃样胞质。肥胖的、无方向性的胞突形成致密的纤维网,常见血管周围小淋巴细胞套。小血管可呈丛状增生伴内皮细胞增生,出现此结构易进展为胶质母细胞瘤(图2-6)。
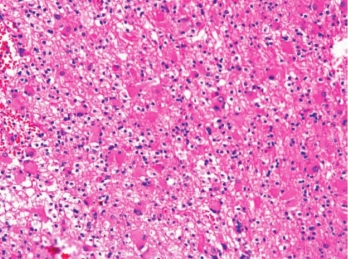
图2-6 肥胖细胞型星形胶质细胞瘤
星形细胞呈多角状或球状,核偏位,部分核固缩,部分可见核仁,有丰富的嗜酸性毛玻璃样胞质和纤维型星形细胞瘤并存
肥胖细胞型星形细胞瘤需与以下情况鉴别。
①原浆型星形细胞瘤:原浆型星形细胞瘤胞质稍丰富,嗜酸性均质。但本瘤瘤细胞多密集排列,呈多角状或球状,核偏位,常见血管周围小淋巴细胞套,但很少有微囊形成。
②胶质母细胞瘤:本瘤易进展为胶质母细胞瘤。但胶质母细胞瘤的肿瘤性星形细胞分化差,常呈多形性,细胞密集,核分裂象多见,并可见怪异的单核细胞或多核瘤巨细胞。明显的微血管增生和(或)坏死是诊断的基本要点。
3.Ⅲ级星形细胞瘤(间变型星形细胞瘤)
【临床表现】
间变型(恶性)星形细胞瘤(anaplastic astrocytoma)是最常见的脑内原发恶性脑肿瘤,约占全部胶质瘤的25%,其恶性程度介于弥漫生长型星形细胞瘤和胶质母细胞瘤之间,多数为低度恶性胶质瘤转变而来。肿瘤好发于大脑半球额叶、颞叶及与顶叶的交界区,也可见于丘脑和脑干,小脑罕见。间变型星形细胞瘤可见于任何年龄,但多发于40-50岁的成年人,临床主要表现包括癫 和局部定位症状。临床预后较差,平均存活时间为2年。肿瘤可以通过细胞外间隙和沿白质束扩散,也可通过室管膜和脑脊液扩散。
和局部定位症状。临床预后较差,平均存活时间为2年。肿瘤可以通过细胞外间隙和沿白质束扩散,也可通过室管膜和脑脊液扩散。
【影像学诊断与鉴别诊断】
(1)CT
①平扫肿瘤呈低密度,囊变部分呈更低密度,瘤周水肿密度低于肿瘤实质部分。
②肿瘤多呈不规则形,或圆形及类圆形,有不同程度的占位效应,主要根据肿瘤的大小及部位而异,轻者表现为局部脑沟、脑裂变平、闭塞,严重者可见一侧脑室受压、变形及中线结构移位。
③增强扫描肿瘤实质部分强化明显,多呈结节状或团块状强化,合并囊变的肿瘤,囊变呈环状强化(图2-7)。
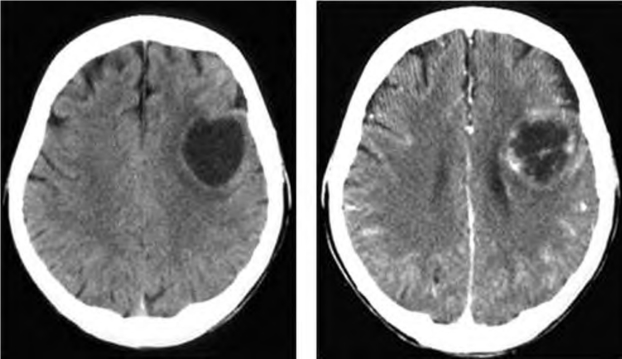
图2-7 左额叶Ⅲ级星形细胞瘤
CT平扫呈类圆形低密度,大部分囊变,周围脑沟裂变浅,增强扫描呈明显周边环状强化
(2)MRI
①由于肿瘤坏死,MRI上信号常不均匀,在T1 WI序列上呈等低混杂信号,有出血时,出血灶呈高信号。在T 2 WI序列,中心常呈高信号,周围见等信号环,再向外为高信号水肿。
②弥散加权成像肿瘤坏死部分呈低信号。
③肿瘤境界常不清楚,增强扫描常呈不规则环状强化,典型者沿白质通道扩散。
④穿刺活检时,肿瘤周围高信号水肿区也可见到肿瘤细胞(图2-8)。
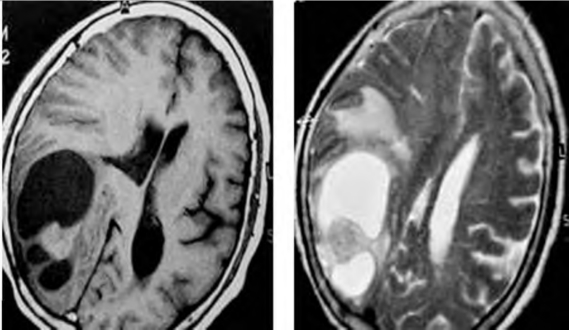
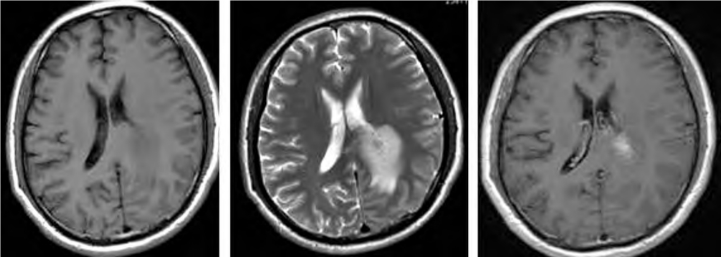
图2-8 右侧顶枕叶Ⅲ级星形细胞瘤
MRI病变呈囊实性,T 2 WI周边可见大片长T2水肿区,右侧脑室后角明显受压,中线结构左移
(3)鉴别诊断:主要与各类星形细胞瘤及脑梗死鉴别,MR氢质子波谱能够对其分化程度提供重要的诊断信息,对良性星形细胞瘤鉴别的敏感性、特异性和准确性分别为100%、86%、96%。常用Cho/NAA比值和Cho/Cr比值判断星形细胞瘤的良、恶性,间变型星形细胞瘤Cho/NAA比值常接近6,而良性星形细胞瘤通常在2~3;间变型星形细胞瘤Cho/Cr比值常接近5,而良性星形细胞瘤通常在2~2.5。间变型星形细胞瘤的不典型表现包括肿瘤呈囊性不强化肿块,或者表现为表面肿块,类似于脑梗死,根据不均质密度和信号,不规则环形强化,典型的间变型星形细胞瘤通常在CT和MRI检查时容易诊断(图2-9)。
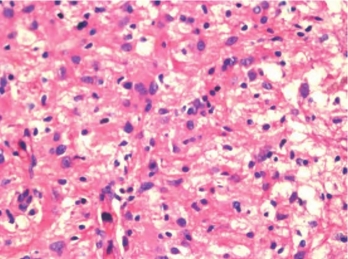
图2-9 间变型星形细胞瘤
瘤细胞密度大,核的大小、形态不一,染色质密集或分散,核仁明显,数目增多
【病理学表现】
(1)大体观察:瘤组织呈颗粒状,质软。
(2)组织病理学:原则上同弥漫型星形细胞瘤,但细胞密度、核异型性和核分裂象增加,区域性或弥漫性高密度细胞区是重要的诊断指标。肾小球样微血管增生或点彩状坏死灶的存在反映发展成胶质母细胞瘤的可能。伴进行性间变病例,核的多型性更为复杂,核的大小、形态不一,染色质密集或分散,核仁明显,数目增多。其他的间变特点是核内包涵体、多核瘤细胞和丰富的核分裂象。肥胖细胞也可存在,但不足以诊断间变型肥胖细胞型星形细胞瘤。毛细血管内衬单层内皮细胞,一般无微血管增生和坏死。
(3)鉴别诊断
①弥漫型星形细胞瘤:间变型星形细胞瘤是在弥漫型星形细胞瘤基础上的去分化和恶变,所以瘤细胞密度、核异型性和核分裂象增加。
②胶质母细胞瘤:胶质母细胞瘤的肿瘤性星形细胞分化差,常呈多形性,且核分裂象多见,并可见怪异的单核或多核瘤巨细胞。明显的微血管增生和(或)坏死是诊断的基本要点。
4.Ⅳ级星形细胞瘤(多形性胶质母细胞瘤)
【临床表现】
胶质母细胞瘤,又称多形性胶质母细胞瘤,按WHO分类属于Ⅳ级胶质瘤,高度恶性,好发于40-60岁的成年人,发病男女比例为2∶1。占星形细胞瘤的55%,年龄大者(55岁以上)可多发,大脑半球多见,好发于额叶、颞叶及各叶交界区及基底节、丘脑。肿瘤浸润范围广,若病变发生于胼胝体则病变向两侧发展,呈蝴蝶状。少见于颅后窝,小儿可发生于脑干。肿瘤与脑干分界不清,瘤血管丰富,血管内皮细胞增生、肿胀,进而导致血管闭塞及血栓形成,瘤体内常因血管闭塞而出血、坏死,液化坏死腔内可见液体。主要临床表现是头痛、癫 、颅内高压表现及局部神经定位征。通常病变进展很快,首发症状到出现颅内高压的时间平均为3~4个月,有时仅表现为癫
、颅内高压表现及局部神经定位征。通常病变进展很快,首发症状到出现颅内高压的时间平均为3~4个月,有时仅表现为癫 。
。
【影像学诊断与鉴别诊断】
(1)CT
①平扫瘤体多呈混杂密度,实质部分通常为等密度或稍高密度,囊变、坏死部分为低密度,少数病例合并出血,急性出血多呈高密度,慢性出血多呈等、低密度。
②占位征象主要取决于肿瘤的大小和部位。瘤周水肿通常呈低密度。
③增强扫描瘤体实质部分呈明显强化,强化方式为团块、结节、环状或花边状(图2-10)。
(2)MRI
①T 1 WI图像肿瘤呈混杂信号,中心坏死囊变区呈低信号,周围见不规则厚壁的肿瘤实质,呈稍低信号,肿瘤实质信号在T 1 WI图高于中心坏死区。有出血时,出血区在T1 WI图像上呈高信号。
②T2 WI上肿瘤信号也不是很均质,中心坏死和周围水肿区呈高信号,肿瘤实质呈稍高信号,其信号低于坏死和水肿区。
③肿瘤占位效应明显。
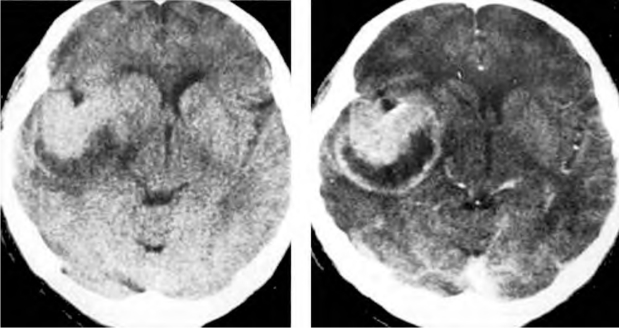
图2-10 右侧颞叶Ⅳ级星形细胞瘤
CT增强扫描病变呈囊实性,实性部分及囊壁明显强化
④增强扫描常表现为显著的环形不规则强化。
⑤多数胶质母细胞瘤在后期沿白质束向周围扩散,可形成卫星病灶,即大的母体肿瘤周围出现一些小的肿瘤灶,在影像学上可与中心病灶相连,也可不与中心病灶相连,但在镜下可与中心病灶相联系。在镜下互相没有联系的多发性胶质母细胞瘤称为多中心性胶质瘤或多发性胶质瘤。
⑥胶质母细胞瘤常沿白质束扩展,通过胼胝体,前联合和后联合扩展到双侧大脑半球,呈蝴蝶样为其典型表现。沿内囊和外囊扩展也常见,肿瘤也可沿蛛网膜下腔脑脊液通道种植(图2-11)。
(3)鉴别诊断:典型的胶质母细胞瘤通常容易诊断,位于胼胝体向双侧半球扩展的胶质母细胞瘤需要与脑原发淋巴瘤鉴别。MR氢质子波谱可以作出诊断,肿瘤实质部分出现明显的脂质波,提示淋巴瘤可能。
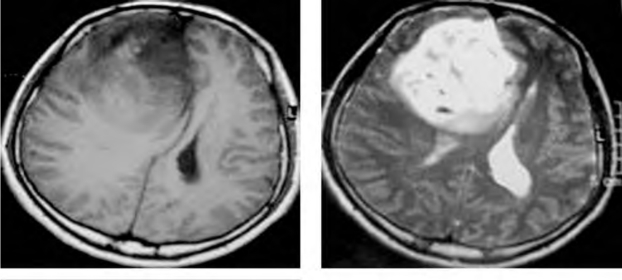
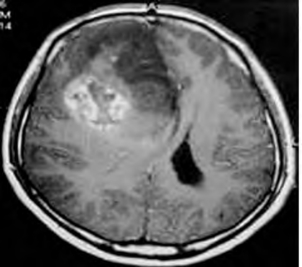
图2-11 右侧额叶Ⅳ级星形细胞瘤
MRI平扫T1 WI呈等低混杂信号、T2 WI呈高信号,增强扫描呈明显不均匀性强化
【病理学表现】
(1)大体观察:切面颜色不一,由于髓鞘崩解坏死呈黄色;新鲜或少量出血呈红色和棕色;中心坏死可占整个肿瘤的80%,周围呈灰色;肿瘤组织坏死液化也可形成含浑浊液体的大囊腔。
(2)组织病理学:肿瘤性星形细胞分化差,常呈多形性,细胞密集,异型性明显,具有活跃的分裂活性。细胞的多形性表现为小细胞、梭形细胞、含脂质的细胞、颗粒细胞等,还可出现鳞状上皮化生、软骨化生、骨化生等,偶尔含腺样和带状上皮结构。多核瘤巨细胞是胶质母细胞瘤的标志,但它既不是必有的特征,也与临床进程无关。当巨细胞成分占优势时,称为巨细胞胶质母细胞瘤。巨细胞形态非常奇异,核可达到20多个,常为角状,核仁明显。肥胖细胞胞质丰富、毛玻璃状,胞核偏位。在胶质母细胞瘤中出现大量肥胖细胞时,提示为继发性胶质母细胞瘤;在Ⅱ~Ⅲ级星形细胞瘤中出现大量肥胖细胞,提示将很快发展为胶质母细胞瘤。血管周围淋巴细胞套在许多胶质母细胞瘤中可以见到,常在肥胖细胞区出现,主要为CD8+T淋巴细胞,CD4+T细胞、B细胞少见。微血管增生是胶质母细胞瘤的重要组织学标志,可呈现“肾小球丛”状微血管增生,常位于坏死区附近。典型的微血管增生包括多层的、核分裂活跃的内皮细胞和平滑肌细胞/血管周细胞增生(图2-12)。常发生血栓形成,引起肿瘤缺血性坏死。缺血性坏死常表现为大片的坏死,在坏死中央区瘤细胞仍可辨认,一般不趋化大量的巨噬细胞,可见扩张血管轮廓;第二种坏死为多灶性小的不规则带状或假栅栏状坏死,周围瘤细胞常发生凋亡,坏死是诊断胶质母细胞瘤的标志。胶质肉瘤为胶质母细胞瘤的另一亚型,肿瘤具有胶质和间叶组织双向分化,即胶质母细胞瘤中出现了肿瘤性间叶组织成分和网状纤维。胶质成分显示典型的胶质母细胞瘤特点,肉瘤区域常显示致密的长梭形细胞排列成鱼刺样纤维肉瘤结构,也可表现为恶性纤维组织细胞瘤样,可见骨和软骨、平滑肌、骨骼肌成分。
(3)鉴别诊断
①间变型星形细胞瘤:间变型星形细胞瘤细胞密度、瘤细胞异型性及核分裂象不及本瘤,虽可见肾小球样微血管增生或点彩状坏死灶,但无大片坏死灶。
②转移癌:转移癌与脑组织分界较清,并有条索状胶原纤维作为间质,癌细胞的多形性不如本瘤,无肾小球样微血管增生。免疫组织化学染色转移癌一般CK、EMA等上皮标记阳性, GFAP阴性。
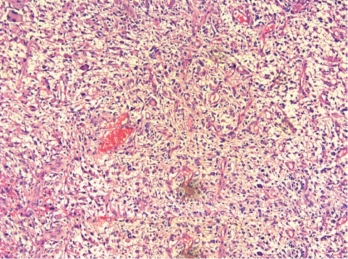
图2-12 多形性胶质母细胞瘤
肿瘤性星形细胞分化差,呈多形性,细胞密集,异型性明显。微血管明显增生
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














