2.9.1 传统过渡态理论
对于过渡态理论建立的基本假设,曾有过长期的探讨研究,目前较一致的看法认为过渡态理论的基本假设如下:
(1)Born-Oppenheimer近似,即基于电子质量一般小于核质量几个数量级的事实,将电子运动和核运动进行了分离处理。由于Born-Oppenheimer近似中只对一种电子态进行了考虑,而对不同电子态之间的跃迁未加考虑,因此也被称为核运动绝热假定,此处的绝热与热力学中的“绝热”无关。
(2)假定反应体系中的反应物状态维持Boltzmann分布。一般将没有化学反应时的热平衡分布称为Boltzmann分布,而当化学反应发生时反应物状态会在一定程度上偏离Boltzmann分布。由于对大多数的热反应来说,这种偏离可以通过非反应性的低能分子之间的碰撞进行补偿,所以可以认为反应物状态对Boltzmann分布的偏离较小,可以忽略。
(3)不返回假定。它认为穿越分隔面的轨线都是反应性轨线,既任一条轨线一旦穿越分隔面就奔向产物区,而不会再返回到反应物区,不返回假定忽略了二次或多次穿越分隔面的轨线。
(4)运动分离假定。该假定将反应体系沿反应坐标方向的运动和其他运动坐标进行了分离,认为其他运动的量子数在反应物区、过渡态区和产物区均不变,是绝热不变量的。
上述四条假定中的(1)、(2)假定是所有热反应速率理论的共有假定,均被接受。(3)、(4)假定则是过渡态理论的特有假定。
对于反应A+B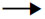 C≠
C≠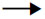 Products来说,反应体系的反应物和活化络合物之间的平衡常数依上述假定可以表述为
Products来说,反应体系的反应物和活化络合物之间的平衡常数依上述假定可以表述为
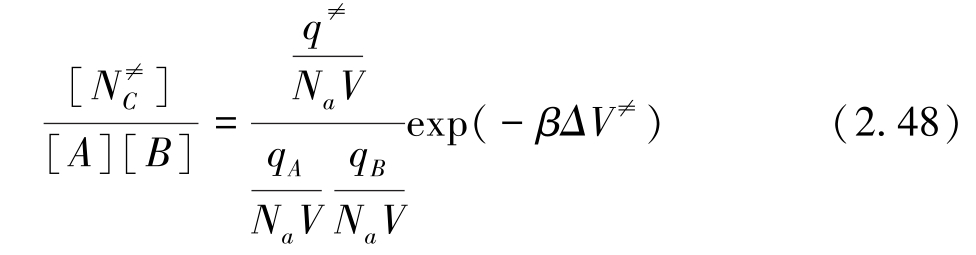
上式中的β代表1/(kBT),kB和T分别代表玻尔兹曼常数以及温度。而ΔV≠是过渡态能量和反应物能量的差值,即经典势垒高度。[A]、[B]和[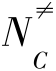 ]分别表示反应物A、反应物B以及活化络合物的浓度,而qA、qB和q≠分别是它们的总配分函数。Na代表Avogadro常数,V代表体积。
]分别表示反应物A、反应物B以及活化络合物的浓度,而qA、qB和q≠分别是它们的总配分函数。Na代表Avogadro常数,V代表体积。
由于不返回假定认为所有由反应物出发形成的活化络合物都一定会变成产物,而不会返回反应物区。因此,产物的生成速率可用下式表示:

其中τ是反应体系通过过渡态状态区所需的时间,而τ又是由
![]()
计算得到的。假设过渡态区间是大小为δ的区域,由于过渡态理论基本假定(2)认为,反应体系的反应物状态维持Boltzmann平衡分配,因此反应体系沿着反应坐标通过过渡态区的平均速度〈v〉可以由下式给出:
![]()
g(v)为一个方向上的Maxwell-Boltzmann速度分布
![]()
式中,活化络合物的约化质量以m来表示,我们可以以一个粒子在长度为δ的一维势箱中的运动来表示活化络合物区沿着反应坐标的运动。则这个一维势箱中的能级为
![]()
其相应的配分函数为
![]()
因为式中只考虑了由反应物方向形成的活化络合物,所以乘以因子1/2来去除反向运动依据运动分离假定,将活化络合物沿反应坐标方向运动的配分函数与其他方向运动的配分函数分离,并作单独处理,如此则减少了一个振动自由度后的活化络合物配分函数,以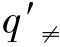 来表示。
来表示。
通过上面的几个方程推得过渡态理论中反应体系的速率常数表达式为
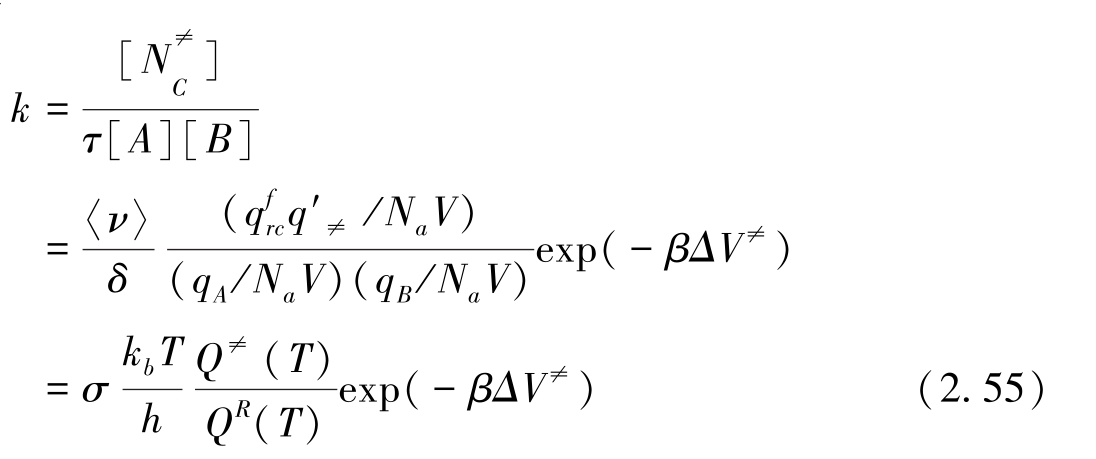
上式中的kb与h分别是Boltzmann常数和Plank常数;QR为反应物的单位体积的配分函数;Q≠为过渡态的单位体积的配分函数;σ是反应的对称数,即由反应物形成活化络合物过程中等同的、不可区分的通道数。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














