一、砷的微生物转化
1.砷的环境分布及迁移
(1)砷在环境中的分布及迁移
砷是地壳上第二十种最丰富的元素,是200种以上矿物的成分。环境中的砷99%以上存在于岩石中。砷在火成岩、石灰石、砂石和页岩中的平均浓度分别是1.5ppm、2.6ppm、4.1ppm和14.5ppm。砷广泛存在于各种矿物中,其中硫矿沉积物中浓度尤其高,其他铜、镍、铅、钴和金矿中也存在,这些矿物的冶炼过程会产生砷的三氧化物(As2O3),产生的砷化合物用于工业砷化学生产,代表性矿物包括砷硫化铁(FeAsS)等。FeAsS也是煤中的重要成分,矿物燃料的燃烧是砷进入环境的重要途径。
土壤和海洋也是砷的重要储库,地壳的平均浓度是3mg/kg,深海沉积物的砷浓度较高,大约为40mg/kg,世界范围土壤砷中值浓度为6mg/kg,典型范围在0.1~40mg/kg。源于硫矿沉积物的土壤砷浓度最高可达800mg/kg,然而有报告说受砷污染的土壤其砷浓度高达30.000mg/kg。海水平均浓度是2μg/L,而淡水中是0.5μg/L。
砷可以在水体中循环与迁移。主要的化学过程是砷的甲基化和脱甲基化,以及砷酸盐的氧化和还原;物理过程主要是吸附与沉积。
在接近中性pH值条件下,砷酸盐可被铁氧化物、氢氧化物以及锰、铝化合物吸附,主要是与前二者的结合。结合砷酸盐成为胶体和颗粒会从水柱流向沉积物,沉积物中的砷浓度通常比上层水高得多。亚砷酸盐的吸附现象也发生在水体中。此外有机物也影响砷的运动,腐殖酸能强烈吸附砷(在pH5~7范围),而富里酸(fulvic acid)能增加它的沥滤和运动。
沉积物中的氧环境对砷的迁移产生影响,在氧化型的环境中砷就会仍然被吸附到铁氧化物中,然而当大量有机碳投入到沉积物中,会导致氧的消耗和降低氧化还原电位,最低的氧化还原电位位于最下层。沉积物中的Fe(Ⅲ)Ox被还原成溶解的Fe(Ⅱ),并释放出吸附的砷到孔隙水(pore waters)中。在缺氧沉积物中大部分Fe(Ⅲ)Ox的催化还原是由微生物进行的。孔隙水中砷扩散往上到达氧化区后可以再和FeOx再结合和再沉淀。
砷在沉积物以及充分氧化的表面区域的循环导致砷主要积累在表面沉积层。砷酸盐往下扩散到硫酸盐还原区可以被还原成亚砷酸盐,这样在酸性条件下,就形成硫化砷(As2S3或AsS)这样的沉淀物,使砷以还原态存在,但如果沉积物受到物理干扰而运动到氧化性环境,砷会被氧化再释放到水柱中。化能无机营养(chemolithotrophic)硫氧化细菌也有助于这个过程和促进砷的运动。
(2)砷形态及其毒性
砷主要以氧化态的砷酸盐(Ⅴ价)、亚砷酸盐(Ⅲ价)、砷元素(0价)和砷气体(-Ⅲ价)的形式存在。在pH 7.0的水体中,这些化合物的主要形式分别是H2AsO、HAsO4、HAsO2、As和AsH3,在氧化条件下(0.2~0.5V),两种负离子的砷酸盐占优势,而在还原性环境中(0~0.1V),非电荷性的砷酸盐占优势。
元素砷罕见,仅在高还原条件下稳定存在。砷的甲基化形式如单甲基砷酸、二甲基砷酸、单甲基亚砷酸和二甲基亚砷酸也能被微生物和浮游植物合成而存在于水体中。
砷酸盐具有强烈的生物毒性,可以作为一种磷酸同系物起作用,能解耦联氧化磷酸化而抑制ATP合成。亚砷酸盐对硫氢基(sulfhydryl groups)有强烈亲和力,因而能抑制酶的活性。美国环保局和国际癌症研究中心已把砷酸盐划为人类致癌剂。
(3)使用及其暴露的风险
砷有广泛的利用价值,其主要用于卫生领域,其次是农业和工业部门。砷被用于农药、杀虫剂、落叶剂、木材防腐剂、防污油漆、食品添加剂、半导体芯片。
砷化合物的广泛使用以及含砷矿的溶出,这大大增加了环境中砷的流通量,因而也增加了对砷的暴露风险。砷暴露主要来源于食品和水源。EPA测定美国人吞食的无机砷大约14mg/天,约占全部砷吸入的20%。有机砷的吸收来源于食物。由于有机砷毒性较无机砷低,且易于快速排出,因此人们更关心对无机砷的吸收。海洋蟹、龙虾等含10~40mg As/ kg湿重。相比较小的狗鱼、鲶鱼等淡水鱼以及猪肉、牛肉也含砷,一般浓度<1mgAs/kg。水中的砷浓度受到局部的地化学的影响。水源水可以受到来源于金属硫矿(例如富砷黄铁矿)沥滤所产生的富砷铁氧化物的影响,其浓度高的可达1000mg/L,这个浓度要比世界卫生组织推荐的高限浓度(10mg/L)高得多。
2.砷的微生物转化
微生物所推动的砷转化包括氧化、还原和甲基化等基本过程。
(1)氧化
微生物氧化砷的能力主要表现在把亚砷酸盐氧化成砷酸盐。粪产碱菌(Alcaligenes faecalis)和砷氧化假单胞菌(Pseudomonas arsenitoxidans)已被证明具有这种能力,后者还能以化能自养代谢方式以亚砷酸盐为唯一能源生长。一些研究证明亚砷酸盐的氧化是共氧化机理控制的过程,在某些情况下,亚砷酸盐氧化可以耦联能量的产生。除了水体中的亚砷酸盐外,砷氧化假单胞菌能攻击含砷黄铁矿中的砷,而像氧化亚铁硫杆菌(Thiobacillus ferrooxidans)这样的细菌也能氧化含砷黄铁矿、三硫化二砷和硫砷铜矿。
(2)还原
微生物具有还原砷化合物(主要是砷酸盐)的能力,这种能力基于两个方面,其一是基于抗性的把砷酸盐还原或亚砷酸盐,然后排出体外;其二是基于生长的利用砷酸盐作为末端电子受体来氧化有机物取得能量生长。
砷酸盐的还原广泛存在,污水、瘤胃液(rumen fluid)、堆肥以及在各种淡水、海洋环境都存在。解乳微球菌(Micrococcus lactilyticus)的细胞抽提物和产气微球菌(M.aerogenes)能以氢作为还原剂把砷酸盐还原成亚砷酸盐。多种假单胞菌(Pseudomonas ssp.)和产碱菌(Alcaligenes ssp.)能还原砷酸盐、亚砷酸盐成砷化三氢(H3As)。甲烷杆菌属(Methanobacterium)菌株M.O.H的完整细胞和细胞抽提物能从砷酸盐产生二甲基砷。然而这些细菌还原砷酸盐的能力未能为它们的生长提供能量,而被认为是代谢过程的附带行为,是一种抗性解毒行为。两种被广泛研究的解毒系统是大肠杆菌和葡萄球菌属细菌的解毒成分。它们还原砷酸盐成亚砷酸盐,并把亚砷酸盐排出体外的系统的相关酶和蛋白质是由ars操纵子编码的。在大肠杆菌中,操纵子位于染色体和质粒R773上,位于膜上的ATPase复合体(ArsA和ArsB)主动输出细胞内的亚砷酸盐,ArsC是一种依赖于NADPH的胞质蛋白,其酶促砷酸盐还原为亚砷酸盐。金黄色葡萄球菌和木糖葡萄球菌的ars操纵子则分别位于质粒pI258和pSX267上。铜绿假单胞菌和肠道细菌科的成员(如志贺氏菌属、柠檬酸细菌属、克雷伯氏菌属、肠杆菌属、沙门氏菌属和欧文氏菌属)的ars操纵子位点与大肠杆菌类似位于染色体上。
许多细菌能在厌氧呼吸中利用砷酸盐作为末端电子受体生长。它们的生长能力和培养基中的砷酸盐浓度成比例。在同样电子供体条件下,砷酸盐作为电子受体比硝酸盐、Mn(Ⅳ)和Fe(Ⅲ)作为电子受体所得能量要少得多,但比硫酸盐要多得多。发生在淡水、咸水环境中沉积物泥浆中砷酸盐还原已被证明可以耦联到细胞产生能量,呼吸抑制剂以及解耦联剂(如二硝基酚、rotenone、2-heptyl-4-hydroxyquinoline、N-oxide)可以阻断砷酸盐还原。伴随砷酸盐还原的一般是乳酸盐、甲酸盐和乙酸盐的氧化。大多砷酸盐呼吸菌都在严格厌氧条件下分离出来,但许多分离菌能耐受少量氧或是微好氧的。砷酸盐呼吸细菌的砷还原速率一般为2×10-13~5×10-13molAs/cell/day。
能利用砷酸盐生长的细菌在系统分类及生理上十分多样。分离菌Desulfotomaculum auripigmentum、Bacillus arsenicoselenatis和Bacillus selenitireducens属于革兰氏阳性细菌,而Sulfurospirillum arsenophilus和Sulfurospirillum barnesii属于变形细菌(真细菌系统发育第一类群)的第五亚群(epsilon subdivision)。Chrysiogenes arsenatis是domain细菌一种更远分支的代表种。Woliella succinogenes也能利用砷酸盐作为末端电子受体,但其在分类上与Sulfurospirilla关系密切。还原砷酸盐的所有菌株都能利用乳酸盐作为碳/能源,但它们能利用的可选择的其他电子受体是不同的。Chrysiogenes arrenatis是至今分离出来的砷酸盐还原菌中唯一能利用醋酸盐作为碳源和电子供体的。D.auripigmentum是这类细菌中唯一能还原硫酸盐的,在某些情况下能导致As2S3的沉积。砷酸盐还原菌的分布不严格限于水环境(aqueous form),S.arsenophilus和D.auripigmentum已被证明能生长在砷酸铁(ferric arsenate FeAsO4·2H2O)上。
许多研究者对几种砷酸盐还原菌生长在砷酸盐或其他无机氧化物上的能力(在乳酸盐存在时)进行了分子生长收获量(YM)的实际测定和产生能量的计算(表11-6)。从表中可见砷酸盐是这些细菌的电子受体,所达到的生长和砷酸盐作为氧化剂在呼吸反应中得到的自由能大致上成比例。然而这些菌株利用砷酸盐的途径不总是同样的,例如SES-3和OREX-4是不完全氧化,乳酸盐被氧化成乙酸盐。而MIT-13则能把乳酸盐氧化成CO2。它们从As(Ⅴ)呼吸得到的ΔG0(耦合到不完全和完全乳酸盐氧化)差别在2倍以上,但观察到的生长收获量是相应不同的。
表11-6 几种砷还原菌利用砷酸盐和其他氧化剂时的生长量和取得的(计算)能量
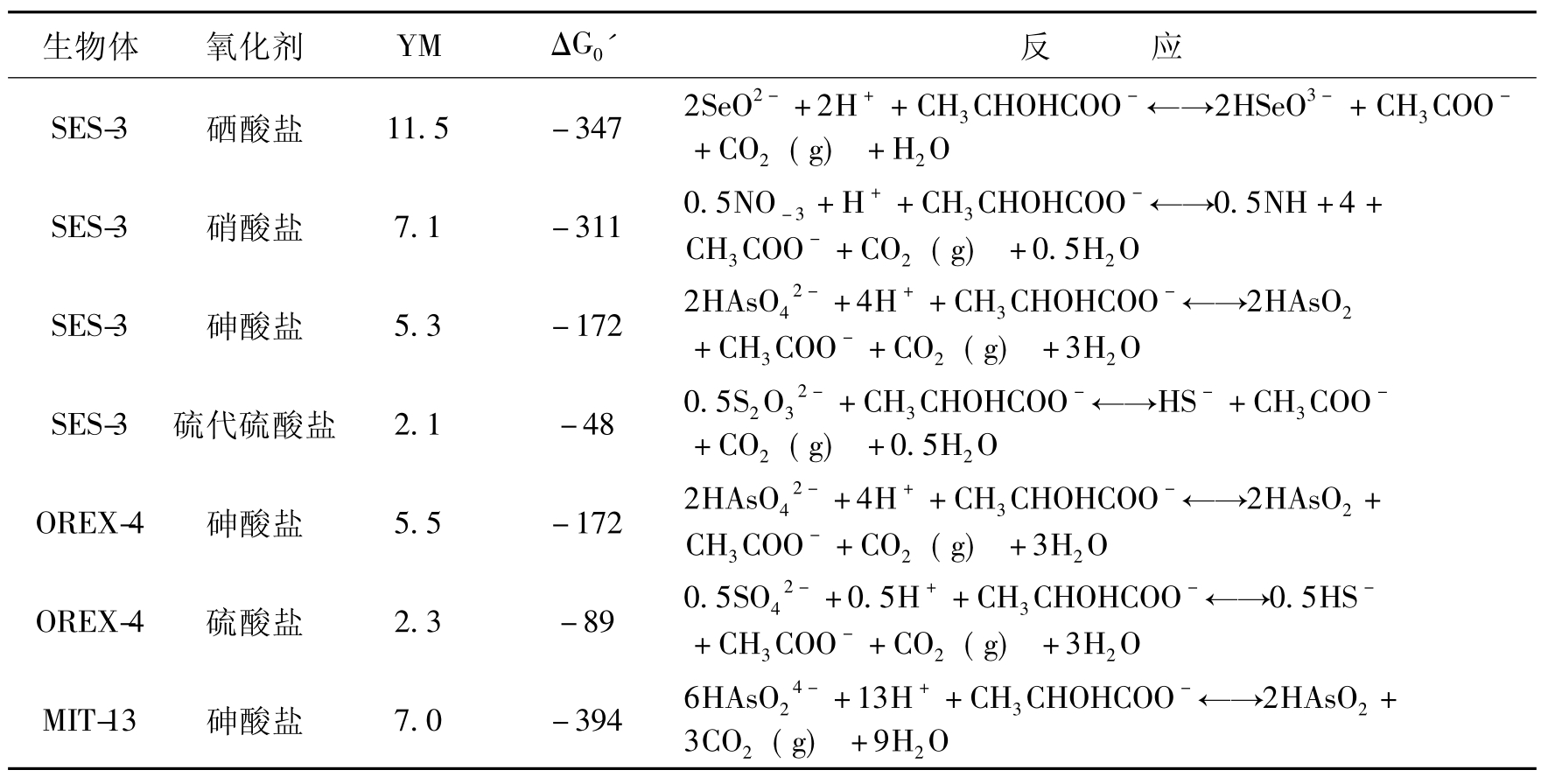
注:计算YM(g细胞/mol乳酸盐)时假设一个细胞干重1.9×10-10mg/细胞。计算(ΔG0'CkJ/mol乳酸盐)设定pH=7,PCO2=1个大气压;SES-3为Sulfurospirillum barnesii的一个菌株;OREX-4为Desulfotomaculum auripigmentum的一个菌株;MIT-13为Sulfurospirillum arsenophilus的一个菌株。
呼吸As(Ⅴ)还原的生化基础也得到研究,呼吸砷酸盐还原酶功能组成上也不同于大肠杆菌、金黄色葡萄球菌中抗砷酸盐的酶(ArsC)。S.barnesii的呼吸砷酸盐还原酶是多亚基内在膜蛋白,天然复合物的分子量超过100kU,C.arsenatis的酶是一种周质异质二聚体,二聚体由两种亚基组成,二者的分子量是87kU(ArrA)和29kU(ArrB)。S.barnesii的Km接近0.2mmol/L,C.arsenatic的Km是0.3mmol/L。二者的砷酸盐还原酶看来是利用辅因子(如钼、铁、酸不稳定硫(acidlabile fulfur))和锌转移电子到砷酸盐。S.barnesii在利用砷酸盐生长时存在b型细胞色素,这种色素也参与电子转移。呼吸砷酸盐还原酶也不能利用硝酸盐、硫酸盐、硒酸盐和延胡索酸作为电子受体,同时酶的合成受到砷酸盐存在的调控。相反ArsC酶是周质单体,其分子量大约为15kU,酶利用被还原的双硫醇(dithiols)转移电子,并有明显较高的Km。金黄色葡萄球菌有一个2mmol/L的Km,而大肠杆菌的Km是8mmol/L。
(3)甲基化
在用含砷颜料希尔绿着色纸糊的房间里曾发生了人的中毒事件。后来研究表明是由于墙壁上真菌生长,砷化物在这些微生物的作用下,释放出一种大蒜气味的挥发性毒物——三甲基砷所致。许多真菌能参与三甲基砷的形成,包括镰孢霉属、曲霉属、拟青霉属、帚霉属、青霉属、红色发癣菌、土生假丝酵母、粉红黏帚霉等。此外许多细菌也能把砷酸盐、亚砷酸盐转变成甲基砷。无色杆菌属、肠杆菌属的许多菌株能把砷酸盐转化成单甲基砷和二甲基砷。气单胞菌属、诺卡氏菌属的许多菌株可以把砷酸盐转变成单甲基砷、二甲基砷和三甲基砷。另一方面许多微生物还能进行脱甲基化过程,重新产生As(Ⅴ)。
和汞甲基化一样,甲基钴胺素是砷生物甲基化中的甲基供体。
(4)砷转化过程在修复砷污染环境中的应用
人类生产、生活活动的加剧造成大量的砷进入流通状态,从而对生态环境构成巨大的压力,砷污染生态环境的情况也常常发生。微生物对砷化合物的转化能力可以在砷污染环境的修复中发挥作用。有研究报道在受砷污染的湖泊沉积物中用最大概率数法(MPN)测定可培养砷还原细菌的密度接近104细胞/g湿重沉积物。而且这些沉积物的微宇宙也能在加入有机酸促进时还原加入的砷酸盐达50%以上。这种砷还原菌被证明能把砷从土壤转移到水体,从而有助于砷污染土壤的修复。而在异位生物反应器中则可以转化污染土壤中的砷,释放出来的亚砷酸盐然后和硫酸盐结合形成沉积物(如As2S3),或者再氧化(通过生物学或化学的)重新形成砷酸盐,形成的砷酸盐通过吸附到三价铁(ferric iron)上得到去除。对砷转化微生物的生理学、生物化学、生态学的深入研究将使我们理解在什么程度和什么条件下可以影响环境中的砷循环,从而有助于提出利用这些微生物修复污染的生态环境。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。

















