4.12 晶体结构参数与晶型的关系
无机化合物的晶型分布规律是晶体化学的一个重要课题,它对新材料设计、地质成矿规律研究等方面都有较大意义。一些科学工作者都在探讨晶体结构参数和晶型分布的关系。
从不同晶体结构型中知道,离子半径比对离子化合物结构有很大影响。拉维斯(Laves)等引入了空间充填概念作为几何大小对它的影响,把离子视为硬球,用一个空间充填因子ψ来表示。其定义是:晶胞中离子的体积和单位晶胞体积之比,即
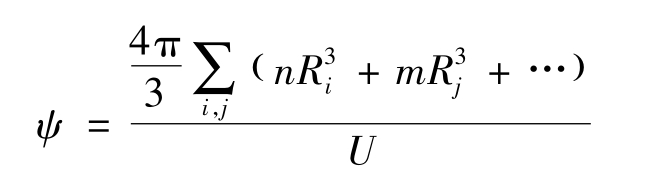
此处n,m,…是在单位晶胞体积U中原子i,j,…的数目,其半径分别是Ri、Rj,…。
现以AX化合物NaCl晶型为例。晶胞常数为a,则ψ=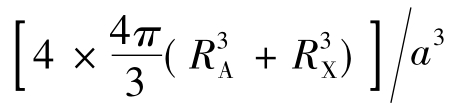 。若A-A接触,2R A= a/
。若A-A接触,2R A= a/ ,则
,则
![]()
此处ε=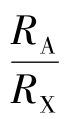 。若A-X接触,RA+RX=a/2,则
。若A-X接触,RA+RX=a/2,则
![]()
若X-X接触,a=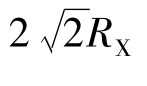 ,则
,则
![]()
将以上三式画出ψ-ε曲线,得出图4.35中NaCl曲线,转折点在ε= 0.414和2.42处,即前和后二式曲线的交点。用同样的方法求出CsCl和ZnS两晶型的ψ曲线,转折点分别在0.731和0.225处。这些转折点表明负离子在0.225、0.414和0.731时开始接触,低于这些数值,结构就不稳定了。该图表明ε>0.59时,CsCl晶型比NaCl晶型有较高的充填。因此当ε<0.731时NaCl晶型在高压影响下很容易变成CsCl晶型结构。由于空间充填曲线没有考虑相对自由能的大小,它不能反映化合物处于哪一种晶型最可能。根据计算,NaCl晶型在能量上比CsCl晶型有利,甚至有几种卤化物的ε>0.731是呈NaCl晶型结构,而不是CsCl晶型结构。事实上,长期以来就认为半径比仅仅是反映离子晶体结构处在某一临界值以下就不稳定,超过该临界值,该晶型才有存在的可能。但是究竟采用哪一种晶型结构,还有赖于相对地静电力作用。
上述方法只考虑几何尺寸对晶型分布的影响,对化学键性质影响忽视了。有人指出:一个原子最外层电子所占壳层的主量子数n可以用来反映该原子和同类其他原子间成键时方向性的量度,n愈大,愈丧失它的方向性特征。虽然这只限制在元素的成键,但莫士尔(Mooser)等考虑到化学键的方向性对晶体结构型分布的影响,就将上述概念引申到化合物中去。用化合物平均主量子数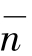 =
=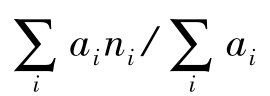 (式中ni和ai分别是化学式中第i个原子的价电子壳层的主量子数和在式中的数目)对电负性之差Δx作图,就可以将不同晶型区分开来。
(式中ni和ai分别是化学式中第i个原子的价电子壳层的主量子数和在式中的数目)对电负性之差Δx作图,就可以将不同晶型区分开来。

图4.35 CsCl、NaCl和ZnS结构填充图(点代表实测数据)
图4.36(a)是A族非过渡金属AX型化合物晶型分布图。其中闪锌矿型、纤锌矿型、NaCl型和CsCl型分占不同区域。取等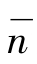 线,随Δx增加,这四种晶型按马德伦常数增大次序相继出现。CsCl晶型具有较高的配位数,高的马德伦常数,就处在NaCl晶型区域的右上方,即高的
线,随Δx增加,这四种晶型按马德伦常数增大次序相继出现。CsCl晶型具有较高的配位数,高的马德伦常数,就处在NaCl晶型区域的右上方,即高的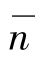 、Δx区。图4.36(b)是AX2型化合物晶型分布图。其他B族非过渡金属AX型、过渡族AX型、A2 X3型、A3 X4型和AB2 X4型等化合物也同样得出不同的晶型分布图。
、Δx区。图4.36(b)是AX2型化合物晶型分布图。其他B族非过渡金属AX型、过渡族AX型、A2 X3型、A3 X4型和AB2 X4型等化合物也同样得出不同的晶型分布图。
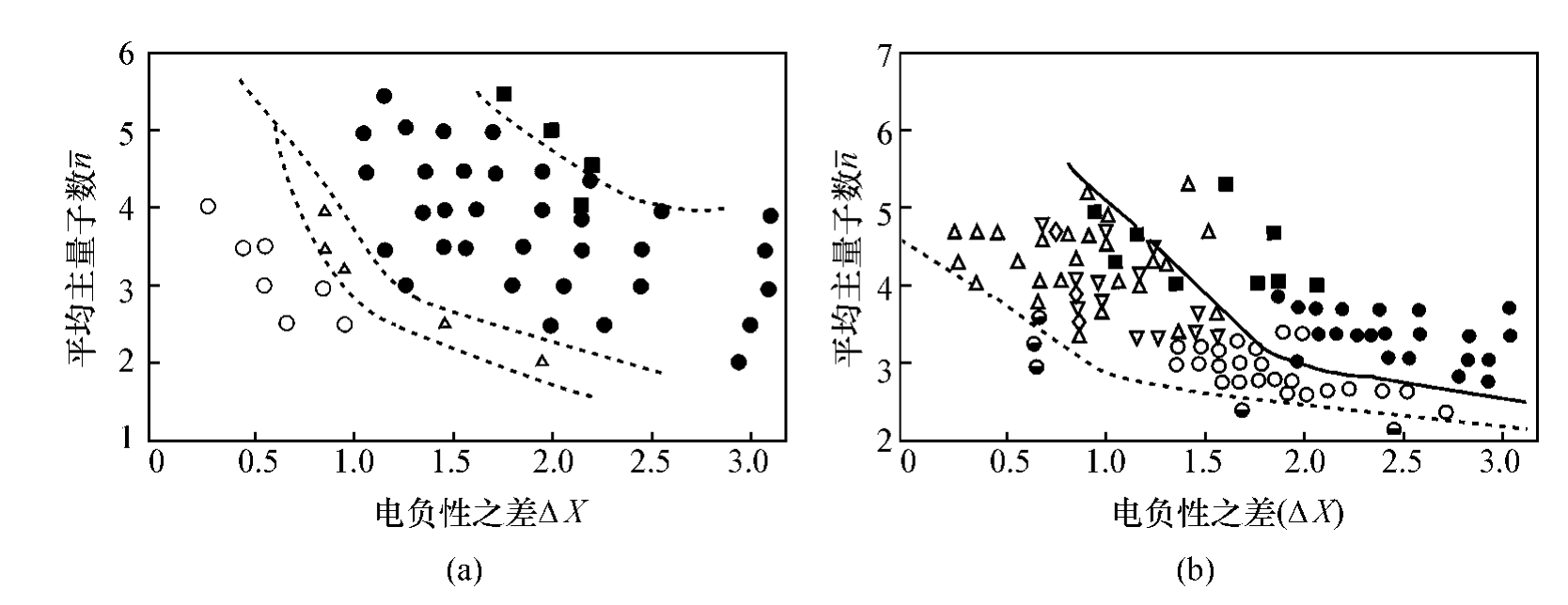
(a)A族非过渡金属AX型化合物:·—NaCl型;■—CsCl型;◇—纤锌矿△型;△—闪型;(b)AX2型化合物:■-PbCl2型;·—CaF2型;○—金红石型;△—Cd I2型;◇—MoS2型;▽—CdCl2型; —SiO2型
—SiO2型
图4.36 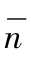 对Δx图
对Δx图
我国化学家陈念贻提出离子电荷半径比之和∑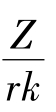 对电负性之差Δx和离子半径之比的乘积rc/ ra作图(rc、ra是正负离子半径),可以得出AX型化合物的晶型分布规律,如图4.37所示。不同晶体结构型处在不同区域。
对电负性之差Δx和离子半径之比的乘积rc/ ra作图(rc、ra是正负离子半径),可以得出AX型化合物的晶型分布规律,如图4.37所示。不同晶体结构型处在不同区域。

(a)AX型化合物的晶型分布图:▼—闪锌矿结构;△—纤锌矿结构;×—岩盐结构;■—CsCl结构;(b)含过渡元素的AX型化合物的晶型分布图:·—MnP结构;▲—NiAs结构;×—岩盐结构
图4.37 AX型化合物的晶型分布规律
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














