认识在不断深化
道尔顿的原子学说开创了化学的新时代,但由于受到当时科学技术水平的限制,该理论不可避免地存在着一定的局限性甚至错误,如将原子看成不可再分的微粒等。在这一理论提出后的近200年间,随着科学技术水平的不断进步,人们对于原子概念及原子结构的认识也在不断深化。大体经历了以下5个阶段。
道尔顿原子学说无法解答的问题之一就是物质起电的原因,在19世纪的最后几十年里,许多实验室都把注意力转为对气体导电的研究,从而发现了阴极射线。阴极射线的本质究竟是什么?这曾引起了长达25年的争论,最后于1879年被英国年轻的物理学家约瑟夫·约翰·汤姆孙(1856—1940)证明为一束带负电的微粒流,1897年他又用威尔逊云雾室测定了该微粒的电量和质量,这就是电子。电子的发现使人们开始认识到原子并非不可再分的实心球体,由于整个原子呈电中性,因此原子中还应有带正电荷的部分,汤姆孙认为正电荷均匀地分布在原子之中,而电子就像果料面包中的果料似的,散布在原子中的正电荷中,这就是原子结构的第一个模型——“布丁模型”(图1-5)。
图1-5 原子的布丁模型
1909—1911年间,来自新西兰的英国物理学家卢瑟福(1871—1937),利用α粒子(即He的原子核,带两个单位正电荷)进行轰击金箔的实验,发现α粒子的散射角远远大于汤姆孙原子模型应给出的角度,个别α粒子甚至折回(图1—6),这说明原子中带正电的部分体积很小(直径约10-15米),却集中了几乎原子的全部质量,他把这原子的带正电的部分称之为原子核。为了避免原子中的电子因原子核的静电吸引而落到核上,他提出了电子绕核作高速运动的“行星绕太阳”式的原子模型(见图1—7)。

图1-6 卢瑟福α粒子散射实验示意图

图1-7 卢瑟福行星式模型
1913年,丹麦物理学家玻尔(1885—1962)为了解释氢原子的光谱为线状光谱(即仅在一些特定波长处才出现光谱线,而不是连续分布的光谱线)的事实,综合了卢瑟福的原子模型和爱因斯坦(1879—1955)的光子学说,提出了自己的原子结构模型。在玻尔的氢原子模型中,电子仍是绕着原子核作高速的匀速圆周运动。但与卢瑟福原子模型的不同之处在于,原子有一系列的稳定状态,每一个稳定状态下原子的能量有一确定值,并有相应的电子绕核轨道半径和运动速度。当氢原子从某一能量状态变为另一能量状态时,就会发射或吸收特定波长的光谱线,其波长为:
![]()
式中,c为光速;λ为光谱线的波长;E1、E2为始态和终态的能量值;n为一常数,称之为普朗克常数,其具体值为6.62×10-34焦·秒。由于式中的E值为一些分立的值,所以λ也为一些分立的波长值。波尔还具体计算了氢原子各稳定状态下的能量值和电子绕核的轨道半径,其结果可见图1-8。波尔的原子结构模型成功地解释了氢光谱,并引入了量子化(即物理量只能是一些分立的量,跳跃式的变化)的概念,这是波尔的一大贡献。但波尔的原子结构模型无法定量地解释更多元素的原子光谱,对于化学键的形成的解释更是“无能为力”,暴露出其局限性。
以上3种原子结构模型不能全面地、科学地描述原子核外电子的运动状态,追究其根本原因,在于这几位科学家对于宏观物质的运动规律深深地印在了自己的脑海里,从而忽略了宏观物体与原子、电子等微观粒子由于质量和活动范围的巨大差异带来的运动规律上的本质差异。实际上,由德国物理学家海森堡(1901—1976)提出的“测不准原理”可知,像原子中的电子这一类受束缚的微观粒子,其本质的属性除微粒性的一面之外,还表现出波动性的另一面,其运动根本就没有确定的轨迹,它们的运动遵循的是物理学中的另一范畴的规律——量子力学规律(1926年提出)。用量子力学理论处理原子体系,所得到的结果即为现代的原子结构,其结论已为大量的实验事实所证明。现代原子结构的具体内容,本书将在以下的几节中作比较详细的介绍。
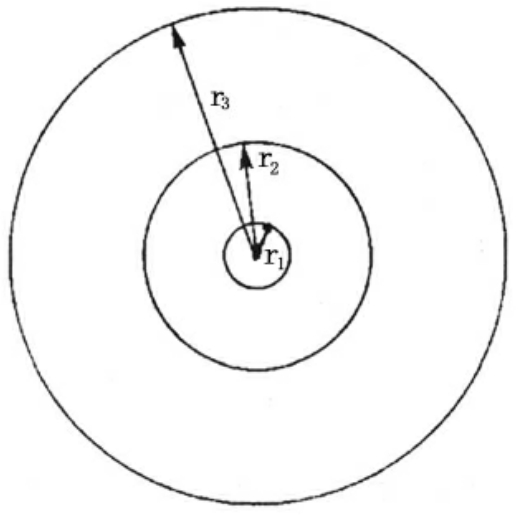
图1-8 波尔氢原子轨道半径
在研究原子核外电子运动状态取得进展的同时,对于原子核组成的认识也有了突破:元素放射性的发现,特别是皮埃尔·居里(1859—1906)和玛丽·居里(1867—1934)夫妇的工作,表明原子核也是可分的,也存在着结构问题。1920年,卢瑟福把氢核作为一种基本粒子,将其称之为“质子”,质子带1个单位正电荷,质量为电子的1836倍,原子核带正电就是由于原子核中质子的“贡献”;1932年,查德维克(1891—1974)用α粒子轰击金属铍时,又发现了原子核内另一种质量与质子相差无几但不带电荷的微粒,这就是“中子”,中子是构成原子核的另一种基本微粒。原子的质量数等于原子核中质子数和中子数之和,而中子的存在对于原子核的带电情况不作贡献,原子的核电荷数等于核内的质子数。查德维克因发现中子而获得了1935年度的诺贝尔物理学奖。这其中还流传着这样一段趣闻:当卢瑟福要将发现中子的诺贝尔奖发给查德维克时,有人提议,居里夫人的女婿和女儿约里奥·居里夫妇也应分享这一奖项,卢瑟福幽默地回答说:“发现中子的诺贝尔奖就单独奖给查德维克吧!至于约里奥·居里夫妇嘛,他们是那样的聪明,相信不久后他们就会因别的项目而获奖的。”情况果然如此,约里奥·居里夫妇在同一年因合成出人工放射性同位素而双双获得了诺贝尔化学奖。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















