腐植酸对高岭土吸附四价铀的影响
Nick Evans1, Peter Warwick1, Tara Lewis1, Nick Bryan2 著
王曰鑫 戚新革 译
(1 英国拉夫堡大学化学系 拉夫伯勒
2 英国曼彻斯特大学化学系放射能化学研究中心 曼彻斯特
3 山西农业大学资源环境学院 太谷 030801)
摘 要:在土壤中,对放射性废物处理的安全性评估,要求评价放射性核素的迁移。pH值从4到8,腐植酸浓度从15 mg/kg到200 mg/kg条件下,腐植酸对高岭土吸附四价铀的影响试验表明,没有腐植酸的情况下,20%~40%的四价铀存在于溶液中;pH值越高,吸附作用越强。在腐植酸的存在下,随着腐植酸浓度和pH值的升高,四价铀的溶解度随之增大,四价铀在腐植酸中的可溶性最高可达90%。腐植酸吸附和四价铀的吸附是对立的,通过测量腐植酸的吸附,可以比较腐植酸吸附四价铀的能力高低。但是,随着pH值的上升,这种吸附作用的影响减弱。敏感性分析表明,在这些系统中,腐植酸表面吸附是线性可加模型模拟这些体系的控制。
关键词:四价铀 腐植酸 三元系统 线性可加模型
Influence of Humic Acid on the Sorption of Uranium(IV) to Kaolin
Nick Evans1, Peter Warwick1, Tara Lewis1, Nick Bryan2 write
Wang Yuexin3, Qi Xinge3 translate
(1 Department of Chemistry, Loughborough University, Loughborough, UK
2 Centre for Radiochemistry Research, School of Chemistry, The University of Manchester, Manchester, UK,
3 College of Resources and Environment, Shanxi Agricultural University, Taigu, 030801)
Abstract: Safety assessments for radioactive waste disposal require estimations of the migration of radionuclides in soils. The influence of humic acid(HA) on the sorption of uranium in its +4 oxidation state to kaolin has been examined from pH 4 to 8, with HA concentrations of 15~200 ppm. In the absence of HA, 20%~40% of the U(IV) was in solution, with more sorption occurring at higher pH. The presence of HA solubilised up to 90% of the uranium with higher solubilities at higher HA concentrations and higher pH values. Uranium sorption was mapped against HA sorption, and it was found that there was a lower level of U(IV) sorption than can be accounted for by just measuring HA sorption. However, this effect got less marked as the pH rose. Sensitivity analysis indicated that the fraction of surface-bound HA is the controlling parameter for modelling in these systems.
Key words: Uranium(IV); humic acid; ternary systems; linear additive model
在异构地面环境中,对放射性废物处理的安全性评估,要求评价放射性核素的迁移。水生系统中矿物质内放射性核素的吸附对地壳的物质迁移产生了重要的影响。天然有机物,尤其是腐植酸(HA),可以对自然固体物中放射性核素的吸附产生极大地影响。非吸附性和吸附性腐植酸存在于地壳,并能够对放射性核素的迁移产生负面影响,这是由于有金属—腐植酸络合物的形成。在HA浓度很高,pH值很低时,腐殖质能提高矿物性金属的吸附能力。
许多潜在的因素造成存储库中放射性废物的数量不断地减少。存储库中铀一般呈+4价,简称U(IV)。一般情况下,U(IV)是难溶物质,基本上保持被吸附状态,比如是固体沉降(铀酰),或是吸附到了矿物表面。然而,在环境系统中,U(IV)跟HA的关系复杂,并且呈游离状态。同时,HAU(IV)络合物可以吸附到表面,变成吸附状态。本文以高岭土为代表,研究了pH值从4到8,HA浓度增大对U(IV)固液相分配的影响。
金属—腐植酸—矿物二元和三元系统的相互作用已经得到了广泛的研究,特别是利用从二元系统中得到的数据来建立三元系统的模型。本文中,线性相加模型(LAM)被用来预测三元系统中U(IV)的分配,此三元系统设计为HA、高岭土和U(IV)。
因此,在这个三元系统中,分析二元之间的相互作用,如U(IV)和HA间(形成稳定络合物常数)、HA和高岭土间(分配系数为Rd值)、U(IV)和高岭土间(分配系数为Rd值)的相互作用可知:Rd值对U(IV)来说具有决定性作用。该研究结果被用来预测地壳内,HA对U(IV)迁移的影响。
1 U(IV)的形态
本研究中用到的U(IV)形态是非常重要的,它决定着U(IV)在不同pH值(pH值为4~8)和电位(Eh值为-600~-700 mV)下的状态。计算结果经过了严格的挑选,用来评估U(IV)水解产物的稳定常数,从而决定U(IV)pH值从0到14的不同状态。可溶性产物UO2的logKsp=54.5,反应式为:
![]()
计算结果如图1。

图1 JCHESS U(IV)形态方程(Ⅳ)
Fig.1 JCHESS speciation of uranium(IV)
注:稳定常数来自Neck和Kim(2001)的研究成果。
该计算结果运用了JCHESS形态方程。该方程中U(IV)的最初浓度是1×10-9 mol/L,与本实验中相似。图1表明,在pH值为3时,U(IV)的主导形态是U(OH)22+和U(OH)3+,pH值从6到14时,主导形态是U(OH)(液相)。需要注意的是,U(OH)2+42和U(OH)3+的常态是估算的,在这个平衡式中,±1价的改变都会使铀的离子形态发生很大变化。
2 实验
除另有说明外,本文中所用到的化学药品都为分析纯。去离子水是从Barnstead/NANO纯净水仪取得,所有溶液是在氮气操作箱中准备的。使用氮气喷射煮沸以及与铁接触除去氧气的水。Eh值用OCRN2电导仪进行实时监测。如果样品的电位超过了-500 mv,就丢弃。高岭土(由Aldrich公司提供,颗粒平均直径570 nm,BET比表面积10.88 m2/g,CEC5.2 meq/100 g)作为研究对象(美森1996)。铀(U,分子质量233)是从UK阿莫汉姆购买的(美森1996),实验过程中全部使用。HA(颗粒分子质量为5700 amu,平均直径为2.663 nm,质子容积为5.3×10-3 mol/L)。4—吗啉磺酸(MES,Fisher)(0.1 mol/L,全过程)用来稳定pH值,并且提供最小的离子力。实验准备和操作是在常温下的氮气操作箱里进行的。样品的活性由TRI-Carb 2750TR/LL型号的液体闪烁计数器(产自堪培拉)测定。UV-Vis吸附测定由PU 8730—扫描分光光度仪在254 nm下完成。pH值是用J-玻璃电极和O-720A pH计测定的。离心作业用的是H-EBA30离心机。
铀原液的配制:无定形沉淀UO2•2H2O加入NG瓶中,再加入250 mL NaOH(0.4 mol/ L),500 mL 0.10 mol/L Na2S2O4溶液和250 mL UO2(NO3)2溶液(0.01 mol/L)。静置2周后,离心,用Na2S2O4(0.05 mol/L)溶液洗净,再次离心,转速为5500转/分钟。然后大部分上清液经0.2 μm的滤纸过滤后,用于测定铀的溶解度。溶解度的测定结果为1.2×10-9 mol/L~4.6×10-9 mol/ L,这说明了U(IV)完全正常,可用来配置不同pH值下的U(IV)溶液浓度。U(IV)溶液浓度分别为1.0×10-9、5.0×10-10、1.0×10-10、5.0×10-11和1.0×10-11 mol/L。每个溶液均取样20 mL,放入NG瓶中,再加入0.1 g高岭土,每个样品一式两份,混合均匀,静置14 d,测定pH值,然后通过0.2 μm的过滤器,测定溶液中上清液的放射性(测定的样本不含有固体物质,并且该瓶壁上的金属和HA的吸附程度可忽略不计)。
为了确定HA在固相和液相之间分配,以MES缓冲液配制浓度为15~200 mol/L的液相HA,经适当的稀释后,254 nm下测定吸光度,以MES缓冲液作为对比溶液。不同浓度的溶液各取15 mL,放入NG瓶中,加入0.1 g高岭土,经反复平衡后,样品过滤,测pH值,并在波长为254 nm下测定吸光度。腐植酸水溶液浓度从254 nm下的腐植酸溶液(mg/L)的吸光度标准曲线上查得。
3 三元实验
从上述实验溶液中吸取相同浓度腐植酸溶液,一式两份,加入NG瓶中,并加入0.1 g高岭土,再加入U(IV)溶液混合均匀后放置14 d,过滤,测定电位、pH值及吸光度,最后各取2 mL样品测定其活性。
4 线性可加模型
线性可加模型的一个重要假设是三元系统中包含有金属、HA和矿物。液相和矿物固相之间金属的分配可以根据从二元系统中得到的分配比例来测定。普遍使用的模型是:
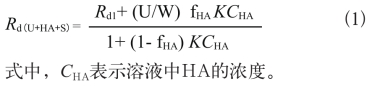
公式(2)中3个二元系统之间的相互作用如下:

5 结果与讨论
EH的显著变化证明了U(IV)的存在。以标准氢电极法测定氧化还原电位,电位值增加了204 mV,但铀的溶解度没有增加,这表明U(IV)氧化态不存在[不考虑原液是否接触过高岭土,混入了HA,存在被氧化的U(IV)等]。事实上,电位值很低就意味着铀仍然是+4价状态。同时值得注意的是这些溶液始终存在连二亚硫酸盐。
5.1 二元系统——铀和高岭土(Rd1)
U(IV)和高岭土之间的Rd1(分配系数)是pH=4.0±0.4,Eh=-603±33时为319±38 mL/g;pH=6.12±0.4,Eh=-625±46时为540±106mL/g;pH=8.29±0.15,Eh=-603±27时为790±145mL/g。在没有HA的情况下,U(IV)在溶液中的百分含量从40%(pH=4)到20%(pH=8)。由于连二亚硫酸盐不与U(IV)络合,对高岭土的U(IV)吸附的影响可以忽略不计。在pH=4时,该吸附剂可能为两种主要物质的混合物,例如U(OH)22+和U(OH)3+。Rd值随着pH上升而上升,直至pH=8时,Rd大概达到800 mL/g为止(图2),此时吸附剂是由U(OH)4(固态)组成。Tarlor和Theng在1995年就报道过高岭土上有2个不同的表面(基础表面和边缘表面),前者带有小部分永久负电荷,后者在性质和规模上依赖于环境的pH值,因此边缘表面可以用来解释吸附随pH值的变化和吸附U(IV)形态的变化。
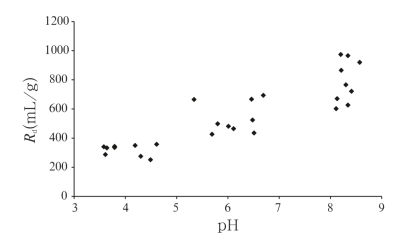
图2 二元系统U(IV)-高岭土中,Rd随pH的变化
Fig.2 Variation of Rd with pH (~3.5 to~8.5) for
the binary U(IV)–kaolin system
注:Eh=-620mV,[U(IV)]=2×10-9到1×10-11 mol/ L,0.1 g高岭土,20 mL溶液。
5.2 二元系统——HA和高岭土(fHA)
如果pH值保持不变,线性可加模型可以成功的被应用,并在所有二元和三元系统中均相同,需要使用缓冲剂控制过程。在没有缓冲剂的情况下,需加入HCl或NaOH控制pH值,进而调控实验。然而,调控下的pH会随时间而变化,缓冲液中HA的吸附对高岭土没有明显的影响。因此,所有的二元和三元系统中用到的缓冲液中都含有HA,数据见表1。高岭土中HA(浓度为15 mg/kg)的含量会随pH值上升而下降,pH值为4.12时,HA的含量为0.96 mg;pH值为4.61时,HA的含量为0.93 mg;pH值为7.56时,HA的含量为0.61 mg。在HA浓度更高时,也出现相同的情况。对于这种现象,许多不同的机构已经提过,并超出了本研究的范围。
表1 在pH值为4、6或8,没有U存在的情况下,HA吸附于高岭土的分数
Tab.1 Fraction of HA bound to kaolin in absence of uranium at pH 4, 6 and 8, [HA]=15~200ppm, 0.1g kaolin,20cm3 sdution
注:[HA]=15~200 mg/kg,0.1 g高岭土,20 mL溶液。
5.3 二元系统—U和HA
U(IV)和AHA之间的稳定常数有指示pH值的功能,但并不是表示每个pH值的对数值。AHA是在实验室中合成的有机物质,本实验参考了Reiller等人测定结果的关系式:logβHA=3.26 pH+0.14,作为上述关系的推导。同时也参考了Warwick等人由实验获得的U(IV)—AHA的对数值。
5.4 三元系统—U、HA和高岭土
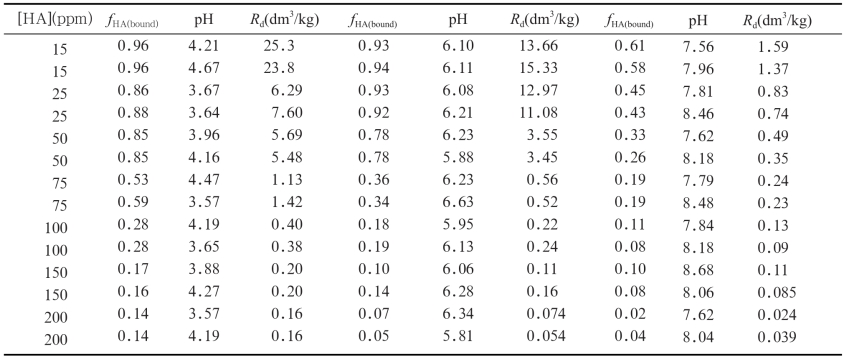
在U(IV)—高岭土二元系统中,20%~40%的U(IV)溶于液体中,如果pH值增大,会有更大的溶解量。HA的存在溶解了90%的U(IV),如果有更高的HA浓度和更高的pH值,U(IV)溶解变的会更大。然而,根据实验结果可得出以下结论:pH值为4时,低HA浓度(15~50 mg/kg)即可产生较高的U(IV)吸附能力,10%~35%的U(IV)溶解;当没有HA的情况下,溶解度可达40%。在HA浓度为75 mg/kg时,U(IV)的溶解度为42%;在稳定系统中,高HA浓度(100~200 mg/kg)可使U(IV)的溶解度达到94%。pH值为6时,没有HA时,有27%的U(IV)溶解;当HA浓度超过15 mg/kg时,U(IV)的溶解度会高于27%;当HA浓度为200 mg/ kg时,U(IV)的溶解度将达到85%。pH=8,HA不存在时,U(IV)溶解度为20%;HA浓度小幅度增长,例如当HA浓度增至15 mg/kg时,也会导致U(IV)溶解度大幅度增长;当HA浓度为15 mg/kg时,U(IV)溶解度为40%;而当HA浓度为200 mg/ kg时,溶解度会增长到90%。系统的电位情况:pH=4时,Eh=-588±48mV;pH=6时,Eh=-646±29mV;pH=8时,Eh=-595±40mV。这些数据表明,控制实验过程,可确保铀始终为+4价状态。
在三元系统中,Rd和HA在3种不同的pH值下的浓度关系在图3中体现出来,将这些数据和有关文献中的数据相比较发现,在自然有机物质存在的情况下,光化性吸附随HA浓度升高而降低,且具有相似性,这种现象由Schemide等人在2000年发现,他检验了千枚岩中矿物在HA存在的情况下对U(IV)的吸附。然而,在低浓度下关于HA 和黄腐酸对膨润土的吸附,Xu等(2006年)却得出了相反的结论。Cheng等(2007)发现,在本文研究的pH值范围内,HA对Na-累托石中钍(IV)的吸附没有影响,而黄腐酸却降低了吸附等,本文的结论与此类似。因此,文献中没有提出明确的模式。
图3 三元系统中,PH=4,6,8时,分配系数(Rd)随HA浓度变化
Fig.3 Variation of distribution coefficient (Rd) as function of [HA] internary system at pH 4, 6 and 8
注:[HA]=15~200 mg/kg,0.1 g高岭土,20 mL溶液,[U(IV)]=1×10-9 mol/L;pH=4时,Eh=-588±48 mV;pH=6时,Eh=-646±29 mV,pH=8时,Eh=-595±40 mV。下同。
线性可加模型已被多次引用。使该模型成立的一个假设是矿物中HA含量远小于高岭土的含量,这表明高岭土表面是不饱和的。如果表面不饱和,U(IV)就有可能直接结合到高岭土表面,或是通过囊括了HA的三元系统结合。通过假设单层覆盖度,可以对高岭土表面HA的覆盖度进行估算。HA分子是平均地镶嵌在表面上,当HA浓度为15 mg/kg时,平均每瓶中含有2.38×1016个分子。如果给予这些分子5.57×10-18 m2的面积,就是给予了被HA覆盖的高岭土0.13 m2表面积。然而,这是假设完全吸附,fHA=0.96,被15 mg/kg HA覆盖的高岭土表面积是0.96×0.13 m2=0.125 m2,允许镶嵌78.56%,这样表面覆盖度就为9%。
前面提到U(IV)和HA间有强烈的相互关系,可以认为这种相关性是通过三元络合形成的。例如,U(IV)的分布是随着HA的分布而变化,这个结论可以通过实验从以下关系式得到验证:

因此,[HA]吸附/[HA]溶液与[U]吸附/[U]溶液互作的曲线图就可绘制。如果梯度接近于1,线性可加模型就不可用,因为[U]吸附和[U]溶液是由[HA]吸附和[HA]溶液决定的。如果梯度不接近于1(图4),高岭土表面对[U]吸附有直接影响,线性可加模型就可以用来决定U(IV)固液相间的分配比例。
图4是高岭土吸附U(IV)溶液的比例和高岭土吸附HA溶液比例的分布函数曲线图。如果U(IV)分配遵循HA的分配规律,梯度值可能为1。然而,本文中这些系统,pH=4、6或8时,梯度值分别为0.387、0.457和0.635。这表明,通过U(IV)吸附比测得的HA吸附要低。同时,在特定pH下,HA表面的任何分馏导致比等量的水络合物吸附量更低的U(IV)-HA络合物的形成。然而,这种影响会随pH升高而变弱。
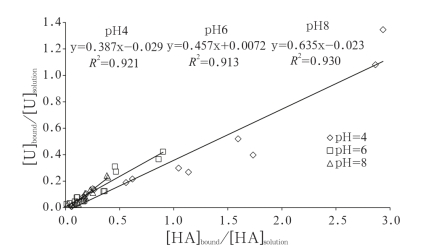
图4 三元系统中,PH=4,6,8时,U(IV)在固液相之间的分配随HA分配的变化
Fig.4 Distribution of U(IV) between bound and solution phases as a function of the distribution of HA in ternary systems at ca.pH 4, 6 and 8
三元Rd值域HA浓度的分布函数见图5。
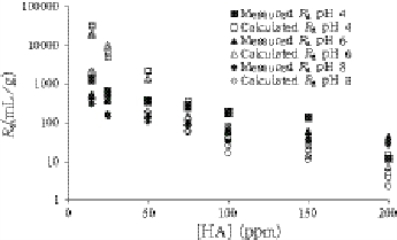
图5 pH=4,6,8时,计算和测得的三元Rd值随HA浓度的变化
Fig. 5 Calculated and observed ternary Rd values as a function of HA concentration at ca. pH 4, 6 and 8
由图5可以看出,由线性可加模型计算出的三元Rd与测量出的三元Rd略有不同。尽管线性可加模型没有考虑HA对高岭土结合位点的阻碍和高岭土吸附对HA结合位点的阻碍,以及空间位阻效应、静电作用和由于吸附而被分开的HA,但从图5中仍可看出,当pH上升和HA浓度更高时,这个模型还是比较准确的。敏感性分析表明,在这个系统中,吸附到表面的HA含量是线性可加模型的控制参数。在二元系统中U(IV)—高岭土的Rd值或液相U(IV)—HA络合物的稳定常数发生变化时,对计算出的三元Rd没有很大影响。然而,二元系统高岭土—HA中,fHA的10%的改变,可通过逐级变化导致计算的三元Rd值的改变。该模型过度依赖于参数值的情况表明,此预测系统中线性可加模型可能不是最佳的方法。
6 结论
在U(IV)—表面二元系统中,约20%~40%的U(IV)为在溶液中,pH越高,吸附越强。U(IV)在HA中的溶解度高达90%,在更高的HA浓度和pH值下,会有更高的溶解度。然而,U(IV)的吸附比测得的HA的吸附要低,这表明在特定pH值下,HA表面的任何分馏都会导致比等量的水络合物更低的U(IV)-HA络合物的形成。这个影响会随pH值上升而变弱。灵敏性分析表明,在平衡系统中,吸附到表面的HA含量是线性可加模型的控制参数。该模型极度依赖于参数值的情况表明,线性可加模型可能不是预测这些体系的最佳方法。
致谢和参考文献(略)
译自:Envirnomental Chemistry Letters, Online FirstTM,17 September 2009。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















