第2节 人类染色体
染色体是遗传物质的载体,生物界中每一物种都有其特定的染色体数目及形态学特征,并且稳定地世代传递。正常人性细胞的全部染色体称为一个染色体组(chromosome set)。具有一个染色体组的细胞称为单倍体(haploid),用n表示;如人的生殖细胞含有23条染色体,属于单倍体,n=23。若细胞中具有两个染色体组,则被称为二倍体(diploid),用2n表示;如人的体细胞包含46条染色体,包括两个染色体组,因此是二倍体,2n=46。
一、人类染色体的特征和类型
在细胞周期的中期,染色体达到最大凝集,形态清晰、典型而最易于辨认,所以常被用于染色体研究和临床染色体病的诊断。显微观察表明,每一中期染色体含有两条姐妹染色单体(sister chromatid),两条单体之间借着丝粒(centromere)相连。着丝粒处含有较多异染色质,凹陷而狭窄,着色较浅,又称为主缢痕或初级缢痕(primary constriction)。着丝粒将染色体纵向分为两部分,即长臂(q)和短臂(p)。染色体长臂和短臂的末端各存在一特化部位——端粒(telomere),其中含有端粒DNA和端粒蛋白,对维持染色体结构的稳定起着重要作用。部分染色体在染色体纵轴上还具有除主缢痕外的另一缢缩的浅染区,称为次缢痕(secondary constriction)。人类染色体中13、14、15、21、22号染色体的末端存在一球形或棒状结构,称为随体(satellite),随体通过一细丝与染色体臂相连(图2-5)。
按照着丝粒的相对位置,人类染色体分为以下三类:①近中着丝粒染色体(metacentric chromosome),着丝粒位于染色体纵轴1/2至5/8处,染色体长臂与短臂接近等长;②亚中着丝粒染色体(submetacentric chromosome),着丝粒偏离中部,位于染色体纵轴5/8至7/8处,长臂与短臂长度有明显差别;③近端着丝粒染色体(subtelocentric chromosome),着丝粒位于染色体纵轴7/8至末端处,短臂很短(图2-6)。此外,在一些动物细胞中尚存在第四种染色体类型,即端着丝粒染色体(telocentric chromosome),其着丝粒位于染色体末端,没有短臂,人类正常细胞不存在此类染色体,但在肿瘤细胞中可见到。
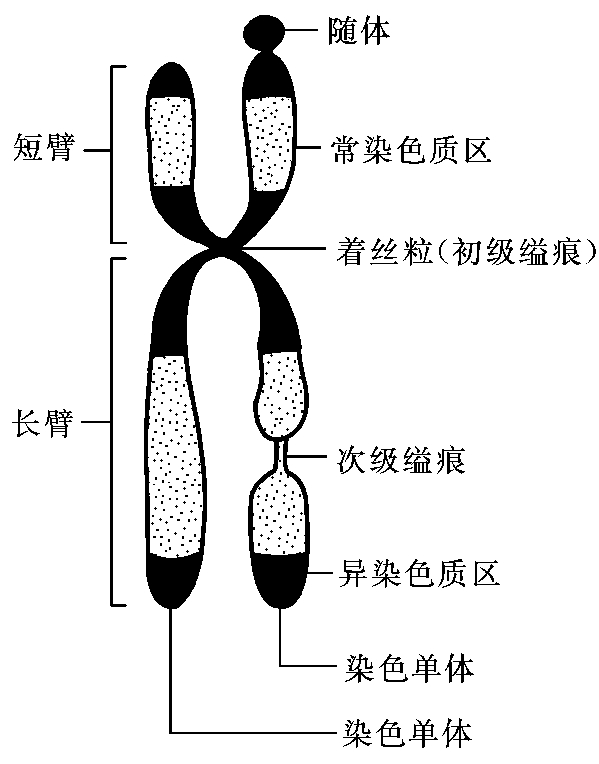
图2-5 中期染色体模式图
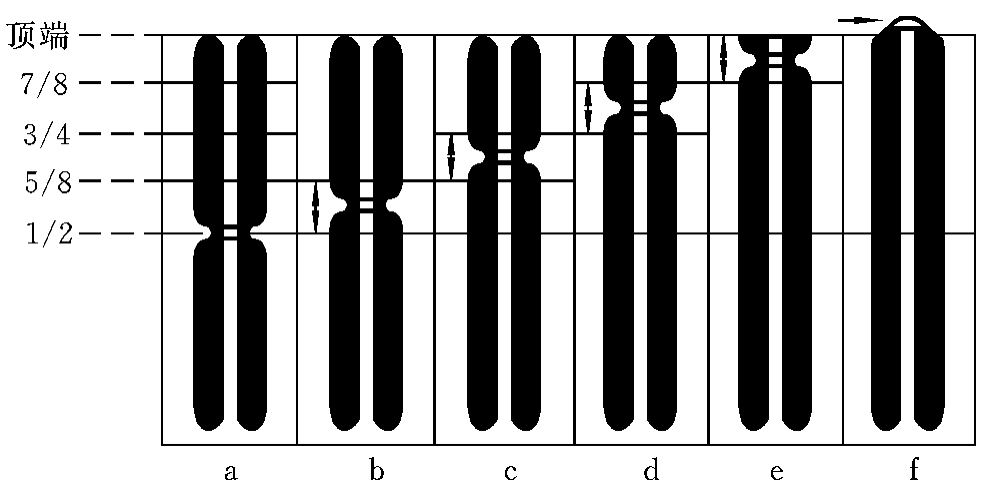
图2-6 染色体的类型
二、人类的正常核型
核型(karyotype)是指一个中期体细胞中的全部染色体,按其大小、形态特征依序排列而成的图像。对这些图像进行染色体数目、形态特征的分析称为核型分析(karyotype analysis)。
(一)人类染色体非显带核型
1956年蒋有兴(Tjio)和Leven证实了人体正常体细胞含有46条染色体。后来多种染色体异常的发现,大大促进了对染色体及相关疾病的研究。为了统一对异常染色体的描述,1960年在美国丹佛、1963年在英国伦敦、1966年在美国芝加哥相继召开了三次国际会议,讨论和制定了人类染色体统一的标准命名系统,即丹佛体制(Denver system)。根据丹佛体制,正常人体细胞中的46条染色体分成23对,其中第1~22对为常染色体(autosome),男女均有;另外一对为性染色体(sex chromosome),男女不一样,男性为XY,女性为XX。这23对染色体按照其大小和着丝粒的位置由1号依次编到22号,并分成7组(A、B、C、D、E、F和G组),X染色体分在C组,Y染色体分在G组(图2-7)。
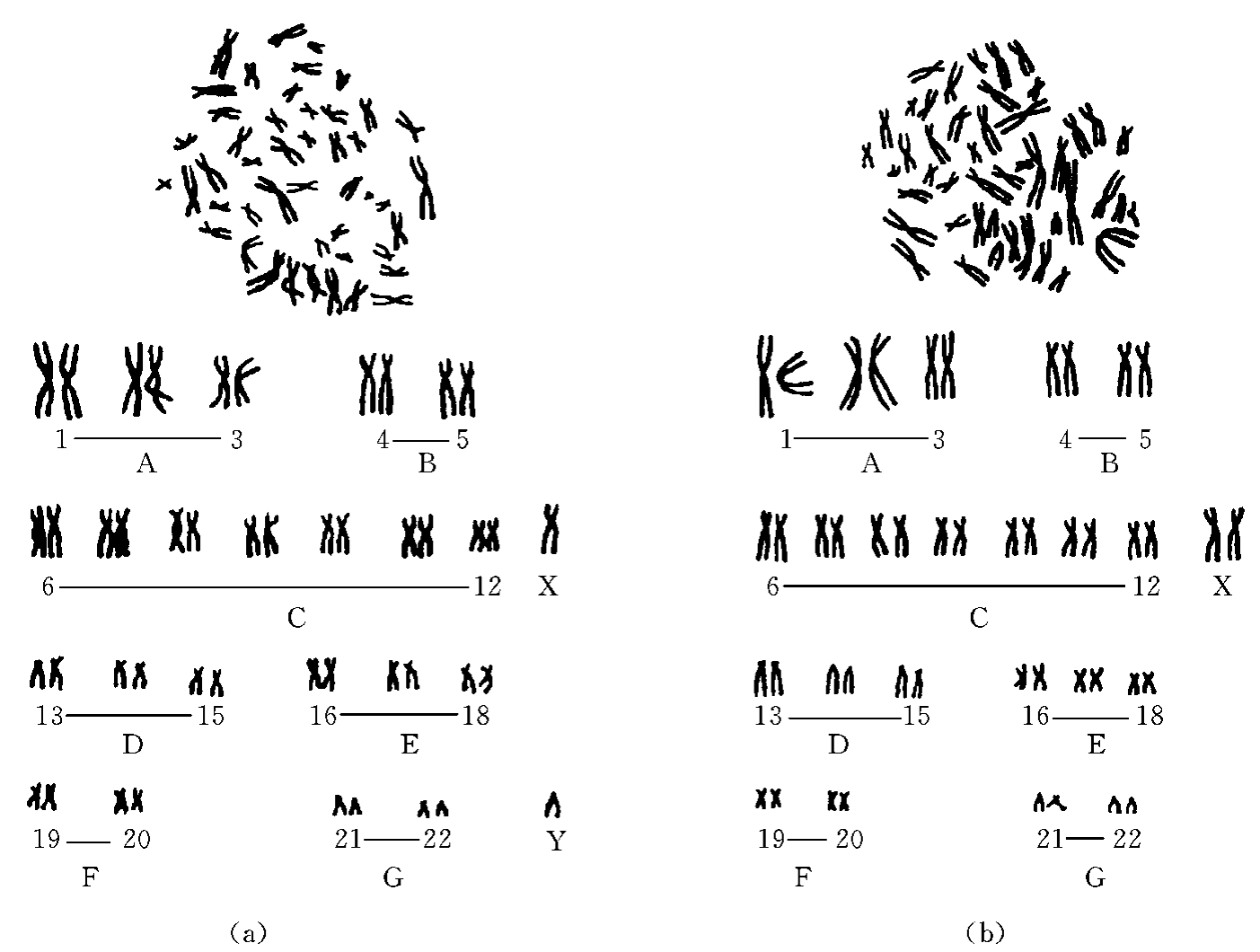
图2-7 正常男性核型(a)和正常女性核型(b)
(1)A组。1~3号染色体,体积大,易于区分。1号染色体最大,为近中着丝粒染色体,长臂近着丝粒处常见次缢痕;2号染色体略小,属于亚中着丝粒染色体;3号染色体是此组中最小的,为近中着丝粒染色体。
(2)B组。4~5号染色体,均为大的亚中着丝粒染色体,但彼此不易区分。
(3)C组。6~12号染色体和X染色体,都是中等大小的亚中着丝粒染色体,故组内区分较困难。9号染色体长臂常可见次缢痕;6、7、8、11号染色体和X染色体的短臂较长,而9、10、12号染色体的短臂较短;X染色体的大小介于7号染色体和8号染色体之间。
(4)D组。13~15号染色体,均为中等大小的近端着丝粒染色体,短臂具有随体,但因制片因素不一定出现,这三对染色体彼此区分较难。
(5)E组。16~18号染色体,中等大小。16号染色体是近中着丝粒染色体,其长臂可见次缢痕;17、18号染色体属于亚中着丝粒染色体,其中18号染色体短臂较短。
(6)F组。19、20号染色体,都是近中着丝粒染色体,较小,难以相互区分。
(7)G组。21、22号染色体和Y染色体,体积最小,均为近端着丝粒染色体。21、22号染色体短臂末端可见随体,但21号染色体稍小于22号染色体;Y染色体较21、22号染色体大,其短臂没有随体,但有时其长臂可见次缢痕。
(二)人类染色体显带核型
1.染色体显带及其命名
非显带的染色体标本由于对某些染色体的组内区分较为困难,对染色体的一些结构畸变更不能正确检出,因此其应用相当受限。20世纪60年代染色体显带技术(banding technique)开始出现,Caspersson等应用荧光染料氮芥喹吖因(quinacrine mustard,QM)处理中期染色体标本后,在荧光显微镜下观察到染色体纵轴上出现明暗相间、宽窄不一的带纹,称为Q带(Q bind),但荧光持续时间短,标本不能长期保存。随后又出现了G显带技术,将经空气干燥的染色体标本经过碱、热、胰酶或蛋白酶处理,然后经Giemsa染液染色,得到与Q带类似的带纹,即G带(G bind),由于该带在普通显微镜下就可观察,并能长期保存,所以其应用最为广泛,现已成为临床诊断染色体病的常规方法。此后又相继出现了与G带明暗相反的R带(R band)、专门显示着丝粒及其周围异染色质区域的C带(C band)、专一显示染色体端粒的T带(T band)和显示核仁组织区的N带(N band)等数种染色体显带技术。1971年在巴黎召开的第四届国际人类细胞遗传学会议,根据Q带、G带和R带,绘制了人类正常体细胞显带核型模式图(图2-8),一套单倍体的染色体带纹达到320条。
国际人类细胞遗传学会议还确定了“人类细胞遗传学命名的国际体制”(An International System of Human Cytogenetic Nomenclature,ISCN),按照该体制,染色体上明显而恒定的结构区域如着丝粒、末端和某些特殊的带,称为界标(landmark);界标之间的区域称为区(region);区内分为若干深浅不一的带(band)。需要注意的是,各区带的编号均从着丝粒朝染色体臂的末端方向依序进行。作为界标的带属于该界标远侧端的第1带;被着丝粒一分为二的带,则可看成两个带,分别属于长、短臂的1区1带。所以,描述一染色体特定带纹时需依次记录染色体号、臂符号、区号、带号,并且书写时不用任何间隔或标点。例如,1号染色体短臂1区2带可表示成1p12(图2-9)。
2.染色体高分辨显带及其命名
1975年,Yunis等建立起人类高分辨显带(high resolution banding)技术。通过观察用早中期、晚前期或更早期的细胞制备的染色体高分辨显带标本可发现,其带纹数量可达到550条、850条或更多,因而更易发现一些常规显带所不能反映的染色体更微细的畸变,在临床染色体检查、肿瘤染色体研究和基因定位中意义重大。高分辨显带是在原来常规基础上再分出亚带、次亚带,因而其描述的方法就是在原带号后加上小数点、亚带号、次亚带号。例如,1号染色体长臂4区3带第1亚带第2次亚带可记录为1q43.12。
三、人类细胞遗传学研究进展
20世纪80年代,出现了荧光原位杂交(fluorescence in situ hybridization,FISH)、染色体特定区带的显微切割和微克隆(microclone)技术,将细胞遗传学与分子生物学有机地结合起来,从而产生了分子细胞遗传学(molecular cytogenetics)。
常规的染色体分析方法,即使是高分辨显带技术,主要对中期染色体的研究有较大意义,对间期细胞核和极其微小的染色体异常的研究则相当困难。FISH技术在20世纪80年代中后期建立,该技术根据核酸探针杂交原理,应用荧光物质标记的单链DNA探针,与染色体标本上的其同源互补序列杂交,利用荧光技术可在核中或染色体上显示特定DNA序列的位置。FISH技术具有快速、安全、方便、特异性强、可多重染色、分辨率和灵敏度高等优点。通过FISH技术,能更准确地认识遗传物质的结构及其细微变化,为各种基因相关疾病的分型、预前和预后提供准确的依据,在临床肿瘤学和产前诊断方面应用广泛。近年来FISH已有较大发展,衍生了一系列新技术,包括原位杂交显带(in situ hybridization banding,ISHB)、比较基因组杂交(comparative genomic hybridization,CGH)、纤维荧光原位杂交(DNA fiber-FISH)、染色体涂染(chromosome painting)、反向染色体涂染等。
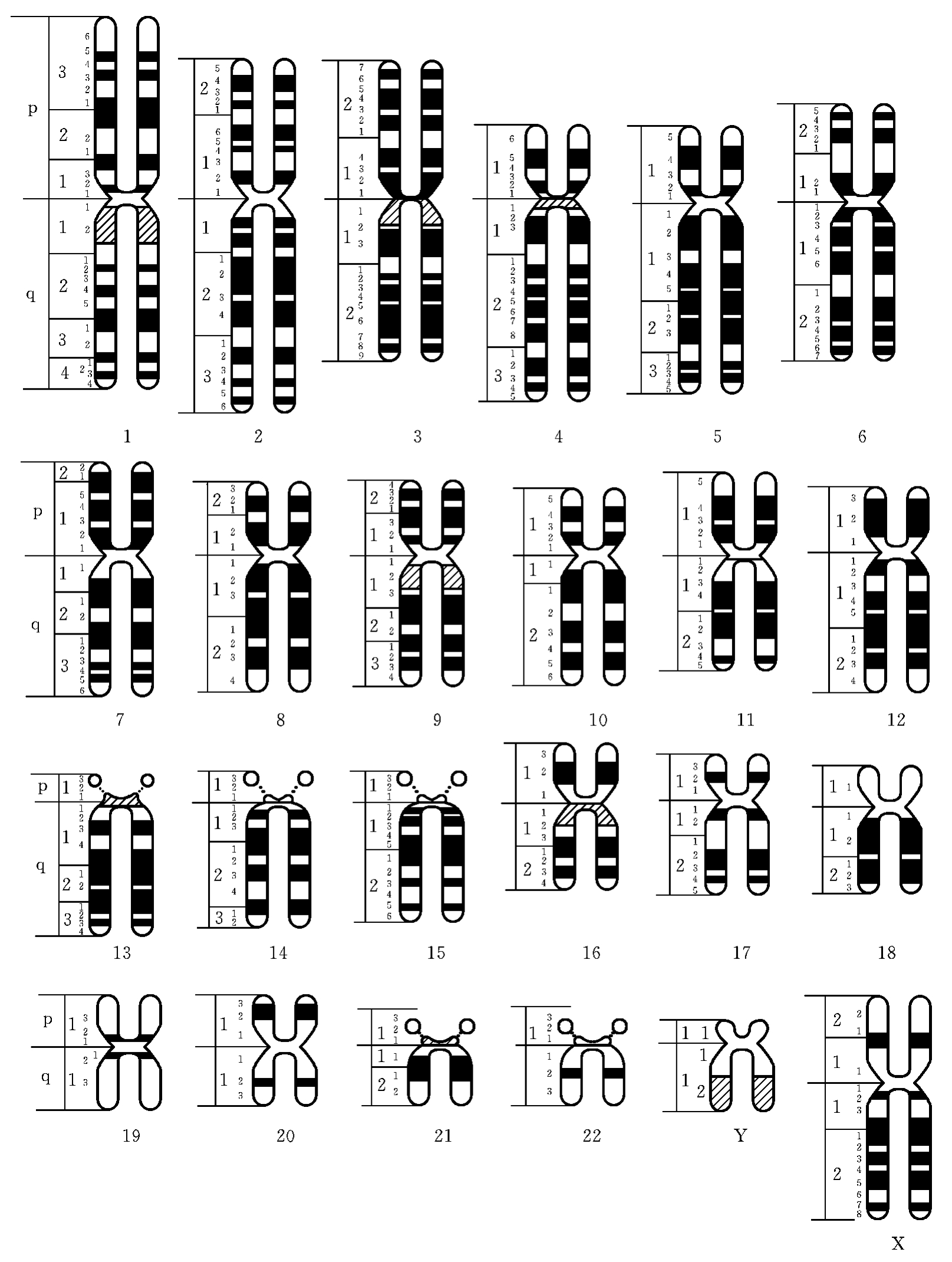
图2-8 人类显带染色体模式图
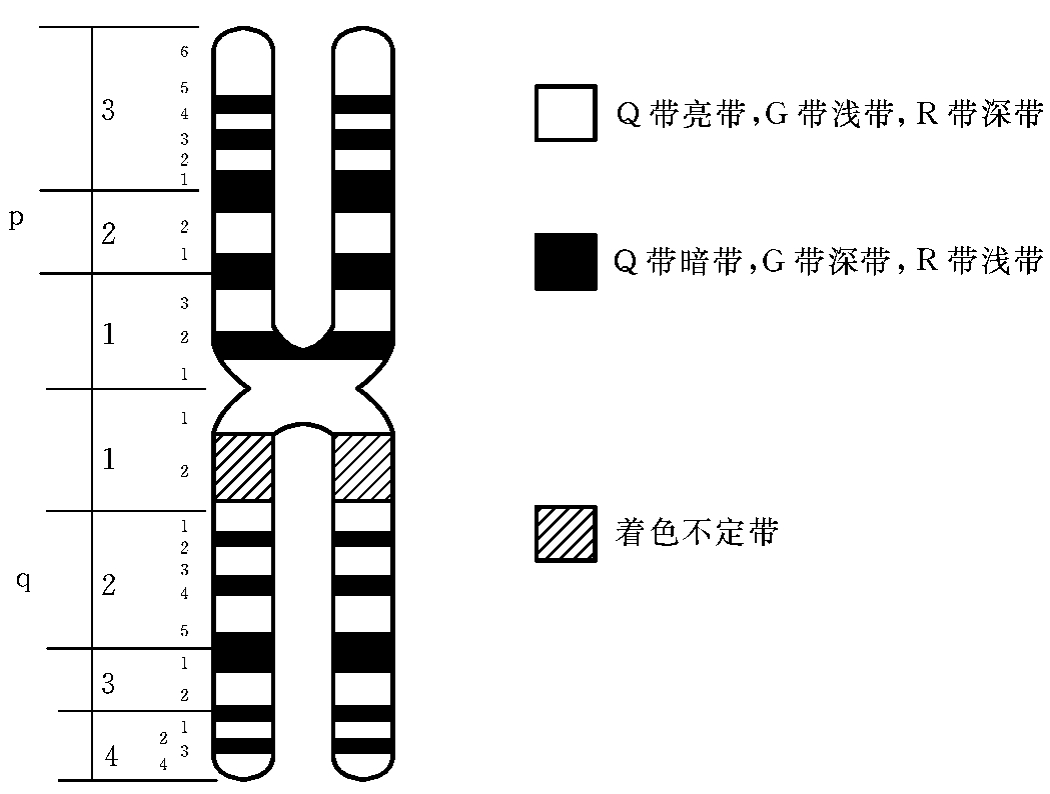
图2-9 人类显带染色体界标、区、带命名示意图
染色体显微切割和显微克隆技术首次应用于1981年Scatenghe对果蝇多线X染色体特定区域的研究,1989年开始应用于人类染色体研究。该技术可以从染色体标本的特定区域切取所需的染色体片段,结合PCR、分子克隆和FISH等分子生物学方法,构建特定染色体或染色体区域DNA文库。与基因组DNA文库相比,从该DNA文库中筛选某一特定基因更为经济和高效。此外,染色体显微切割和显微克隆技术还可用于特异性探针的制备、疾病遗传学特征的分析以及有关基因的鉴定、分析、克隆和定位等领域。
分子细胞遗传学已成为细胞遗传学研究发展的主流。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















