溶解过程特点
溶解过程特点
1.盐和碱溶解性规律
含有钾、钠、硝酸根、铵根的物质都溶于水。
含Cl的化合物只有AgCl不溶于水,其他都溶于水。
含的化合物只有BaSO不溶于水,其他都溶于水。
含的化合物只有K2CO3、Na2CO3、(NH4)2CO3溶于水,其他都不溶于水。
溶于水的碱:氢氧化锂、氢氧化钾、氢氧化钙、氢氧化钠和氨水,其他碱不溶于水。
难溶性碱中,Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀,其他难溶性碱为白色[包括Fe(OH)2]。
注意:沉淀物中,AgCl和BaSO4不溶于酸,其他沉淀物能溶于酸,如Mg(OH)2、CaCO3、BaCO3、Ag2CO3等。
大部分酸及酸性氧化物能溶于水(酸性氧化物+水→酸);大部分碱性氧化物不溶于水,能溶的有:氧化钡、氧化钾、氧化钙、氧化钠(碱性氧化物+水→碱)。
2.其他溶解现象和非溶解现象
在初级化学知识中,关于溶液的形成介绍很多,可从中深刻认识到溶解过程是复杂的物理化学过程。
Fe、CaCO3不溶于水,而溶于盐酸:前者是物理性溶解,后者是化学性溶解,体现了化学性质。
少量的氧气溶于水,二氧化碳气体溶于水:前者得到很稀的溶液,后者得到的是碳酸溶液,属质变。
NaCl溶于水而难溶于酒精,I2溶于酒精而难溶于水:同种物质在不同物质中溶解度不同,不同物质在同种物质中溶解度也不同,其内因是相似相溶。
KNO3在热水中溶解多,Ca(OH)2在热水中溶解少:物质的溶解度随温度变化,大多数物质的溶解度随温度升高而增大,少数物质变化不大,极少数物质随温度升高而减小。
100mL酒精中加100mL水,所得酒精水溶液少于200mL:酒精分子与水分子相互交融,说明分子之间有间隔。
100g食盐加100mL水,得食盐水溶液少于200g:溶解达到饱和,食盐未溶解完全。
将一缺角的蓝矾晶体置于定温饱和硫酸铜溶液中,缺角补上了,但晶体质量未变:溶解与结晶每时每刻都在进行,只是溶解与结晶速度相等,表面处于动态平衡中。
NaOH、H2SO4溶于水温度升高,NH4NO3溶于水温度降低:溶解过程包括吸热扩散和放热水合,Q放<Q吸时水溶液降温,Q放=Q吸时温度不变,Q放>Q吸时温度升高。此为溶解的热现象。
CuSO4溶于水呈蓝色,KMnO4溶于水呈紫红色:溶解过程中存在形成水合分子、水合离子的过程,而一些水合离子呈现特殊的颜色,如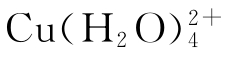 呈蓝色。此为溶解的水合问题。
呈蓝色。此为溶解的水合问题。
C12H22O11溶于水不能导电,NaCl溶于水能导电:酸、碱、盐溶于水发生离解,产生自由移动的阴阳离子,故能导电;而一些有机物不能发生离解。此为溶解的电离问题。
向动植物油脂加入纯碱、洗涤剂,如洗碗、洗衣服等:发生乳化作用,使大集团化解,化整为零各个击破。此为乳化现象。再如,牛奶置于水中,分散不均一、不稳定,形成的是乳浊液,久置后分层。
海绵、皱纹纸吸水:接纳、吸收,并未真正溶解,属渗透问题。
溶解过程是一种复杂的过程,某些过程出现丰富的表象。真正的溶解是达到了分子、原子、离子层次的分散,而不是乳化等一般意义上的分散。只有具有均一、稳定特征的分散体系才是溶液。
影响物质溶解的因素:①搅拌或振荡:搅拌或振荡可以加快物质溶解的速度;②升温:温度升高可以加快物质溶解的速度;③溶剂:选用的溶剂不同,物质的溶解性也不同。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















