第一节 煤气脱硫方法的选用
一、煤气脱硫技术分类
脱除煤气中硫化物的方法很多,按脱硫剂的状态,可分为干法和湿法两大类,见表5.1.1。
表5.1.1 煤气的脱硫与脱碳方法
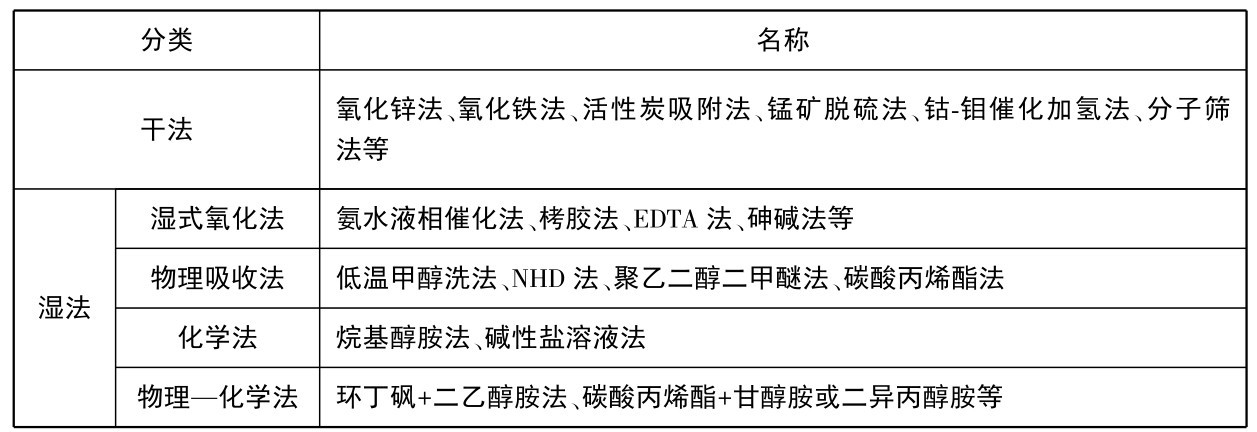
1.干法脱硫
所用的脱硫剂为固体。 当含有硫化物的煤气通过固体脱硫剂时,由于选择性吸附、化学反应的原因,使硫化物被脱硫剂截留,而煤气得到净化。
2.湿法脱硫
利用液体吸收剂选择性地吸收煤气中的硫化物,实现煤气中硫化物的脱除。 根据原理不同,湿法脱硫又可分为湿式氧化法、物理吸收法、化学吸收法和物理—化学吸收法。
(1)湿式氧化法
借助于吸收溶液中载氧体的催化作用,将吸收的H2S转化成为硫黄,从而使吸收溶液获得再生。 该法主要有改良ADA法、栲胶法、氨水催化法、PDS法及络合铁法等。
(2)物理吸收法
利用有机溶剂作为吸收剂,在吸收设备内选择性地吸收煤气中的硫化物。 吸收液进行再生还原,解析出硫化氢。 常用的方法有低温甲醇洗法、聚乙二醇二甲醚(NHD)法。
(3)化学吸收法
以弱碱性溶液为吸收剂。与H2S进行化学反应而形成有机化合物,当吸收富液温度升高、压力降低时。该化合物即分解放出H2S。烷基醇胺法、碱性盐溶液法等都是属于这类方法。
(4)物理—化学吸收法
该法的吸收液由物理溶剂和化学溶剂组成,因而其兼有物理吸收和化学反应两种性质。
二、干法脱硫技术
煤气干法脱硫技术应用较早,最早应用于煤气的干法脱硫技术是以沼铁矿为脱硫剂的氧化铁脱硫技术,之后,随着煤气脱硫活性炭的研究成功及其生产成本的相对降低,活性炭脱硫技术也开始被广泛应用。
1.氧化铁法脱硫技术
最早使用的氧化铁脱硫剂为沼铁矿和人工氧化铁,为增加其孔隙率,脱硫剂以木屑为填充料,再喷洒适量的水和少量熟石灰,反复翻晒制成,其p H值一般为8~9,该种脱硫剂脱硫效率较低,必须塔外再生,再生困难,不久便被其他脱硫剂所取代。 现在TF型脱硫剂应用较广,该种脱硫剂脱硫效率较高,并可以进行塔内再生。
氧化铁脱硫和再生反应过程如下:
(1)脱硫过程
2Fe(OH)3+3H2S →Fe2S3+6H2O
Fe(OH)3+H2S →2Fe(OH)2+S+2H2O
Fe(OH)2+H2S →Fe S+2H2O
(2)再生过程
2Fe2S3+3O2+6H2O →4Fe(OH)3+6S
4Fe S+3O2+6H2O →4Fe(OH)3+4S
氧化铁脱硫剂再生是一个放热过程,如果再生过快,放热剧烈,脱硫剂容易起火燃烧,这种火灾现象曾在多个企业发生。
干法脱硫是在圆柱状脱硫塔内装填一定高度的脱硫剂,煤气自下而上通过脱硫剂,H2S被去除,实现脱硫过程,常用的脱硫剂为氧化铁,其粒状为圆柱状,氧化铁脱硫的原理如下:
Fe2O3·H2O+3H2S →Fe2S3·H2O+3H2O
由上面的反应方程式可以看出,Fe2O3吸收H2S变成Fe2S3,随着煤气的不断产生,氧化铁吸收H2S,当吸收H2S达到一定的量,H2S的去除率将大大降低,直至失效。Fe2S3是可以还原再生的,与O2和H2O发生化学反应可还原为Fe2O3,原理如下:
2Fe2S3·H2O+3O2→2Fe2O3·H2O+6S
综合以上两反应式,煤气脱硫反应式如下:

由以上化学反应方程式可以看出,Fe2O3吸收H2S变成Fe2S3,Fe2S3要还原成Fe2O3,需要O2和H2O,通过空压机在脱硫塔之前向煤气中投加空气即可满足脱硫剂还原对O2的要求。
2.活性炭法脱硫技术
活性炭脱硫主要是利用活性炭的催化和吸附作用,活性炭的催化活性很强,煤气中的H2S在活性炭的催化作用下,与煤气中少量的O2发生氧化反应,反应生成的单质S吸附于活性炭表面。 当活性炭脱硫剂吸附达到饱和时,脱硫效率明显下降,必须进行再生。 活性炭的再生根据所吸附的物质而定,S在常压下,190℃时开始熔化,440℃左右便升华变为气态,所以,一般利用450~500℃的过热蒸汽对活性炭脱硫剂进行再生,当脱硫剂温度提高到一定程度时,单质硫便从活性炭中析出,析出的硫流入硫回收池,水冷后形成固态硫。
活性炭脱硫的脱硫反应过程如下:
2H2S+O2→S+2H2O
3.氧化锌法脱硫技术
化锌脱硫剂可直接脱除硫化氢和硫醇,反应式为:
Zn O+H2S →Zn S+H2O
Zn O+C2H5SH →Zn S+C2H4+H2O
对于硫氧化碳和二硫化碳等有机硫,则部分先转化为硫化氢,然后再被氧化锌吸收;部分有机硫可直接被氧化锌吸收,反应过程为:
CS2+4H2→CH4+2H2S
COS+H2→CO+H2S
Zn O+COS →Zn S+CO2
Zn O+CS2→2Zn S+CO2
氧化锌脱硫剂对噻吩的转化能力很弱,又不能直接吸收,因此单独使用氧化锌脱硫剂是不能把有机硫完全脱除的。 氧化锌脱硫的化学反应速率很快,硫化物从脱硫剂外表面通过毛细也到达其内表面,内扩散速度较慢,无疑是脱硫过程的控制步骤。 因此氧化锌脱硫剂粒度小,孔隙率大,有利于脱硫反应的进行。 同样压力高也有利于提高脱硫反应速度和脱硫剂利用率。
氧化锌脱硫剂是以氧化锌为主体,约占95%,并添加少量氧化锰、氧化铜或氧化镁为助剂。 根据脱硫温度的不同,可分高温脱硫氧化锌脱硫剂和常温脱硫氧化锌脱硫剂。
三、湿法脱硫技术
1.湿式氧化法
湿式氧化法脱硫技术是国内化工行业广泛使用的脱硫方法之一,顾名思义它是用稀碱液吸收气相中的H2S,在吸收H2S的液相中由于氧化催化剂的作用,将H2S氧化为元素硫并分离回收。因此该技术包括H2S吸收、氧化和硫回收。和其他的化学和物理方法相比:
(1)该法适用原料气中H2S含量低(小于20g/m3),CO2含量较高工况,即适用于煤气和焦炉气等的脱硫。 国内目前已有几百套生产装置在运行。
(2)本技术的特点是可将H2S直接氧化为单质硫,不需要专门设置克劳斯硫回收装置,流程短,操作简便。
(3)该技术总的硫回收率在80%~85%,高于其他配套克劳斯硫回收的方法。
(4)溶液的硫容量低和副产少量盐是该技术的弊病。 硫容量低使脱硫成本上升,少量副盐使碱的耗量上升,增加了操作的复杂性。
20世纪70、80年代是我国化肥工业蓬勃发展时期,也是国内湿式氧化法脱硫技术快速工业化的年代,近千套的小合成氨厂是方便开发新技术的生产试验基地,那时除对传统的ADA和醇胺法进行深入研究外,当时有代表性的方法有栲胶法、FD法、茶酚法和EDFA法等均在工业生产中得到了应用。 经过近30年的发展,伴随市场经济和环保法规的建立,到目前为止,优胜劣汰,现存的有明显技术特色,市场占有率高的典型代表有络合催化和酚醌催化两大类。 随着时间的迁移,占据市场主导地位的方法,20世纪80年代是改良ADA和氨水液相法,80年代末至90年代为栲胶法和PDS,最近几年,888异军突起,市场占据率顿然上升。
以往湿式氧化法脱硫技术主要运用于煤气粗脱硫,近几年来,其运用范围不断扩展,目前已推广到变换气和焦炉气脱硫、尿素生产中CO2、低温甲醇洗尾气、变压吸附脱碳尾气等高浓度CO2气体的脱硫。
湿式氧化法实质上就是一种伴有氧化反应的湿式酸碱中和的过程,通过催化氧化,使负二价的硫转化成单质硫分离出去。 其反应原理如下:
第一步用氨水或纯碱液吸收气体中的H2S进行中和反应。
气相中H2S被溶液吸收而转入液相中,
H2S+H2O——H2S·H2O →HS-+H++H2O ①
在液相中离子反应
HS-1+H++2Na+CO2-3→Na HS+Na HCO3 ②
综合①和②则为
H2S+Na2CO3 →Na HS+Na HCO3 ③
第二步采用载氧体催化剂进行催化氧化反应把HS-、S-2氧化成单质硫。
液相中的氧化催化反应
Na HS+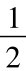 O2→Na OH+S↓ ④
O2→Na OH+S↓ ④
第三步加入或喷射自吸空气氧化失活的催化剂,使其得到再生,恢复活性、循环使用。同时将单质硫浮选出来分离出去,熔炼硫黄。
Na HCO3+Na OH →Na2CO3+H2O ⑤
从工艺上看,第一步吸收反应肯定在脱硫塔中进行。 气液两相逆流接触,通过传质(填料)H2S从气相介面向液相介面转移,进入液相主体。酸碱中和反应,生成相应的盐转化为富液。 此过程中受气膜控制属扩散式吸收。 然而催化、氧化、析硫的第二步化学反应,也主要在脱硫塔内进行。 因而,也形成了这种复杂相系共存格局。 故此,传质面积、喷淋密度、液气比、碱度、p H值、催化剂浓度、反应温度等都会影响吸收的选择性及析硫再生和气体净化度。
催化剂在整个过程中的变化示意为下:
载氧体(氧化态)+H2S →载氧体(还原态)+S↓
载氧体(还原态)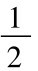 O2(空气)→载氧体(氧化态)+H2O
O2(空气)→载氧体(氧化态)+H2O
载氧体即催化剂,氧化态的载氧体将溶液中被吸收的H2S氧化成单质硫,同时自己变成还原态的载氧体。 再生时还原态的载氧体被空气中的氧转换为氧化态的载氧体,这样周而复始地循环变化,达到脱除气相中H2S的目标。溶液中生成的单质硫以硫泡沫的形式,再生时溢出再生槽后送硫回收,加工为成品硫黄后外售。
2.化学吸收法
化学吸收法主要包括醇胺法(对不同天然气组成有广泛的适应性)、热钾碱法(主要用于合成气脱除CO2)。
烷基醇胺是一类弱碱性有机化合物,其水溶液具有吸收H2S和CO2的能力。醇胺法包括一乙醇胺法(MEA)、二乙醇胺法(DEA)、二异丙醇胺法(ADIP)以及具有选择性吸收的改良甲基二乙醇胺法(MDEA)。
一乙醇胺(MEA)在各种烷基醇胺中是碱性最强的,它与H2S等酸性气体的反应速度最快,吸收能力最大,且一乙醇胺稳定性好,热降解少,价格低廉易回收。 一乙醇胺的缺点是与有机硫化物COS和CS2会形成降解产物,它的饱和蒸汽压比其他胺类高,气化损失大。
二乙醇胺(DEA)既可脱除H2S,又可脱除CO2,也没有选择性。与MEA不同,DEA可用于原料气中含有COS的场合。 虽然DEA的分子量较高,但由于它能适应两倍以上MEA的负荷,因而它的应用仍然经济。 DEA溶液再生之后一般具有较MEA溶液低得多的残余酸气浓度。
二异丙醇胺(ADIP)属于仲胺,它吸收H2S和CO2的化学反应与其他烷基醇胺相同。不同的是,二异丙醇胺在吸收过程中,能与COS、CS2生成可再生的化合物,因而用于处理含COS和CS2的酸性气体时,该吸收溶液的降解损失小。二异丙醇胺的缺点是吸收H2S的速度比较慢,当气体中有O2、HCN存在时,会引起二异丙醇胺的降解损失。
甲基二乙醇胺是一种叔胺,与其他烷基醇胺法相比,它对H2S的吸收具有较高的选择性,MDEA不易降解、腐蚀性小,特别适用于从高浓度的酸性气体中选择性吸收H2S。但MDEA工艺对有机硫的脱除效率低。
活化热钾碱法工艺是在热碳酸钾溶液中添加一定量的活化剂加快碳酸钾与CO2的反应速度;并降低液面上方CO2平衡分压,从而提高CO2的吸收速度和气体净化度。该工艺主要用于脱碳,同时能脱除硫化氢、有机硫化物。
3.物理吸收法
物理吸收法是利用有机溶剂在一定压力下进行物理吸收脱硫,然后减压而释放出硫化物气体,溶剂得以再生。 物理溶剂法主要有低温甲醇法(Rectisol)和聚乙二醇二甲醚法(NHD),此外还有碳酸丙烯酯法(Fluar)和N-甲基吡啶烷酮法(Purisol)等。 物理吸收法能耗低、吸收重烃、净化度高,需特殊再生措施,主要用于脱碳。
其中,低温甲醇法将在后面的章节中做详细介绍。 下面对聚乙二醇二甲醚法(NHD)作简要介绍。
20世纪60年代美国联合化学公司(Allies Chemical Corp)开发的一种酸性气体物理吸收溶剂—NHD脱碳液,其化学名称为聚乙二醇二甲醚,商品名为Selexol。 我国南化(集团)公司研究院和杭州化工研究所于20世纪80年代从脱碳液筛选开始着手研究,找出了用于脱硫、脱碳的聚乙二醇二甲醚最佳脱碳液组成(命名为NHD)。 可以与国外开发的先进净化工艺Selexol法相抗衡,填补了国内空白。 其物化性质与Selexol相似,但其组分含量与分子量都不同。聚乙二醇二甲醚结构式为CH3O—(CH2CH2O)n—CH3,聚合度n不同,物性不同,n<10时,为五色或淡黄色透明液体,随着n的不断增大,其黏度逐渐增大,直至为白色或土灰色固体。式中n=3~8,是一种浅黄色或无色透明液体,接近中性,无味、无毒、无腐蚀性,化学和热稳定性较好,使用时不起泡,不污染环境。
NHD溶剂对气体中硫化物和二氧化碳具有较大的溶解能力,尤其是对硫化氢有良好的选择吸收性,蒸汽压低,运转时溶剂耗损少,是一种较理想的物理吸收剂,适合于以煤(油)为原料、酸气分压较高的合成气等的气体净化,脱硫时需消耗少量热量,脱碳时需消耗少量冷量,属低能耗的净化方法。
4.物理-化学法
这是一种将化学吸收剂与物理吸收剂联合应用的脱硫方法,目前以环丁砜法最为常用。环丁砜法是用烷基醇胺和环丁砜的混合水溶液作为吸收剂,因此,兼有物理溶剂法和胺法的优点,其溶剂特性来自环丁砜,而化学特性来自二异丙醇胺和水。 在酸性气体分压高的条件下,物理吸收剂环丁砜容许很高的酸性气体负荷,而化学溶剂DIPA可使处理过的气体中残余酸气浓度减小到最低。 所以环丁砜法明显超过常用的乙醇胺溶液的能力,特别在高压和酸性组分浓度高时处理气流是有效的。 环丁砜脱硫法所用溶剂一般是由DIPA、环丁砜和水组成。 实验表明,溶液中环丁砜浓度高,适于脱除有机硫(COS),反之,低的环丁砜浓度则使溶液适合于脱除H2S。
四、脱硫方法的选择
1.湿法脱硫技术的选择
①原料气体中硫化氢含量中等,如硫化氢含量为2%~3%的粗天然气净化,当前应用最广泛的是烷基醇胺法。
②原料气中硫含量低,并且含有较高的二氧化碳,用直接氧化法脱硫较合适,如改良
ADA法、栲胶法、氨水液相催化法等。 这几种方法技术成熟、过程完善、各项技术经济指标较好,特别是栲胶法运行费用低。
③原料气的硫化氢、二氧化碳等酸性气体含量较高时,用物理溶剂或者物理-化学混合溶剂吸收,再生时放出的硫化氢用克劳斯法回收硫黄。 这类方法的共同特点是溶剂吸收能力强,能耗低。
2.干法脱硫技术的选择
①含有少量H2S及RSH的原料气体,单用Zn O脱除即可。
②含硫较高的原料气体,用活性炭和Zn O串联。
③如果原料气中的COS较多,应先将COS进行水解,再用Zn O或活性炭脱除。
④如果原料气中含有少量的硫醇和噻吩,可直接用分子筛脱除。
⑤对含有机硫较高的液态烃,先要经Co-Mo加氢转化,再经湿法脱硫,再用氧化锌等脱除。
五、干法脱硫与湿法脱硫技术结合应用
对于一些对煤气中的H2S比较敏感的行业,可以结合干法脱硫与湿法脱硫技术的优点,将两种脱硫方法结合起来应用,利用湿法脱硫先将煤气中的大部分H2S脱除,然后,再利用干法脱硫对煤气中的H2S进行精脱,从而,达到较高的脱硫净度。这样既利用了湿法脱硫可以在线调整的优点,又利用了干法脱硫脱硫效率高的优点,并克服了由于干法脱硫脱硫剂硫容因素造成的脱硫剂失效过快的问题。
为了保持人们优良的生存环境和提高企业最终产品质量,对煤气进行脱硫是非常有必要的,而采用何种脱硫方法值得厂家研究与探讨,我们在选择何种脱硫方法,要结合各种脱硫方法的优缺点,优化选择。
从目前国内外大中型煤气化装置所采用的脱除酸性气体的工艺来看,属于冷法的低温甲醇洗工艺和NHD工艺较常见,而且多以低温甲醇洗工艺为主。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















