实验二 沸点的测定
一、实验目的
1.了解沸点测定的意义。
2.熟悉沸点测定的操作。
二、基本原理
纯的液体受热至其饱和蒸气压与外界压力相等时就会沸腾,此时的温度就是该液态物质的沸点。在一定的压力下,每一种液态化合物都有固定的沸点。对于同一种化合物而言,在不同的压力下其沸点是不同的,但通常所说的沸点是指常压下的沸点。纯的液态有机化合物其沸程(沸点范围)为0.5℃~1℃。因此,通过沸点测定不仅可以鉴别不同的有机化合物,而且还可以协助其他方法判断有机化合物的纯度。沸点是有机化合物的物理常数之一。表3-3列出了部分标准化合物的沸点。
表3-3 标准化合物样品的沸点
沸点测定方法有常量法和微量法两种。常量法用的是蒸馏装置,其操作也与简单蒸馏相同,但此法需要较多的样品(10 mL以上)。微量法测定沸点,可采用如图3-2所示的沸点测定装置,在盛有热浴的悌勒熔点测定管中进行。
三、仪器和试剂
1.仪器
温度计(200℃) 酒精灯
毛细管 表面皿
2.试剂
四、实验步骤
1.沸点测定管的准备
外管的制作:用内径约为l cm、壁厚约为1 mm的玻璃管拉制成内径约为4 mm的细管,截取长70~80 mm的一段,封闭其一端,封口底要薄。此管作为外管。
内管的制作:内管又称起泡管,它有两种制作方法:
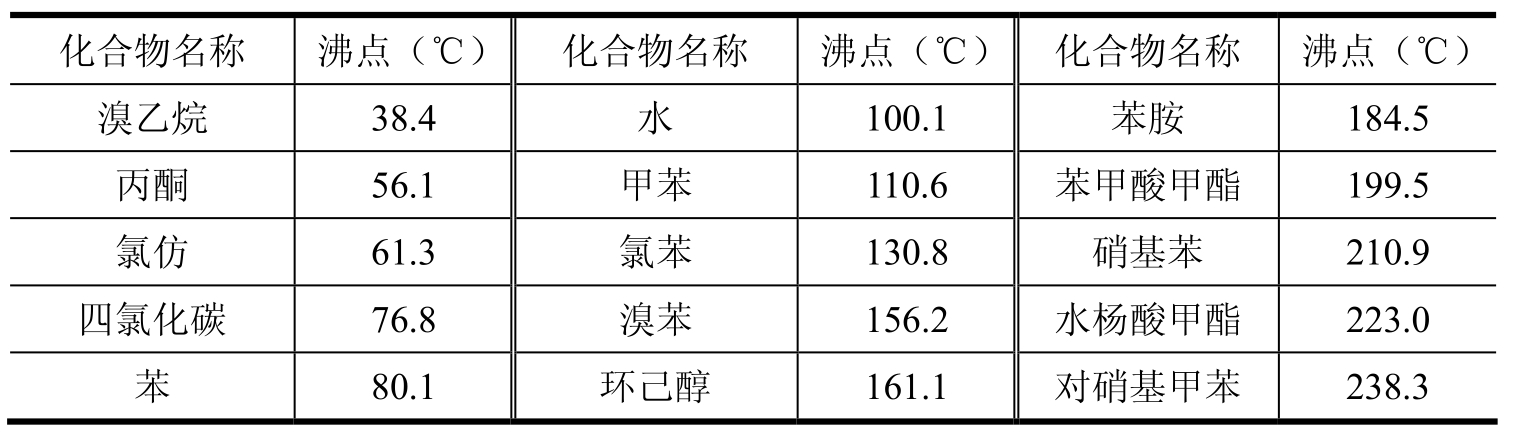
①取内径为1 mm、长80~90 mm的两管,各将其一端熔封,然后将两封口在灯焰上对接,冷却后,在离接头4~5 mm处平整地截断,作为内管。如图3-2(a)所示。
②取一内径为1 mm、长80~90 mm的毛细管封闭其一端作为内管。
2.样品的填装及仪器的装置
用细吸管置几滴液体样品于外管中,样品高度约10 mm。将内管插入外管,并使其封口对接处位于样品液面以下(如采用②法制作的内管,则将内管开口向下插入外管的样品中),然后将沸点管用橡皮圈固定于温度计的一侧,使外管中样品的位置处于温度计水银球的中部,如图3-2(b)、(c)所示。将温度计插入悌勒熔点测定管的热浴中,插入深度与测定熔点时的要求相同。
图3-2 沸点测定装置
3.沸点测定
将热浴慢慢地加热,使温度均匀上升,由于气体受热膨胀,内管中便有断断续续的小气泡冒出,当温度上升到接近样品的沸点时,气泡增多,此时应调节火焰,降低升温速度。当温度稍高于样品沸点时,便有一连串的小气泡出现,立即停止加热,使浴温自行冷却。气泡逸出的速度渐渐减慢,仔细观察并记录最后一个气泡出现而刚欲缩回内管时的温度,即为毛细管内液体的蒸气压与外界压力平衡时的温度,亦即该液体样品的沸点。可重复测定几次,要求几次测定值相差不超过1℃。
五、实验内容
1.测定丙酮、乙醇、水、环己醇的沸点。
2.教师指定1~2个未知物,测其沸点。
思考题
1.用微量法测定沸点,为什么把最后一个气泡刚欲缩回内管时的温度作为沸点?
2.测定某种液体有固定的沸点,能否认为该液体是一个纯的化合物?为什么?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















