【目的与要求】
(1)了解低沸点液体的蒸馏技术;
(2)巩固分液漏斗的使用;
(3)巩固亲核取代反应的机理。
【反应式】
1.常量合成
【所需试剂】
溴化钠15.0 g(0.15 mol);95%乙醇5 mL(7.6 g,0.17 mol);浓硫酸19 mL(34.96 g,0.357 mol)。
【操作步骤】
在100 mL圆底烧瓶中加入10 mL 95%乙醇及9 mL水[1],在不断振摇和冷却水冷却下,慢慢加入19 mL浓硫酸,冷至室温后,加入15 g研成粉末状的溴化钠,稍加振摇混合后,加入几粒沸石。安装常压蒸馏装置。在接收器中加入冰水,使接收管的末端刚好与冰水接触为宜[2]。
将混合物在电热套上加热蒸馏。先用小火加热,约20 min后,慢慢升高温度,直至无油状物流出为止[3]。
将馏出物倒入分液漏斗中,分出的有机层置于25 mL干燥的锥形瓶中[4],在冰水浴中,边振摇边滴加浓硫酸,直至锥形瓶底分出硫酸层为止[5]。用干燥的分液漏斗分出硫酸液,将溴乙烷的粗产品倒入蒸馏瓶中,用水浴加热蒸馏。用已称重干燥的锥形瓶作接收器,并将接收器外用冰水浴冷却,收集37℃~40℃馏分。产品重约11 g。
2.半微量合成
【所需试剂】
溴化钠7.70 g(0.075mol);95%乙醇5mL(3.95 g,86.0mL);浓硫酸10mL(18.40 g,0.188 mol)。
【操作步骤】
在50 mL圆底烧瓶中加入5 mL 95%乙醇及4 mL水[1],在不断振摇和冷却水冷却下,慢慢加入10 mL浓硫酸,冷至室温后,加入7.7 g研成粉末状的溴化钠,稍加振摇混合后,加入磁子搅拌。安装成常压蒸馏装置。在接收器中加入冰水,使接收管的末端刚好与冰水接触为宜[2]。
将混合物在石棉网上加热蒸馏。先用小火加热,约20 min后,慢慢加大火焰升高温度,直至无油状物流出为止[3]。
将馏出物倒入分液漏斗中,分出的有机层置于25 mL干燥的锥形瓶中[4]。在冰水浴中,边振摇边滴加浓硫酸,直至锥形瓶底分出硫酸层为止[5]。用干燥的分液漏斗分出硫酸液,将溴乙烷的粗产品倒入蒸馏瓶中,用水浴加热蒸馏。用已称重干燥的锥形瓶作接收器,并将接收器外用冰水浴冷却,收集37℃~40℃馏分。产品重约5 g。
【注释】
[1]加入水是为了防止反应进行时产生大量泡沫,减少副产物乙醚的生成,避免氢溴酸的挥发。
[2]由于溴乙烷的沸点较低,为使冷凝充分,必须选用冷凝效果好的冷凝管,各个接头处要严密不漏气。为了减少其挥发,常在接收器内预盛冷水,并使接液管的末端刚好浸入冷水中。(因为溴乙烷在水中的溶解度很小,低温时也不与水作用。)
[3]结束蒸馏时,注意在移去热源前,先将接收器与接液管离开,以防倒吸。
[4]尽量除去水分,否则加浓硫酸时,产生大量的热使产物挥发。
[5]加入硫酸,可以除去乙醚、乙醇、水等杂质。为防止产物挥发,应在冷却下操作。
【思考题】
(1)本实验都有哪些副产物存在?是如何除去的?
(2)为了减少产品的挥发,本实验采取了哪些措施?
【产物谱图】
溴乙烷的红外谱图如图4-3所示,溴乙烷的1H-NMR谱图如图4-4所示。
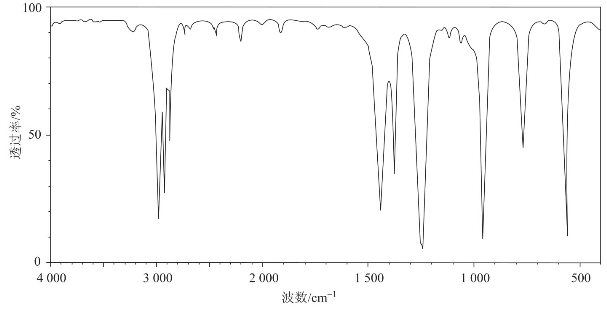
图4-3 溴乙烷的红外谱图
图4-4 溴乙烷的1H-NMR谱图
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















