【摘要】:在一瞬间,因体积扩大造成二氧化氮浓度降低,至使颜色变浅。约一、两秒钟后,颜色又变深,最后A、C两瓶中二氧化氮的颜色与B瓶的颜色无有多大差别,表明A瓶中二氧化氮的浓度又与原来的浓度相近,这就说明了反应:2NO2N2O4随着压强的减小,平衡向左发生了移动,至使二氧化氮增多。可以看到B、D瓶瓶的颜色要比A、C瓶浅得多,说明了B、D中的二氧化氮减少了。由此可知反应:2NO2N2O4随着压强的增大,平衡向右发生了移动。
压强对化学平衡影响实验的改进
①将两个150ml连通的充有二氧化氮气体的圆底烧瓶(A、B)固定在铁架台上(如图1),叫学生观察。
连通的目的是为了使学生看到两个烧瓶中的二氧化氮处于相同的条件下,且浓度相同。
②拆去A、B两个烧瓶之间的连通管,将导气管口夹好,勿使烧瓶中二氧化氮外逸。
③在一个250ml的圆底烧瓶(C)中放入5ml四氯化碳,在酒精灯上加热,待烧瓶中的空气被赶尽后,迅速与A瓶连接好(如图2)。当C瓶冷至室温时,四氯化碳又变为液体,烧瓶C中形成真空,打开A瓶导气管的夹子,可以看到二氧化氮迅速从A瓶扩散到C瓶中。在一瞬间,因体积扩大造成二氧化氮浓度降低,至使颜色变浅。约一、两秒钟后,颜色又变深,最后A、C两瓶中二氧化氮的颜色与B瓶的颜色无有多大差别,表明A瓶中二氧化氮的浓度又与原来的浓度相近,这就说明了反应:2NO2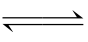 N2O4随着压强的减小,平衡向左发生了移动,至使二氧化氮增多。
N2O4随着压强的减小,平衡向左发生了移动,至使二氧化氮增多。

图1

图2
④再取一个250ml的圆底烧瓶(D),放入5ml四氯化碳,按着3的做法与B瓶连接好,当B、D瓶的颜色与A、C瓶的颜色相同时,打开D瓶排气导管的水止夹,待空气压入后,(压强亦随之增大),再夹好。(此过程二氧化氮不会外逸)可以看到B、D瓶瓶的颜色要比A、C瓶浅得多,说明了B、D中的二氧化氮减少了。由此可知反应:2NO2 N2O4随着压强的增大,平衡向右发生了移动。
N2O4随着压强的增大,平衡向右发生了移动。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















