实验86 磷系列化合物的制备
实验提要
1.NaH2PO4·2H2O的性质与制备
NaH2PO4·2H2O为无色斜方晶系晶体,极易溶于水,难溶于醇、醚。在潮湿的空气中易潮解而结块,在水中的溶解度见表5-6。由此表可知,在温度低于40℃条件下,由饱和溶液中结晶才能得到NaH2PO4·2H2O。NaH2PO4·2H2O加热可失去结晶水,加热至225~250℃脱水生成酸式焦磷酸钠(Na2H2P2O7),350~400℃脱水生成(NaPO3)6。磷酸二氢钠在工业上有广泛的应用,如锅炉水处理、电镀、制革、染料助剂及医药、云母片砌合等,还是制备六偏磷酸钠和缩聚磷酸钠的原料。
表5-6 磷酸二氢钠在水中的溶解度[g·(100g H2O)-1]
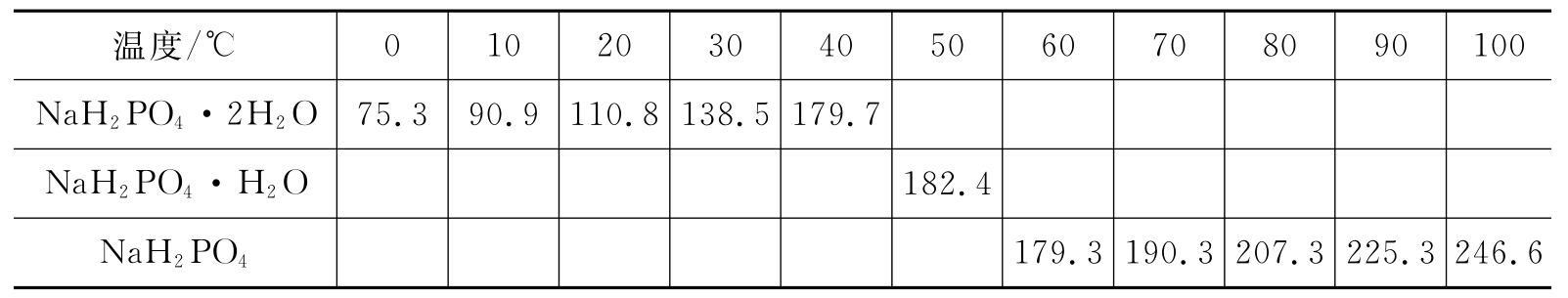
控制适当的pH值,由H3PO4与Na2CO3(或NaOH)反应,可以制得NaH2PO4·2H2O,也可以由Na2HPO4与H3PO4反应而制得。
![]()
2.Na2HPO4·12H2O的性质与制备
Na2HPO4·12H2O为无色透明单斜晶系菱形晶体,在空气中易风化,易溶于水,难溶于乙醇。磷酸氢二钠在水中的溶解度见表5-7。由此表可知,当温度低于30℃时,可得到Na2HPO4·12H2O结晶。100℃以上失去结晶水成为无水物,250℃时脱水生成焦磷酸钠。该化合物广泛用于锅炉软水剂、鞣革、木材、纸张的防火剂、釉药、焊药、油漆颜料以及医药、食品等行业,也是制取焦磷酸钠及其他磷酸盐的原料。
表5-7 磷酸氢二钠在水中的溶解度[g·(100g H2O)-1]
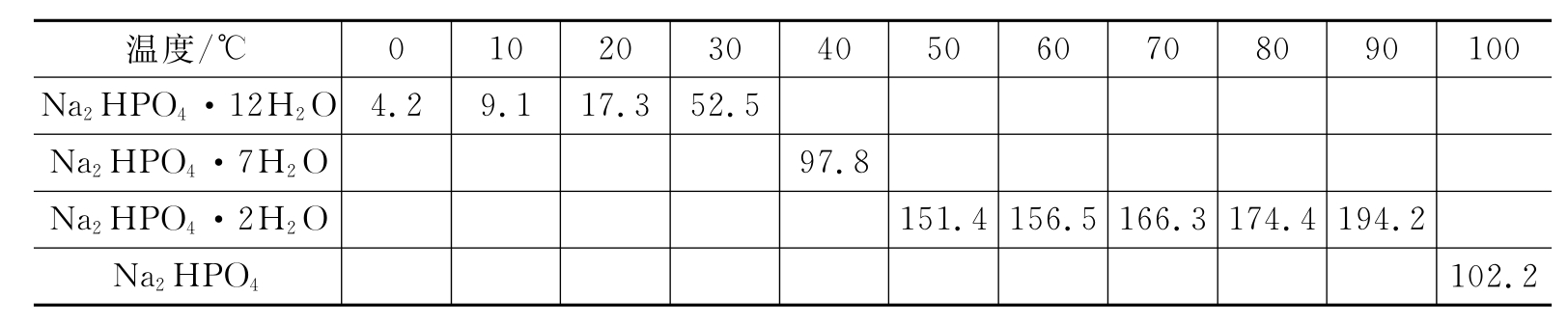
Na2HPO4·12H2O可由H3PO4与Na2CO3(或NaOH)反应,控制适当的pH值而得。
![]()
3.(NaPO3)6 的性质与制备
(NaPO3)6为无色透明玻璃状或白色粒状晶体,有较强的吸湿性,易溶于水(溶解速度慢),难溶于有机溶剂。在温水、酸或碱溶液中易水解形成正磷酸盐。与一些重金属或碱土金属离子作用生成沉淀,若(NaPO3)6过量可形成配合物而溶解。其制备方法一般是以NaH2PO4·2H2O为原料,经过脱水、灼烧,然后急剧冷却而制得。
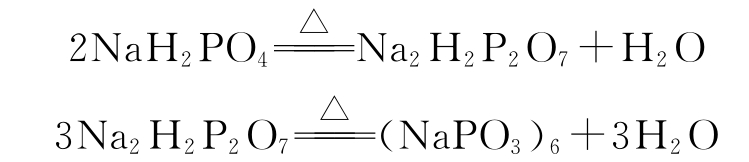
4.Na4P2O7·10H2O的性质与制备
Na4P2O7·10H2O为无色单斜晶系晶体,易溶于水和酸,难溶于醇和氨水。焦磷酸钠在水中的溶解度见表5-8。由此表可知,当温度低于76℃时,可得到Na4P2O7· 10H2O结晶。加热易脱水成无水物,水溶液煮沸即水解为Na2HPO4。碱土金属及铜、银等金属离子与Na4P2O7反应生成沉淀,加入过量Na4P2O7可使其形成配合物而溶解。Na4P2O7与Ag+生成Ag4P2O7白色沉淀,而磷酸盐与Ag+反应生成Ag3PO4黄色沉淀,常以此鉴定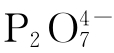 和
和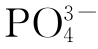 。
。
表5-8 焦磷酸钠在水中的溶解度[g·(100g H2O)-1]
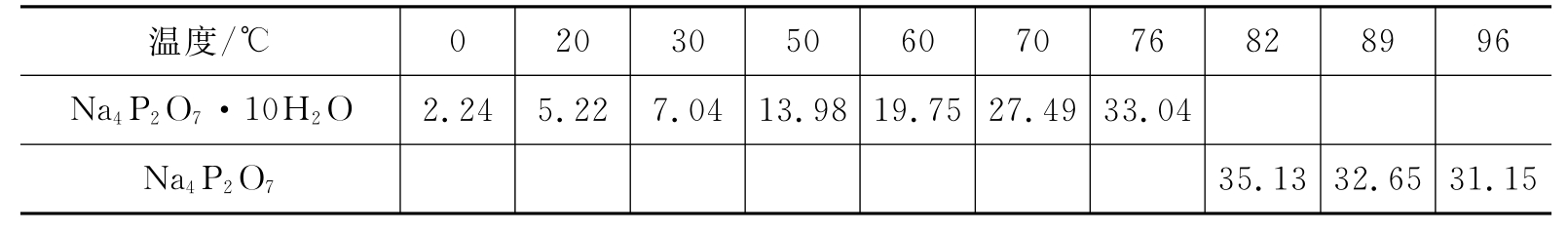
Na4P2O7一般采用焦化法进行制备。将磷酸氢二钠熔融、脱水、缩合,可制得无水焦磷酸钠,再将其溶于水,在适当条件下结晶而制得。
![]()
实验要求
每个学生任选一组题目,进行实验方案的设计与磷系列化合物的制备。
(1)以工业磷酸(1∶20)和碳酸钠(s)为原料设计合理的制备方案,制备4.0g NaH2PO4·2H2O(理论量),再以此为原料制备(NaPO3)6。
(2)以工业磷酸(1∶20)和碳酸钠(s)为原料设计合理的制备方案,制备3.0g Na2HPO4·12H2O(理论量),再以此为原料制备Na4P2O7·10H2O。
实验方案应包括实验步骤,计算主要原料的用量,最佳实验条件(温度、浓度、pH值等条件),以及所选择的实验仪器等,并用流程图简单地表示。
制得产物后,要求观察晶形并做性质检验:用低倍显微镜观察Na2HPO4·12H2O、 Na4P2O7·10H2O或NaH2PO4·2H2O晶体的晶型。试验焦磷酸盐与金属离子(如Cu2+、Cd2+)形成配合物的性质,并与Na2HPO4溶液进行比较。
思考题
(1)制备NaH2PO4·2H2O和Na2HPO4·12H2O时,结晶开始析出的温度应分别控制在什么温度以下?为什么?
(2)制备Na4P2O7和(NaPO3)6时,怎样检验缩合反应是否完全?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。













