范霍夫的推理——立体苯模型
凯库勒的原子价、四价碳、碳与碳相连成链以及苯的环状平面结构等学说,经俄国化学家布特列洛夫(1828~1886)等人归纳、总结,形成了有机分子的平面结构理论。但这一理论只是从平面结构上研究有机分子内原子的排列顺序。他们所绘出的有机结构式与现在中学课本中的平面结构式很相似。随着实验资料和数据的积累,很需要就有机分子中原子在三维空间的排布进行研究。首先提出有机分子中原子排布的立体结构理论的,是凯库勒的学生范霍夫(1852~1911,见图5-8)及其同学勒贝尔(1847~1930)。

图5-8 范霍夫(右)与美国化学会创始人之一克拉克(左)
1872年,范霍夫在莱顿大学数学系毕业后,为了在化学上得到深造,他先到波恩拜已经成名的有机化学家凯库勒为师,得到有机分子结构等化学知识的良好训练。次年凯库勒推荐他去巴黎医学院的武慈实验室,在著名化学家武兹指导下,范霍夫与法国同窗好友勒贝尔二人深得教益,后来他们双双成为新的有机立体化学的创立者。
19世纪中叶,很多人发现某些有机化合物有旋光现象。法国学者巴斯德首先发现酒石酸、葡萄酸具有左旋和右旋两种不同结构。后来,德国化学家威利森努斯(1835~1902)发现乳酸也具有旋光异构现象。在巴黎,武兹指导范霍夫和勒贝尔分别对某些有机化合物的旋光异构现象进行了广泛研究,二人于1874年分别提出了碳的正四面体构型学说。
一天,范霍夫正坐在乌德勒支大学图书馆认真阅读威利森努斯关于乳酸的一篇论文,并随手在纸上画出乳酸的化学式。当他把视线集中到分子中心的2号碳原子时,忽然联想到,如果将这个碳原子上的不同取代基都换成氢原子的话,这个乳酸分子不就变成一个甲烷分子了吗?他进一步想像:甲烷分子中氢、碳原子若排列在同一平面上,情况会怎样呢?范霍夫激动地奔出图书馆,他在大街上边走边想:让甲烷分子的4个氢原子都与碳原子排列在一个平面上是否可能呢?数学、物理知识广博的范霍夫想到,按自然界中一切都趋向于最小能量状态的原则,4个氢原子应当均匀地分布在一个碳原子周围;那么,在三维空间里甲烷分子是什么样子呢?范霍夫终于顿悟:正四面体!当然应该是正四面体,只有它才是甲烷分子最恰当的空间排列方式(见图5-9)!
范霍夫继续思考:假如用4个不同的取代基替换碳原子周围的氢原子,可能的空间排列方式只有两种。范霍夫回到图书馆,在乳酸化学式旁画出两个互成镜像的正四面体。在归纳了这些设想以后,他惊奇地发现:物质旋光特性的差异与它们的分子空间结构密切相关,这不就是物质产生旋光异构的秘密吗!
考察CHBrClF分子,两个异构体互成镜像(见图5-9),正如人的两只手,这种异物称“对映异构”,也就是旋光异构。连接4个不同原子或原子团的碳原子,称不对称碳原子或“手性碳”。
范霍夫认为,在已建立的经典有机结构理论中,人们尚不了解原子所处实际位置,原有的化学结构式不能反映某些有机化合物的立体异构现象。范霍夫于1874年发表《立体化学引论》,在这篇11页长的文章中,首次提出“不对称碳原子(手性碳)”新概念。范霍夫还用他提出的正四面体模型解释了酒石酸分子的旋光现象:酒石酸分子有两种变体——右旋酒石酸和左旋酒石酸;二者混合后,可得到光学上不活泼的外消旋酒石酸。
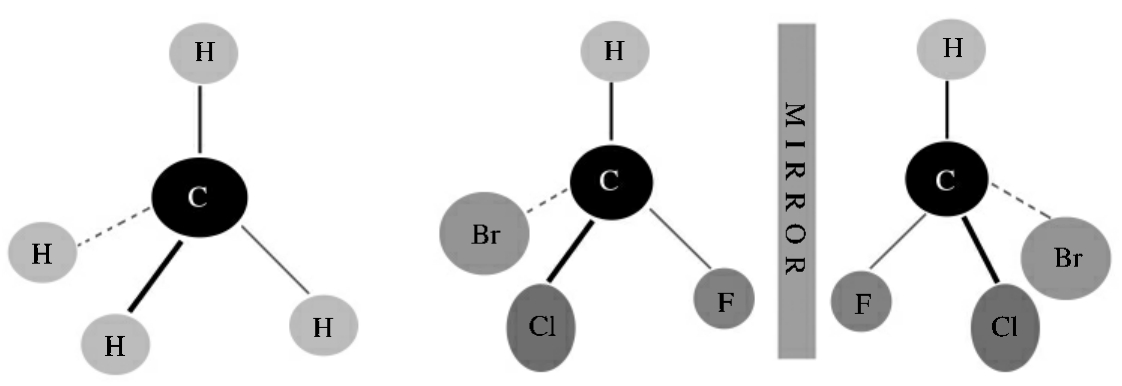
图5-9 甲烷分子的结构和CHBrClF的异构现象
分子的空间立体结构假说不仅能解释旋光异构现象,还能解释诸如二氯甲烷没有异构体的现象。平面结构理论推测二氯甲烷应该有两个异构体:一个分子中两个氯原子是相邻的关系,另一个分子中两个氯原子是相对的关系(见图5-10)。
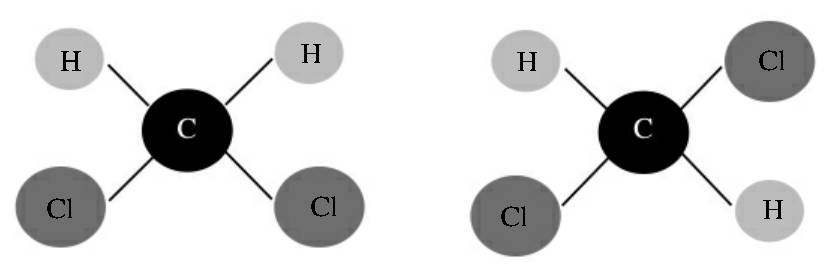
图5-10 平面结构理论认为二氯甲烷有两个异构体
但从碳的四面体理论来看,氯原子位于四面体的两个顶点上,总是相邻关系,没有相对关系,所以二氯甲烷没有异构体。
分子空间结构假说甫一诞生即在整个化学界引起广泛影响,有眼光的化学家立即看到新假说的深刻含义,称赞范霍夫的创举:“这是一个出色的假说!……它将在有机化学方面引起变革。”威利森努斯教授写信给范霍夫说:“您在理论方面的研究成果使我感到非常高兴。我在您的文章中,不仅看到了说明迄今未弄清楚的事实的极其机智的尝试,而且我也相信,这种尝试在我们这门科学中……将具有划时代的意义。”许多人都积极支持和鼓励范霍夫把自己的论文译成法文、德文等多种文字予以广泛传播。
当然也有人不了解新学说的真正含义,甚至激烈抨击范霍夫。如德国化学家、《实验化学杂志》主编柯尔贝(1818~1884)就写文章讽刺说:“有一位乌德勒支兽医学院的范霍夫博士,对精确的化学研究不感兴趣。在他的《立体化学》中宣告说,他认为最方便的是乘上他从兽医学院租来的飞马,当他勇敢地飞向化学的帕纳萨斯山的顶峰时,他发现,原子是如何自行地在宇宙空间中组合起来的。”更有人断言范霍夫假说与物理定律不相容。然而,批评文章反而推动了新理论在科学界的迅速传播,许多读过柯尔贝等人的文章的人对范霍夫的理论发生了兴趣。“一朝醒来,名声大噪”,柯尔贝等人的批评反而成就了范霍夫的名声,他不久就被阿姆斯特丹大学聘为讲师,1878年又成为化学教授。
范霍夫首创“不对称碳原子”概念,并建立了碳的正四面体构型假说(范霍夫—勒贝尔模型),尽管当时的学术界不乏微词,却无法阻挡这个假说成为立体化学诞生的标志。
1878~1896年间,范霍夫在阿姆斯特丹大学先后担任化学教授、矿物学和地质学教授,曾任化学系主任。这期间,他对化学热力学与化学亲和力、化学动力学和稀溶液的渗透压及其规律进行了深刻而广泛的探索,在这些领域建立了物理化学基础。他和奥斯特瓦尔德(1853~1932)、阿累尼乌斯(1859~1927)被后人称为创建“物理化学”的三剑客。
范霍夫在化学上的诸多开创性贡献表明他高于前人和他的同时代人,从而得到了崇高的荣誉。这与他自幼热爱化学,具有数学、物理学广博而深邃的知识素养分不开;注意哲学修养、不断探求科学方法更使他的创造想像如虎添翼,他总是站在哲学的高度去把握问题的精髓,因而常常胜人一筹。
范霍夫少年时对化学实验的浓厚兴趣,后来成为取得各项成果的基础。他重视实验,但又不像当时多数科学家那样局限于狭隘的经验。他善于巧妙运用数学方法整理实验结果,并注意用类比等逻辑推理从数学方程式推导出理论新结论,这是他创立物理化学新学科的重要方法。而在立体化学的创立过程中,则主要体现了他对模型方法以及科学假说方法的深刻理解和灵活应用。
自1885年以后,范霍夫一直都是荷兰皇家科学院成员,还先后当选为哥根廷皇家科学院、伦敦化学会、美国化学会以及德国研究院的外籍成员,获得了许多荣誉奖章。1901年他荣获第一届诺贝尔化学奖,以后的日子他依然保持朴素的生活习惯,作为化学家、农场主,仍然在每天早上驾着一辆马车为用户送奶。
当研究遇到困难时,他也曾多次出国寻求更好的研究环境。然而,高薪和优越舒适的生活条件都没能留住这位荷兰人,一旦国内有了适当的设备条件,他就毅然回国。
他勤奋终生,常废寝忘食、夜以继日地每天工作10多小时。年近花甲时,范霍夫积劳成疾,被越来越重的肺结核病困扰着。他的同行、挚友阿累尼乌斯专程来柏林探视,在被病魔折磨得不成样子的范霍夫面前,阿累尼乌斯倍感心酸与难过。这次会面是两位物理化学界巨匠的诀别,1911年3月1日,年仅59岁的范霍夫不幸早逝,震惊了世界化学界。范霍夫的骨灰被安放在柏林达莱姆公墓,供后人瞻仰。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















