常规MRI在脑肿瘤的诊断和鉴别诊断方面具有重要作用,对多数脑肿瘤可以定性诊断,但在部分肿瘤间鉴别诊断仍有困难,尤其当肿瘤表现不典型时。各种肿瘤由于血管生成不同,其PWI结果间存在一定的差异,PWI结合常规MRI有助于脑肿瘤的定性诊断和鉴别诊断。

图3-3-10 肿瘤复发
注:间变性星形细胞瘤术后1个月,手术区见不规则环形强化(A),CBV图示强化灶为低灌注,为术后改变,侧脑室旁见一明显高灌注区(↑),表明肿瘤复发
颅后窝的毛细胞型星形细胞瘤和血管母细胞瘤在常规MRI上均可表现为囊结节型,囊性部分较大,肿瘤结节强化明显,边界清楚,两者间的鉴别诊断有一定困难。血管母细胞瘤属血管源性肿瘤,病理上主要由幼稚的新生血管构成,血供极丰富,PWI为明显高灌注,其rCBV平均为9.37~15.60(图3-3-11);而毛细胞型星形细胞瘤虽然强化明显,但其新生血管并不丰富,CBV较低,rCBV平均为1.19~1.89(图3-3-12),明显低于血管母细胞瘤,且两者rCBV间无重叠,PWI可很好的区分两种肿瘤。
四脑室区的室管膜瘤和髓母细胞瘤有时鉴别困难,前者的WHO分级为Ⅱ级,血管较少,其血流灌注与灰质相似;而髓母细胞瘤则为高度恶性肿瘤,其WHO分级为Ⅳ级,血供丰富,PWI上表现为高灌注,明显高于室管膜瘤。
脑转移瘤非常常见,约占幕上肿瘤的50%。肿瘤细胞通过血液进入中枢神经系统,其新生的血管与原肿瘤有关,而与脑内原发肿瘤明显不同。转移瘤一般为多发,常位于灰白质交界区,边界清楚,有原发肿瘤病史,多不难诊断。但单发转移瘤亦很常见,占脑转移瘤的30%~50%,在无原发恶性肿瘤病史时需要同胶质瘤,尤其是高级别胶质瘤鉴别,两者在常规MRI上表现相似,有时鉴别困难。转移瘤和高级别胶质瘤肿瘤实质均为高灌注,两者rCBV间无明显差异。转移瘤呈膨胀性生长,瘤周水肿为单纯血管源性水肿,没有肿瘤细胞浸润和新生血管,PWI上呈低灌注,rCBV较低(图3-3-13),一般为0~0.5;而高级别胶质瘤瘤周水肿区内有肿瘤细胞浸润和血管生成,PWI上呈高灌注,rCBV值较高(图3-3-8),一般为1.2~2.5。瘤周水肿的PWI可有效区分转移瘤和高级别胶质瘤。瘤周水肿PWI技术的关键点是兴趣区的选取,此兴趣区为紧邻强化病灶,在T1WI上为低信号,T2WI上为高信号,增强后无强化。

图3-3-11 血管母细胞瘤
注:增强T1WI(A)示左小脑半球囊结节性病灶,结节明显强化。CBV图(B)示结节明显高灌注,远高于正常脑组织

图3-3-12 毛细胞星形细胞瘤
注:增强T1WI(A)示左小脑半球囊实性病灶,实性部分明显强化。CBV图(B)示实性部分为低灌注,与脑白质灌注相似

图3-3-13 肺癌脑转移瘤
注:T2WI(A)示肿瘤位于左额叶,呈高信号,信号不均匀,兴趣区放置于靠近肿瘤的瘤周水肿区。CBV与T2WI叠加图(B)示瘤周水肿区为低灌注,rCBV为0.39
近年来,由于免疫抑制药的应用、免疫缺陷性疾病等原因,脑原发性淋巴瘤(primary cerebral lymphoma,PCL)发病率逐渐上升,与胶质母细胞瘤之比已由过去的1∶250上升到1∶6。与胶质母细胞瘤需要手术治疗不同,PCL对放疗和化疗敏感。手术并不改善PCL的预后,相反可能导致神经功能缺损和手术所致死亡。常规MRI上淋巴瘤常为多发、明显强化,位于深部灰质或室管膜下,常累及胼胝体,有时与高级别胶质瘤,甚至脱髓鞘性病变不易鉴别。组织学上PCL包绕宿主血管生长,血管生成并不明显,因此尽管增强T1WI上强化明显,但PWI上为低灌注(图3-3-14),rCBV明显低于高级别胶质瘤,两者可得到有效区分。
胶质瘤病是种少见的脑肿瘤,其特征是中度多形性胶质细胞蔓延浸润已有的结构而并不破坏这些结构,有丝分裂、坏死和血管生成很少见。常规MRI上表现为局限性或弥漫性浸润性信号异常,增强后没有强化,诊断有时困难。PWI可发现其缺乏血管生成的特点,rCBV低于低级别胶质瘤,甚至低于正常白质。
颅内脑外肿瘤多富血供,且没有BBB,增强T1WI上明显强化。一般情况下,脑外肿瘤具有明显的特征,如蛛网膜下腔增宽、脑瘤界面等,一般易于同脑内肿瘤区分。当高级别胶质瘤位于脑表面,甚至侵犯脑膜时,或脑外肿瘤侵犯脑实质时,两者有时不易鉴别。高级别胶质瘤在PWI上为高灌注,脑膜瘤也是如此。通过修正进入组织间隙对比剂的影响,发现修正后的脑膜瘤rCBV高于高级别胶质瘤,但由于其后处理繁琐,实际工作中很少进行后处理修正。对脑膜瘤等脑外肿瘤,由于对比剂渗漏明显,rCBV被明显低估,因此肿瘤实质rCBV不能有效区分脑膜瘤和胶质瘤。脑膜瘤由于没有血脑屏障,Gd-DTPA在首过期间即迅速通过血管壁进入肿瘤组织间隙产生T2*增强效应,使首过效应曲线的上升支恢复缓慢,因此MTT明显延长(图3-3-15)。胶质瘤等脑内肿瘤即使有BBB的破坏,对比剂漏出的速率亦不及脑膜瘤快,其MTT的延长不如脑膜瘤明显(图3-3-16),因此MTT可用于脑内肿瘤与脑膜瘤间的鉴别。亦有研究者提出用首过曲线鉴别两者,脑膜瘤等脑外肿瘤表现为首过结束后无明显信号恢复,曲线远离基线,而脑内肿瘤首过结束后信号明显恢复,曲线离基线较近。这一现象可能与成像参数有关,并非总是如此。
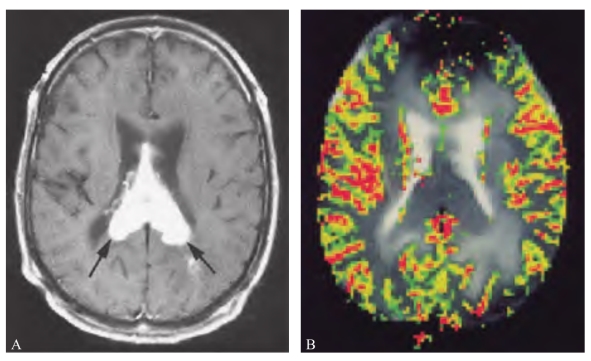
图3-3-14 脑原发性淋巴瘤(PCL)
注: 72岁男性,增强T1WI(A)示肿瘤均匀性强化,累及胼胝体压部。CBV图(B)示肿瘤低灌注,rCBV为0.89~1.10
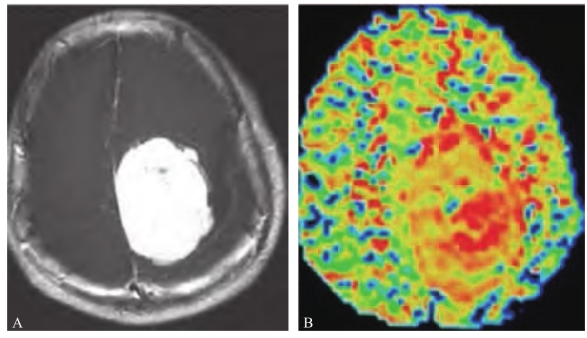
图3-3-15 大脑镰旁脑膜瘤
注:增强T1WI(A)示肿瘤均匀性强化,MTT图(B)示肿瘤MTT较正常脑组织延长
脑膜瘤和高级别胶质瘤瘤周水肿区血管生成存在差异,在脑膜瘤没有明显的新生血管,瘤周水肿区脑组织由于水肿和肿瘤的压迫,灌注减低,远离肿瘤的水肿区,由于水肿和肿瘤压迫减轻,灌注逐渐增加至接近正常脑组织;而在高级别胶质瘤则有血管生成,但随着离肿瘤边缘距离的延长,血管生成逐渐减少。PWI上表现为脑膜瘤瘤周水肿的rCBV随着与肿瘤距离增大而增大,而高级别胶质瘤表现正相反,即随着与肿瘤距离增大而减小。
富血供的脑膜瘤,术中出血多明显,既影响手术野的观察,同时给患者带来潜在的危险,常规MRI对肿瘤血供程度的判断并不可靠。根据PWI的结果选择性地对高灌注的脑膜瘤行术前栓塞,能够减少术中出血,并可用PWI观察栓塞后肿瘤血供的变化。
常规MRI上,脑肿瘤尚须与一些非肿瘤性病变鉴别,包括感染、脱髓鞘,甚至脑梗死。病毒性脑炎和弓形虫脑炎在PWI上呈明显低灌注,rCBV低于正常白质。肿瘤样脱髓鞘病变(tumefactive demyelinating lesion,TDL)在常规影像学上表现为强化的占位性病变、程度不等的灶周水肿和中心坏死,与胶质瘤不易鉴别,甚至在组织学上,TDL由于细胞密度增高、伴有有丝分裂特征的非典型性反应性胶质细胞,亦不易与胶质瘤相区分。尤其是单发TDL, 极易误诊为脑肿瘤,导致手术甚至放疗。组织病理学上,TDL的显著特点之一是病灶内仅有正常血管,而没有新生血管。PWI上TDL因此呈低灌注,明显低于高级别胶质瘤。PWI原始图像上,TDL病灶内可见到条状血管样结构,随对比剂的流入和流出信号强度相应改变,于对比剂浓度达高峰时最为明显,呈明显低信号(图3-3-17),可能为病灶包绕的正常室旁血管或其分支,这一征象未见于其他病变。

图3-3-16 右顶叶胶质母细胞瘤
注:增强T1WI(A)示肿瘤不均匀性强化,位于脑表面。MTT图(B)示肿瘤MTT与正常脑组织相同

图3-3-17 肿瘤样脱髓鞘病变(TDL)
注:轴位FLAIR(A)上右额叶病灶类似肿瘤,左侧见3个小病灶(↑),增强T1WI上(B)右额叶病灶呈不完整厚环状强化。PWI对比剂达峰值时原始图像(C)示病灶中心低信号血管样结构
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。

















