实验七 呼吸系统疾病
一、目的与要求
(1)掌握肺气肿、肺源性心脏病、大叶性肺炎、小叶性肺炎等的病理改变及临床病理联系,以及肺癌的病理分型及病变特点。
(2)熟悉支气管扩张症、硅肺的病理改变。
二、实验内容
(一)基础实验
1.复习相关的组织学知识
肺的表面被覆光滑而薄的脏层胸膜,透过胸膜可见许多呈多角形的肺小叶。正常肺为浅红色,质软,呈海绵状。成人肺的重量相当于自己体重的1/50。左肺分为上、下两叶,右肺分为上、中、下三叶。支气管从肺门到肺边缘由粗逐渐变细。气管、各级支气管、肺的组织学结构,请参阅本书实验三与实验十四。
2.大体标本观察
(1)肺气肿
肺组织膨胀,体积增大,边缘钝圆,组织柔软而失去弹性。切面肺组织呈海绵状或蜂窝状,可见肺大疱形成。此外,小支气管及细支气管腔内有炎性分泌物阻塞。肺表面及切面可见黑色斑点散在,此为炭末沉积。
(2)肺源性心脏病
心脏增大,重量增加,外观呈球形,右心室壁明显增厚(>0.5cm),右心腔明显扩张,右心室占据心尖部,心尖钝圆。右心室乳头肌、肉柱显著增粗,室上嵴增厚,肺动脉圆锥明显膨隆,各瓣膜无明显异常。
(3)支气管扩张症
肺切面见支气管(多在三级以下)呈囊状或圆柱状扩张,管壁可见部分增厚,部分变薄,支气管内膜粗糙,有横行皱襞形成,管腔内常见黄色脓性渗出物,周围肺组织有萎陷、纤维化和肺气肿形成。
(4)大叶性肺炎
病变肺叶体积增大,切面呈灰白色(灰色肝变期)或红褐色(红色肝变期)。这两期的肺组织均发生实变,肺质实如肝,外观比较干燥,切面粗糙,呈颗粒状,胸膜表面有少量纤维素性渗出物附着。
(5)小叶性肺炎
肺切面可见大小不等、形态不规则、散在的灰黄色实变灶,边界不十分清楚,病灶往往是以细支气管为中心,细支气管腔内还可见到灰黄色的脓性渗出物。个别区域的病灶互相融合成为较大的不整形病灶。
(6)硅肺
可见肺组织明显纤维化,胸膜增厚,肺组织质地变硬(标本可直立不倒),重量增加(入水下沉)。肺表面及切面均可见散在分布的灰白色、粟粒大小、分界清楚的硅结节,该结节触及有砂粒感,若硅结节相互融合可形成较大的结节,弥漫散布于全肺。
(7)肺癌
①中央型肺癌:主支气管或叶支气管的管壁上可见灰白色、粗糙不平的肿瘤组织,突入管腔,引起管腔狭窄,形成或大或小的肿块,并向周围浸润性生长,以致肺门淋巴结有癌细胞转移,造成淋巴结肿大,肿大的淋巴结与肺门肿块融合。癌组织周围的肺组织有时可见肺不张、支气管扩张及小叶性肺炎等病变。②周围型肺癌:肺周边部见孤立的、呈结节状或球形的癌结节,与支气管关系不明显,若侵犯胸膜时,可见胸膜增厚、粗糙或附有纤维素。
3.组织切片观察
(1)肺气肿
肺组织中大部分肺泡腔扩张,肺泡壁变薄或断裂,致使肺泡互相融合成较大的囊腔(图7-1)。肺泡间隔内毛细血管数量减少,肺间质纤维组织轻度增生,肺小动脉内膜纤维性增厚,小支气管和细支气管可见慢性炎症改变。
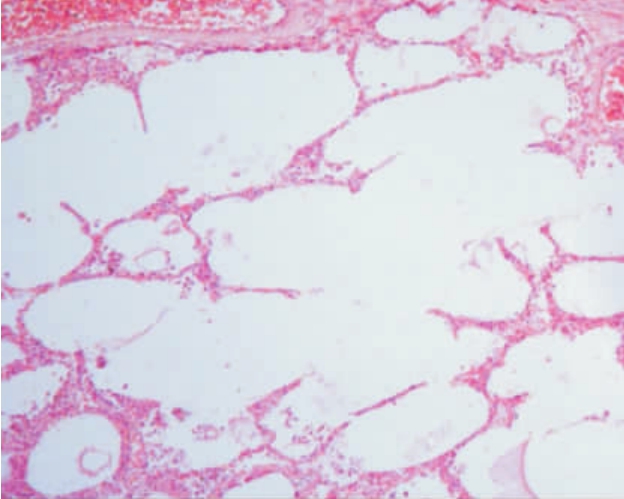
图7-1 肺气肿

图7-2 小叶性肺炎
(2)小叶性肺炎
病变呈灶状分布,病灶中心常见细支气管,细支气管腔内及其周围肺泡腔内充满炎性渗出物,其成分多为中性粒细胞,还有少量单核细胞、浆液、气泡等(图7-2)。病变区周围肺组织有代偿性肺气肿。
(3)大叶性肺炎
肺组织呈弥漫实变状态,几乎见不到空虚的肺泡。肺泡腔内充满大量中性粒细胞和纤维素,个别区域的肺泡腔内还可见到少量红细胞,此为灰色肝变期的表现(图7-3(a))。肺泡壁毛细血管由于受压而呈贫血状态。支气管周围组织水肿,血管充血,有单核细胞及中性粒细胞浸润。部分切片中可以看到胸膜上有纤维素渗出。
若肺泡壁毛细血管扩张充血,肺泡腔内见大量红细胞、少量中性粒细胞和纤维素,此为红色肝变期的表现(图7-3(b))。

图7-3 大叶性肺炎
(4)间质性肺炎
病变主要位于肺的间质,病变比较弥漫。肺泡壁明显增宽,其内血管扩张充血,肺间质水肿,可见淋巴细胞和单核细胞浸润(图7-4)。肺泡腔内一般无炎性渗出物,或仅有少量浆液。有时合并小叶性肺炎。
(5)硅肺
肺组织内见程度不同的纤维组织增生及大小不等的硅结节,硅结节由玻璃样变性的胶原纤维构成,这些胶原纤维呈同心圆状或旋涡状排列,结节内偶见内膜增厚的血管,结节周围可见纤维组织增生(图7-5)。

图7-4 间质性肺炎

图7-5 硅肺
(6)支气管扩张症
支气管壁呈不同程度的组织破坏及慢性炎症改变,支气管壁增厚,管腔扩张(图7-6)。黏膜上皮萎缩、脱落或增生,常伴有鳞状上皮化生,可有糜烂或溃疡形成。黏膜下血管充血,淋巴细胞、浆细胞浸润,管壁腺体、软骨、弹力纤维、平滑肌被破坏,萎缩甚至消失,并被炎性肉芽组织取代。病变支气管周围肺组织纤维化,淋巴组织增生。
(7)肺癌(小细胞肺癌)
癌细胞排列成片状或巢状,为弥漫分布,癌细胞体积较小,呈长圆形,大小不一致,细胞质少。细胞核多呈卵圆形或三角形,似燕麦状,细胞核深染,有较多病理性核分裂象(图7-7)。癌组织可见坏死,呈粉染无结构状。肿瘤的边缘可见少量肺组织,其肺泡腔内也可见癌组织浸润。

图7-6 支气管扩张症

图7-7 肺癌(小细胞肺癌)
4.绘图及描述
画出肺气肿、小叶性肺炎、肺癌的结构特点,并进行描述。
5.思考题
(1)大叶性肺炎、小叶性肺炎与间质性肺炎在病理变化上如何鉴别?
(2)长期慢性支气管炎可引起什么后果?
(3)有哪些肺部疾病可引起肺源性心脏病?其机制如何?
(4)肺气肿和硅肺对人体有何危害?
(二)综合型/创新型实验
1.临床病理讨论
病史摘要
患者,男,48岁。5d前因淋雨而发热、咳嗽,医生曾给予其消炎退热药,但患者没有服用,第5天夜里病情突然恶化,呼吸困难,颜面发紫,脉细弱,急送医院抢救,途中死亡。
尸检摘要
肺:体积增大,重量增加,左肺上、下两叶均发生实变,质较硬,颜色为灰白色,切面干燥,呈颗粒状。右肺下叶完全实变,上叶中、下部发生实变,上叶上部及中叶肺组织疏松,呈海绵状,质软。肺膜增厚,并与胸壁发生纤维性粘连。镜下取自实变部位的肺组织切片可见大部分肺泡腔内充满粉染的纤维素,纤维素网中可见大量中性粒细胞,红细胞较少。肺泡壁毛细血管受压呈贫血状态,但肺泡壁结构完整,未遭破坏。少数肺泡腔内见淡粉色的水肿液和红细胞,肺膜增厚,可见粉染的纤维素。取自右肺中叶的切片可见肺泡扩张,肺泡壁无断裂。
肝:在低倍镜下见肝窦及中央静脉扩张、充血,肝细胞索狭窄,在高倍镜下见肝细胞中有粉染颗粒和边界较清楚的圆形空泡。
主动脉:镜下见主动脉壁增厚,内膜粗糙不平,有较多淡黄色斑块,隆起于内膜表面,斑块表面为增生的纤维组织,并发生透明变性,下方为粉染无定形物质,其中可见针状胆固醇结晶,尚可见蓝染的钙盐沉积。斑块底部及周边可见肉芽组织和少量泡沫细胞。
讨论题
(1)请根据临床和病理资料作出病理诊断。
(2)分析患者死亡的原因。
(3)肺部病变可能引起哪些并发症?
(4)右肺中叶为何种病变?
(5)肺部病变与主动脉的病变是否有联系?
2.创新型实验
肺癌组织学分型:
(1)实验目的:使学生初步了解外科病理学肿瘤的组织分型的判定方法,熟悉免疫组织化学技术的原理、实验步骤和结果判定。
(2)实验原理:鳞状上皮、腺上皮、神经内分泌细胞均可表达相对特异性分子,结合HE染色(苏木精-伊红染色)切片、临床特征、影像学特点即可分型。
(3)实验步骤:
①观察肺癌的HE染色切片,根据肿瘤的形态特点初步分型。
②查资料,选择恰当的实验方法、适当的分子标记物进行鉴别和验证。
③实验设计。
④完成实验过程。
⑤结果分析。
(4)实验方法:免疫组织化学染色。
抗体:高分子量角蛋白、低分子量角蛋白、TTF-1、CgA(Syn、Leu7)。
免疫组织化学染色的步骤:
①切片常规脱蜡至水。
②用3%H2O2封闭10min,蒸馏水洗2min,加PBS缓冲液。
③加第一抗体于37℃保温1h,用PBS缓冲液洗3次,每次5min。
④加酶标第二抗体,置于室温下15min,用PBS缓冲液洗3次,每次5min。
⑤加入DAB(二氨基联苯胺)显色。
⑥用苏木精复染,水洗。
⑦脱水、透明、封片。
(5)实验结果:高分子量角蛋白(+),可诊断为鳞状细胞癌;低分子量角蛋白(+),可诊断为腺癌;CgA(Syn、Leu7)(+),可诊断为神经内分泌癌,结合HE染色可判定为小细胞癌、大细胞癌或类癌。
赵瑞波(哈尔滨医科大学)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















