造血干细胞是体内各种血细胞的惟一来源,是生成各种血细胞的原始细胞,又称多能干细胞,主要存在于骨髓、外周血、脐带血中,见图1-1。造血干细胞在一定的微环境和某些因素的调节下,增殖分化为各类血细胞的祖细胞,称造血祖细胞。它也是一种相当原始的具有增殖能力的细胞,但已失去多向分化能力,只能向一个或几个血细胞系定向增殖分化,产生成熟的血细胞。
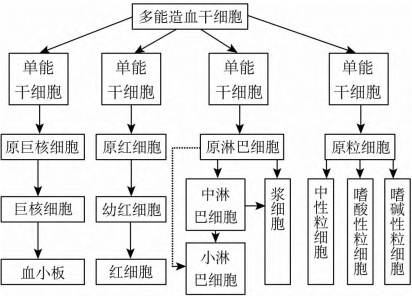
图1-1 造血干细胞的分化
(一)造血干细胞的生物学特性
1.高度的自我更新能力 造血干细胞自我更新能力维持着正常机体的全部生命过程。在正常情况下,分裂后的子细胞有半数保持自我更新能力,另一半离开干细胞池进入增殖分化池,成为早期祖细胞。这种不对称性分裂始终可维持干细胞的数量不变,故能维持正常机体长期、恒定地造血。
2.多向分化能力 一般情况下,造血干细胞大部分处于静止期,仅少数进入增殖期,在多种造血因子的调控下向各系血细胞分化。造血干细胞不仅可分化成为造血细胞,同时也可产生某些非造血细胞,如破骨细胞。
3.长期造血功能重建 体内造血干细胞在移植后能建立永久性造血重建,而长期培养起始细胞,相当于体内造血干细胞,在体外能启动长期造血。
4.造血干细胞的不均一性 造血干细胞不是单一的细胞群体,而是由不同年龄等级的干细胞组成。凡处于周期中连续不断增殖和加速增殖的造血干细胞,其自我更新能力随之减弱,而G0期的造血干细胞则具有更大的自我更新能力。
(二)血细胞的生成
已知体内所有的血细胞均来源于造血干细胞。造血干细胞在骨髓造血微环境、造血生长因子、造血抑制因子等多种因素的影响及调节下,分化为系列限制性造血祖细胞。各系祖细胞同样受骨髓微环境和造血因子的调控,增殖分化为各系成熟的血细胞,见图1-2。
1.红细胞生成 正常人红细胞的生成包括造血干细胞分化为红系祖细胞、红系前体细胞(原始红细胞至晚幼红细胞)的增殖与分化、网织红细胞的增殖与成熟以及网织红细胞向外周血释放成熟红细胞的过程。
造血干细胞分化为红系祖细胞,后者是处于造血干细胞和红系前体细胞之间的细胞群。红系祖细胞向红系前体细胞的分化是随机的同系限制性过程,是调节红细胞生成自体稳定机制中的一个关键过程。限制祖细胞只向单一红系细胞发育。这种限制可能是由于细胞表面特异性造血因子受体的表达,如红细胞生成素(EPO)受体,以及造血微环境作用的结果。红系祖细胞在EPO作用下向红系前体细胞分化、增殖,最后成为成熟的红细胞。这类细胞在高浓度的EPO条件下,当培养延续到14~16d,培养体系中会骤然生成由30 000~40 000个红系细胞组成的红系集落,称为红系爆式形成单位(BFU-E),可分化为红系集落形成单位(CFU-E)。BFU-E和CFU-E是红系祖细胞群中两类性质不同的细胞亚群,BFU-E是更接近造血干细胞的红系祖细胞。

图1-2 血细胞的生成
红系祖细胞分化到红系前体细胞阶段,则可以用形态学标准加以区分,这包括原始红细胞、早幼红细胞、中幼红细胞、晚幼红细胞、网织红细胞及成熟红细胞(彩图1)。红细胞成熟是血红蛋白增加和细胞核活性衰减的过程。随着细胞的成熟,有核红细胞中的血红蛋白含量不断增加,RNA的含量不断减少。到了晚幼红细胞则细胞核浓缩并脱出,被单核-巨噬细胞吞噬,或在脾脏内碎裂、溶解,成为无细胞核的网织红细胞。在成熟红细胞阶段不再合成血红蛋白。网织红细胞通过骨髓-血液屏障释放入血,进一步发育成熟,成为血液循环中成熟红细胞,并发挥红细胞的功能。
2.粒细胞、单核细胞的生成和分布 粒细胞和单核细胞来源于共同的祖细胞,也就是先由造血干细胞分化产生粒细胞-巨噬细胞系造血祖细胞,后者进一步分化形成粒细胞系祖细胞和单核-巨噬细胞系祖细胞。在骨髓微环境和造血因子的影响及调控下,祖细胞增殖分化形成粒细胞、单核细胞或两者混合存在的集落。在适宜的条件下体外培养形成粒细胞集落形成单位(CFU-G)、单核-巨噬细胞系集落形成单位(CFU-M)和粒细胞-巨噬细胞系集落形成单位(CFU-GM)。
经过造血干细胞、祖细胞阶段,粒细胞继续增殖分化,直至产生成熟粒细胞。此过程包括原始粒细胞、早幼粒细胞、中幼粒细胞、晚幼粒细胞、杆状核粒细胞和分叶核粒细胞,并在中幼粒阶段开始分化为中性、嗜酸性和嗜碱性粒细胞(彩图2)。粒细胞的整个生成过程可分为骨髓期和外周血期。骨髓期的细胞又分为增殖池和贮存池,增殖池包括由干(祖)细胞至中幼粒阶段的细胞,自晚幼粒阶段细胞不再分裂,骨髓中的晚幼粒、杆状核和分叶核粒细胞构成贮存池。成熟粒细胞释放入外周血构成血液粒细胞总池,其中一半细胞在血液中自由循环,称为循环池,而另一半细胞松散地黏附于毛细血管内皮上,称为边缘池,两者之间可以自由交换,维持动态平衡。当有炎症等刺激时,粒细胞可离开血液循环返回组织,但这些细胞不能再返回血液循环。
单核细胞经干细胞、祖细胞阶段,进一步增殖分化形成原始单核细胞、幼稚单核细胞,最终分化成熟为单核细胞(彩图3)。骨髓中成熟的单核细胞很快释放入血液循环。在血液循环中单核细胞的半数清除时间约为8.4h。单核细胞进入组织后,在适当刺激下发育成巨噬细胞。血液中的单核细胞和组织中的巨噬细胞形成单核-巨噬细胞系统,在机体的防御机制中发挥重要作用。
3.巨核细胞生成及血小板的产生 巨核细胞是血小板的前体细胞,巨核细胞生成是一个复杂的过程,包括造血干细胞分化形成巨核细胞系祖细胞,后者分化增殖产生巨核细胞,巨核细胞分化成熟,最终生成血小板。
造血干细胞分化形成巨核细胞系祖细胞,即能增殖产生新的巨核细胞的造血前体细胞。经过巨核细胞的增殖阶段,各级祖细胞经过分裂生长,直至形成不再具备增殖能力的巨核细胞。
失去增殖能力的巨核细胞进入成熟阶段,在形态学上从不能识别逐渐分化为可以识别的巨核细胞,后者包括原始巨核细胞、幼稚巨核细胞、颗粒巨核细胞、产板巨核细胞和裸核(彩图4)。巨核细胞的成熟过程包括细胞核的多倍体化和细胞质界膜系统的发育及细胞器的成熟。与此同时,巨核细胞胞质体积增大,细胞内颗粒逐渐增多,生成与血小板功能相关的蛋白质和酶,而界膜系统广泛形成,将胞质分割成许多小片,并形成血小板膜。最后,巨核细胞胞质碎裂脱落产生血小板,释放进入血液循环,在止血和凝血过程中发挥重要作用。
4.淋巴细胞的生成和分布 淋巴细胞(彩图5)主要包括T淋巴细胞和B淋巴细胞。淋巴系干/祖细胞是T淋巴细胞和B淋巴细胞的共同祖先细胞,和髓系的干/祖细胞一样,都来自骨髓的多能造血干细胞。淋巴系干/祖细胞在骨髓中进一步分化为T系前体细胞和B系前体细胞。随后,T系前体细胞迁移至胸腺,在胸腺微环境诱导下进一步发育分化,经不成熟的胸腺细胞,分化形成具有免疫功能的成熟T淋巴细胞;而B系前体细胞则在骨髓中继续分化增殖,经原始B淋巴细胞、幼稚B淋巴细胞,分化为成熟的B淋巴细胞。成熟B淋巴细胞经抗原刺激可继续分化为能合成和分泌免疫球蛋白的浆细胞,见图1-3。

图1-3 淋巴细胞的生成
在淋巴细胞中,除T淋巴细胞和B淋巴细胞外,还有一群既没有T淋巴细胞和B淋巴细胞表面标志又不具备特别识别功能的非T非B淋巴细胞。它们也由淋巴系干(祖)细胞分化增殖产生,经非T非B前体细胞、裸细胞,在骨髓内发育成熟。这包括自然杀伤细胞(NK)、淋巴因子活化的杀伤细胞(LAK)以及肿瘤浸润淋巴细胞(TIL)。
成熟淋巴细胞多储存于脾脏、淋巴结和其他淋巴组织中,外周血液循环的淋巴细胞不足全身所有淋巴细胞总数的5%。淋巴组织中的淋巴细胞能再进入血液循环,两者之间保持动态平衡。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














