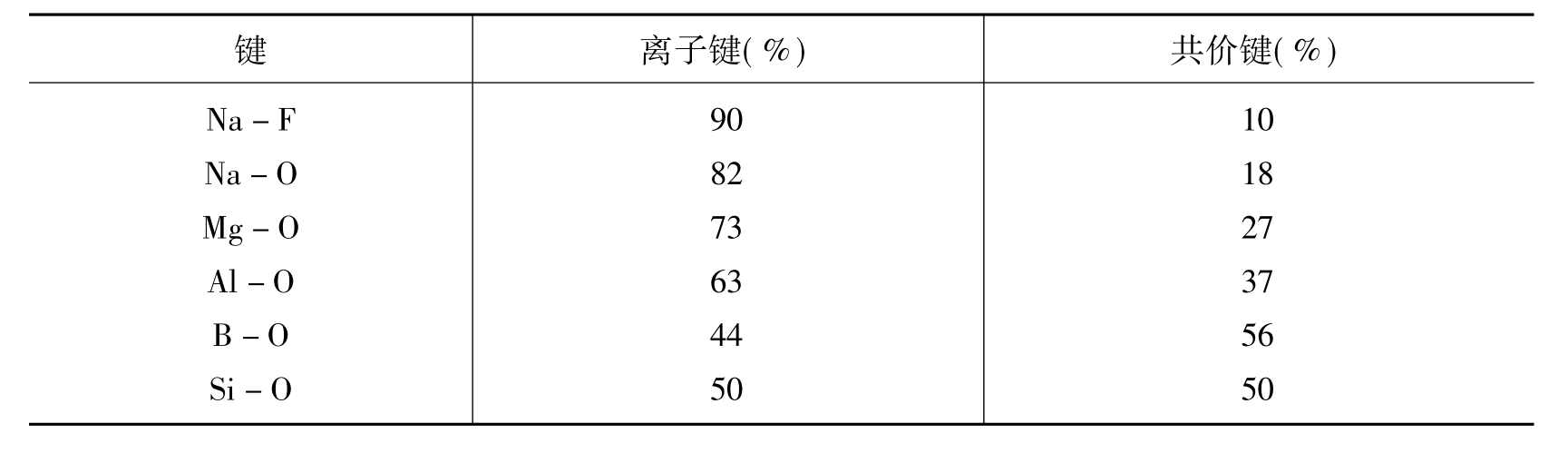
【摘要】:当原子间通过化学结合力产生了结合时,一般称为形成了化学键。典型的化学键有三种:离子键、共价键和金属键。电负性相差较大的元素的原子结合时即成离子键,而电负性相差较小的则成共价键。表4.2给出了一些硅酸盐中常见的原子结合键中离子键所占的成分,可以看出实际上往往形成许多过渡类型的键。此外,在一个晶体中不一定只存在一种性质的键,而经常是几种形式的键组合起来构成晶体,对很多硅酸盐晶体来说就是这样。
4.1 晶体中的化学键
用X射线进行结构分析证明晶体是具有空间格子构造的固体。也就是说,晶体中的质点(离子、原子或分子)在三维空间的排列是很有规律的。
质点之间具有相互结合的作用力,保证质点在晶体内一定的位置上作有规则的排列。当原子间通过化学结合力产生了结合时,一般称为形成了化学键。而分子之间的结合一般称为分子键或范德华键。典型的化学键有三种:离子键、共价键和金属键。这三种化学键和分子键总称为键的四种型式。
硅酸盐中碱金属离子与O2-的结合一般认为是比较典型的离子键,而Si-O结合键中,离子键和共价键成分各占50%。根据元素电负性(见表4.1)的不同,可以大致估计原子之间化学键的性质。电负性相差较大的元素的原子结合时即成离子键,而电负性相差较小的则成共价键。
表4.1 元素电负性值(X)
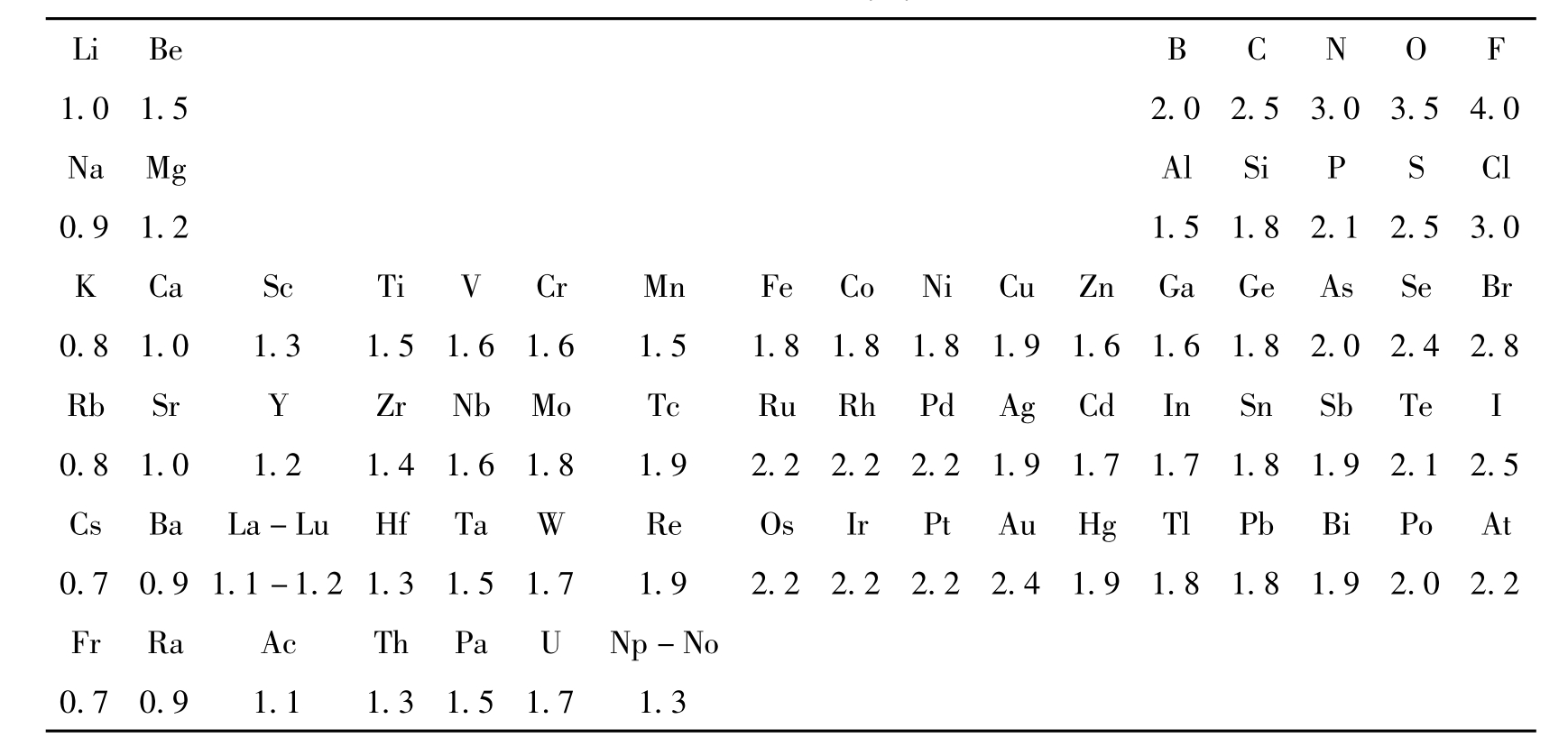
由两元素电负性的差值X A-X B,可从图4.1中查出该结合键中离子键所占的成分。表4.2给出了一些硅酸盐中常见的原子结合键中离子键所占的成分,可以看出实际上往往形成许多过渡类型的键。
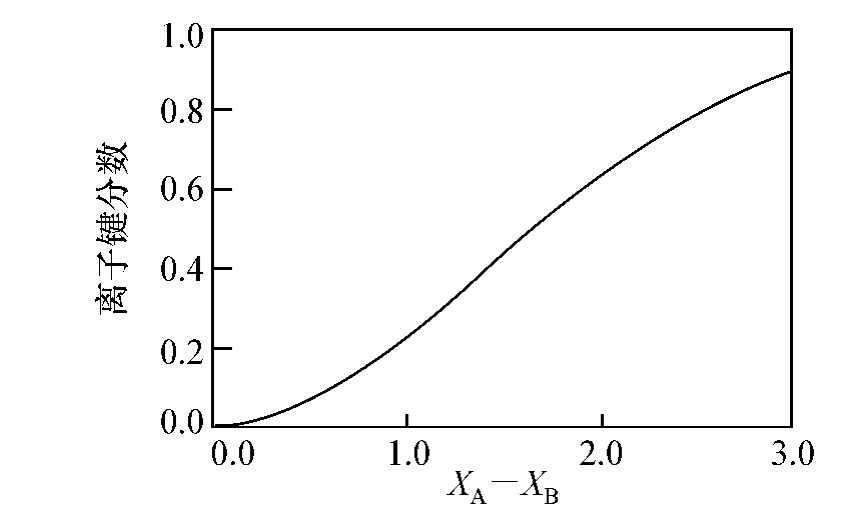
图4.1 A-B键的离子键分数与原子电负性的差X A-X B的关系
此外,在一个晶体中不一定只存在一种性质的键,而经常是几种形式的键组合起来构成晶体,对很多硅酸盐晶体来说就是这样。例如在黏土矿物中就存在有分子键和带共价性的离子键。
表4.2 硅酸盐中常见的原子结合键中离子键所占的成分
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















