二、金属中常见的三种晶格
由于金属键的结合特点,使金属内部原子趋向于作高度对称、最紧密和最简单的排列。金属原子的这种排列特点,决定了金属具有密度大,强度高,塑性、韧性好以及一系列良好工艺性能的特点,而成为最重要的工程材料。大多数金属的晶体结构都比较简单,其中常见的有以下三种。
(一)体心立方晶格
体心立方晶格的晶胞如图2-5所示。它是一个立方体。其晶格常数a=b=c,α=β=γ=90°。故晶格常数通常只用一个a来表示。体心立方晶格中原子排列的特征是:在立方体的中心和8个顶角上各有一个原子。由于每个顶角上的原子各为周围8个晶胞所共有,体心原子为该晶胞所独有,故一个体心立方晶胞中的实际原子数为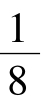 ×8+1=2个。由图2-5可见,这种晶胞在其立方体对角线方向上的原子是彼此紧密接触排列的,故由该对角线长度√3a上所分布的原子数目(共2个),可计算出其原子半径的尺寸为r=
×8+1=2个。由图2-5可见,这种晶胞在其立方体对角线方向上的原子是彼此紧密接触排列的,故由该对角线长度√3a上所分布的原子数目(共2个),可计算出其原子半径的尺寸为r=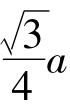 。
。
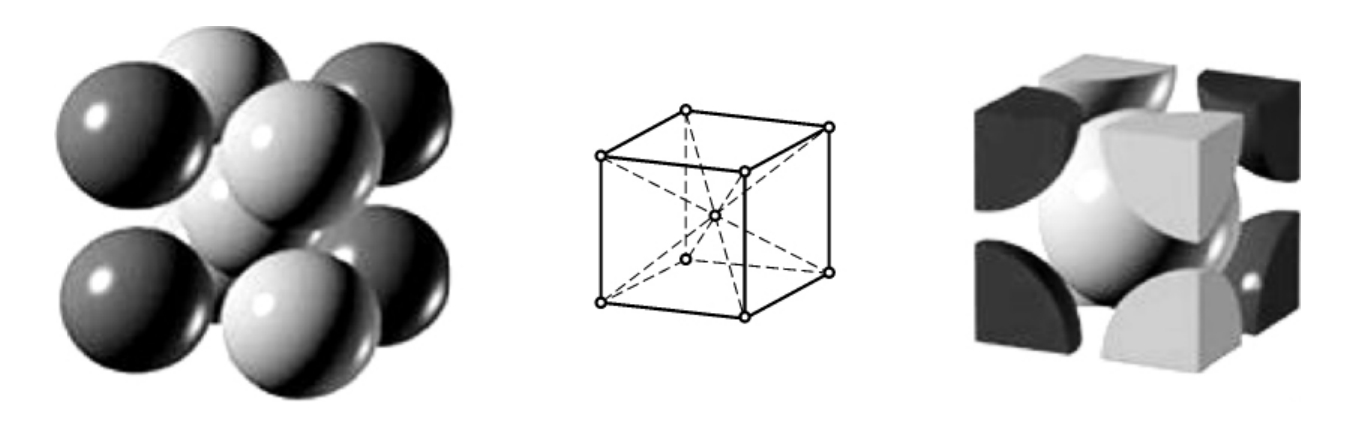
图2-5 体心立方晶胞
具有体心立方晶格的金属有铬(Cr)、钨(W)、钼(Mo)、钒(V)、α-Fe(室温下的铁)等。
(二)面心立方晶格
面心立方晶格的晶胞如图2-6所示。它也是一个立方体,所以也只用一个晶格常数a表示即可。面心立方晶胞原子排列的特征是:在立方体的6个表面的中心和8个顶角上各有一个原子。晶胞顶角上的原子为相邻的8个晶胞所共有,而每个面心的原子各为两个晶胞所共有。故一个面心立方晶胞中的实际原子数为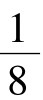 ×8+
×8+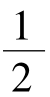 ×6=4个。显然,在这种晶胞中,每个底面对角线上各原子彼此相互接触,因而其原子半径的尺寸应为r=
×6=4个。显然,在这种晶胞中,每个底面对角线上各原子彼此相互接触,因而其原子半径的尺寸应为r=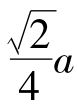 。
。
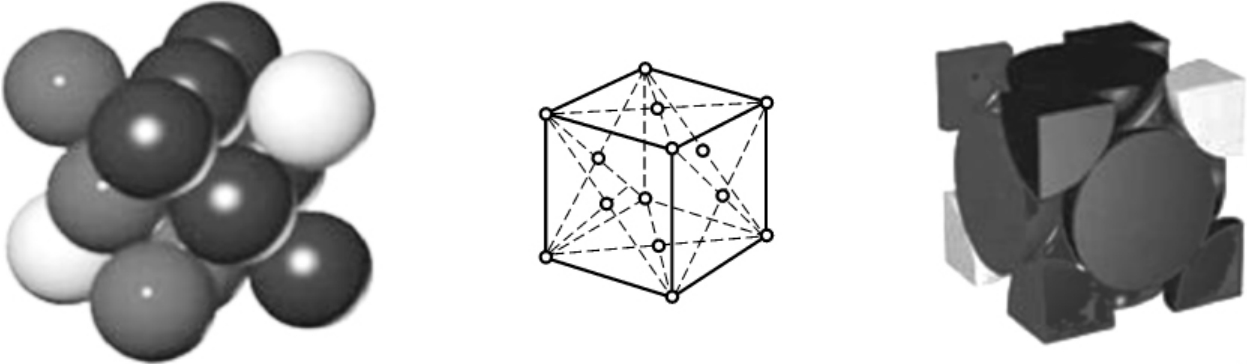
图2-6 面心立方晶胞
具有面心立方晶格的金属有γ-Fe(912~1394℃区间的铁)、铝(Al)、铜(Cu)、镍(Ni)、金(Au)、银(Ag)等。
(三)密排六方晶格
密排六方晶格的晶胞如图2-7所示。该晶胞是一个正六方柱体,由6个呈长方形的侧面和两个呈六边形的底面所组成。因此要用两个晶格常数表示,一是柱体的高度c,另一个是六边形的边长a。晶胞中原子排列特征是:在晶胞的12个顶角和上、下两个六边形底面的中心各有一个原子,此外在晶胞中间还有3个原子,它们在柱体高1/2处以柱体中心线对称组成一个等边三角形。晶胞每个顶角上的原子各为与其相邻的6个晶胞所共有,上下底面中心的原子各为两个晶胞所共有,晶胞中3个原子为晶胞所独有。故一个密排六方晶胞中的实际原子数为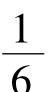 ×12+
×12+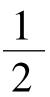 ×2+3=6个。
×2+3=6个。

图2-7 密排六方晶胞
具有密排六方晶格的金属有:镁(Mg)、锌(Zn)、镉(Cd)等。
除以上3种晶格外,少数金属还具有其他类型的晶格,但一般很少遇到。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















