(一)PTK-Ras-MAPK信号转导通路
1.Ras的作用 Ras是小分子G蛋白家族的成员之一,是PTK介导的信号转导通路中的一个关键组分,参与调控细胞生长、增殖,影响细胞分化、形态发生和凋亡。活化的PTK信号跨膜传递到Ras蛋白,通过丝裂原激活蛋白激酶(mitogen-activated protein kinase,MAPK)的级联反应传送到细胞核。
2.MAPK的作用 MAPK是一组丝/苏氨酸蛋白激酶,可经膜受体转换并传递细胞因子、生长因子、神经递质、激素、细胞应激及细胞黏附等的信号,并将其带入细胞核内。所有真核细胞都能表达MAPK,其通路的基本组成包括MAPKKK(MAPK kinase kinase)、MAPKK(MAPK kinase)和MAPK,这三级能依次激活,共同调节细胞的生长、分化、分裂、对环境的应激适应、炎症反应等多种重要的细胞生理/病理过程。MAPK家族种类繁多,主要有细胞外信号调节蛋白激酶(extracellular signal-regulated kinase,ERK)、c-JNK氨基末端激酶(c-Jun N-terminal kinase,JNK)/应激激活蛋白激酶(stress-activated protein kinase,SAPK)和p38 MAPK3个亚家族,它们上游的MAPKK和MAPKKK都不同。ERK可分为ERK1、ERK2和ERK3,大部分底物是能调控细胞周期和细胞分化的蛋白质。ERK1和ERK2是脯氨酸依赖的丝/苏氨酸蛋白激酶,优先催化底物中Pro-X-Ser/Thr或Ser/Thr-Pro序列磷酸化。细胞未受刺激时,MAPK处于静止状态。在细胞受到刺激后,MAPK接受上游分子MAPKK和MAPKKK的活化信号而激活,表现为逐级磷酸化。MAPK家族成员的活化需要分子中一个Thr-X-Tyr模体中的Thr和Tyr残基同时磷酸化,这两个残基的磷酸化由MAPKK单独完成。因此,MAPKKK和MAPK属于蛋白丝氨酸/苏氨酸激酶。MAPKK是同时具有磷酸化丝氨酸/苏氨酸和酪氨酸的双功能激酶。
3.转导信号的主要过程 PTK-Ras-MAPK系统转导信号的主要过程如下。
(1)受体活化:当配体与受体的胞外区结合后,相邻受体二聚化,构象改变,PTK活性增强,胞内区的酪氨酸残基在激酶作用下自身磷酸化,产生了可被SH2结构域识别和结合的位点。
(2)活化的受体识别含有SH2结构域的接头蛋白:接头蛋白GRB2有1个SH2结构域和2个SH3结构域。它一边通过其SH2结构域识别并结合到活化PTK的磷酸化酪氨酸残基上,一边通过SH3结构域识别并结合下游的信号蛋白——鸟苷酸交换因子SOS,形成GRB2-SOS复合物,经核苷酸交换,将信号传递到Ras。
(3)在SOS的作用下激活Ras蛋白:GRB2通过N-末端的SH2结构域将GRB2-SOS复合物与受体连接,并将其转移至细胞膜上,募集SOS,提高SOS在细胞膜上的局部浓度。SOS发挥其核苷酸转移酶的活性,激活下游Ras蛋白。
(4)启动MAPK级联反应:活化的Ras作用于其下游分子Raf(属于MAPKKK),Raf作用于MEK(属于MAPKK),磷酸化的MEK再作用于ERK(属于MAPK)。
(5)MAPK介导生物学效应:MAPK可调节花生四烯酸的代谢和细胞微管形成;催化细胞核内多种反式作用因子(如转录因子)磷酸化,开关基因转录等(图12-17)。
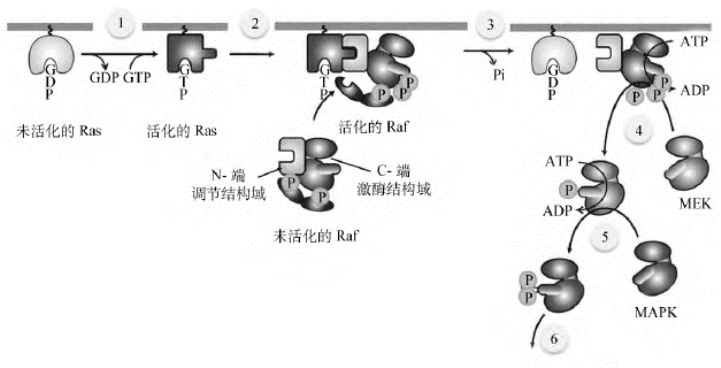
图12-17 PTK-Ras-MAPK信号转导通路
1.GTP取代GOP后,Ras被激活;2.活化的Ras募集、结合并激活Raf;3.GTP水解导致Ras与Raf分离;4.Raf活化MEK;5.MEK活化MAPK;6.激活许多转录因子
(二)JAKs-STAT信号转导通路
干扰素、白细胞介素-2、白细胞介素-3等细胞因子受体缺乏酪氨酸蛋白激酶活性,但能通过与之相结合的蛋白酪氨酸激酶JAKs(Janus kinase)传递信息。JAKs再通过激活下游的信号转导子和转录激活子(signal transductor and activator of transcription,STAT)最终影响基因转录,此途径称为JAKs-STAT信号转导通路。
1.JAK的家族成员、结构域及其作用 JAK是Firmback-Kraft在1990年发现的,也是一类酪氨酸蛋白激酶。1994年正式命名为JAKs家族,目前已发现5种JAK,分别是JAK1、JAK2、JAK3、JAK4和TYK2。该家族无跨膜结构域和Src同源结构域(SH2、SH3、PH结构域),但有7个JH(Janus homology)结构域(图12-18)。其中JH1和JH2为所有PTK所共有,羧基端的JH1为催化结构域,JH2为激酶相关结构域,是保守基团,功能不清。JH3、JH4为完全保守序列,JH6和JH7有1个保守氨基酸。JH3~JH7功能不详,可能与细胞因子受体结合有关。
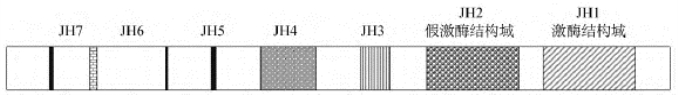
图12-18 JAKs的结构
2.STAT的家族成员、结构域及其主要作用 STAT是一种核内转录因子,由750~850个氨基酸残基组成,在静息细胞中存在于胞质。
(1)家族成员:目前已发现6种STAT,包括STAT1α/β、STAT2、STAT3、STAT4、STAT5a、STAT5b和STAT6。
(2)结构域:STAT在结构上主要由N-末端结构域(ND)、卷曲螺旋结构域、DNA结合结构域、接头结构域(LD)、SH2结构域及C-末端的转录活性功能结构域(transcription activation domain,TAD)组成(图12-19)。N-末端结构域是STAT二聚化和STAT二聚体相互作用结构域。卷曲螺旋结构域是STAT与其他已结合在靶启动区或溶液中的转录因子相互作用的部位。DNA结合结构域位于400~500氨基酸残基之间,LD结构域参与转录。SH2结构域位于600~700氨基酸残基之间,具有高度的保守性,对于STAT的活化和功能有其重要作用。

图12-19 STAT的结构
(3)主要作用:①使STAT蛋白与酪氨酸已被磷酸化的受体亚基结合;②已与受体结合的STAT的Tyr残基被JAK磷酸化后,通过SH2结构域产生二聚体;③对STAT与活化的JAK结合有重要作用。TAD上存在丝氨酸磷酸化位点,保守性极差。
3.生理功能 JAKs-STAT信号转导通路是在研究干扰素信号传递过程中最先发现的(图12-20)。
(1)当配体与受体结合后,受体二聚化,增加了与JAK的亲和力,使受体亚基上JAK相互靠近并进一步活化。同时,JAK也使受体上Tyr残基磷酸化,吸引有SH2结构域的STAT与之结合,并催化STAT的Tyr701磷酸化,Tyr701磷酸化是STAT入核的必要条件。磷酸化的STAT与受体亲和力降低并与之解离,形成二聚体或与其他蛋白形成复合物进入细胞核,结合于启动子相关序列,作为转录因子调节相关基因表达,改变靶细胞的增殖和分化。
(2)不同的受体偶联不同的JAK家族成员,使该途径传递的信号具有多样性和灵活性。如红细胞生成素(erythropoietin,EPO)受体、生长激素(growth hormone,GH)受体、催乳素(prolactin,PRL)受体和粒细胞集落刺激因子(granulocyte-colony stimulating factor,G-CSF)受体能与JAK2结合,干扰素α、β与JAK1和TYK2结合,干扰素γ则与JAK1和JAK2结合。1994年关于血管紧张素Ⅱ可活化STAT1的报道,首次证明G蛋白偶联的受体也可引起该通路的激活,从而扩大了JAKs-STAT信号转导通路在多种信号分子、多种受体结构传递信息过程中存在的可能性。
(三)NF-κB信号转导通路
核因子-κB(nuclear factor-κB,NF-κB)几乎存在于所有细胞中,是真核细胞的转录因子。1986年首先发现它是B细胞中免疫球蛋白kappa轻链转录所需要的核转录因子,后被证实广泛参与机体防御反应、组织损伤和应激、细胞分化和凋亡及肿瘤生长抑制等过程。肿瘤坏死因子受体(TNF-R)、白细胞介素-1受体等促炎细胞因子受体家族主要通过NF-κB信号转导通路介导信号。

图12-20 JAKs-STAT信号转导通路
NF-κB由p50和p65两个亚单位组合成同源或异源二聚体,即p50-p50、p65-p65和p50-p65,在体内发挥生理功能的主要是p50-p65二聚体。NF-κB结构内包括DNA结合区、蛋白质二聚化区和核定位信号。静止状态下,NF-κB在胞质内与NF-κB抑制蛋白(inhibitor of NF-κB,IκB)结合成无活性的复合物。当TNFα作用于相应受体后,通过第二信使神经酰胺(Cer)等激活系统,而病毒感染、脂多糖、活性氧中间体、佛波酯、双链RNA以及活化的PKA和PKC等通过IκB的磷酸化使其从NF-κB脱落,直接激活NF-κB。活化的NF-κB转位进入细胞核,与NF-κB结合增强元件特异性结合,影响多种细胞因子、黏附因子、免疫受体、急性时相蛋白和应激反应蛋白基因的转录(图12-21)。
用氧化物刺激肺组织后,肺部炎症细胞浸润,同时内皮细胞核内NF-κB迅速增加,低血容量休克可诱导肺组织NF-κB激活,流感病毒等刺激呼吸道上皮细胞后可激活NF-κB,哮喘患者气道中NF-κB激活增加,可造成细胞因子网络失衡及某些细胞因子和黏附因子高表达。如果阻断NF-κB激活则可改善肺部炎症反应。
(四)TGF-β信号转导通路
1.转化生长因子(transforming growth factor,TGF)超家族 可分为多个亚家族,包括TGF-β/activin家族、BMP(bone morphogenetic protein)/GDF(growth and differentiation factor)/MIS(muellerian inhibiting substance)家族。参与细胞的增殖、分化、迁移和凋亡等多种反应。TGF-β超家族受体分为2个亚族,即TβRⅠ和TβRⅡ。其特征是自身具有蛋白丝氨酸/苏氨酸激酶催化结构域。
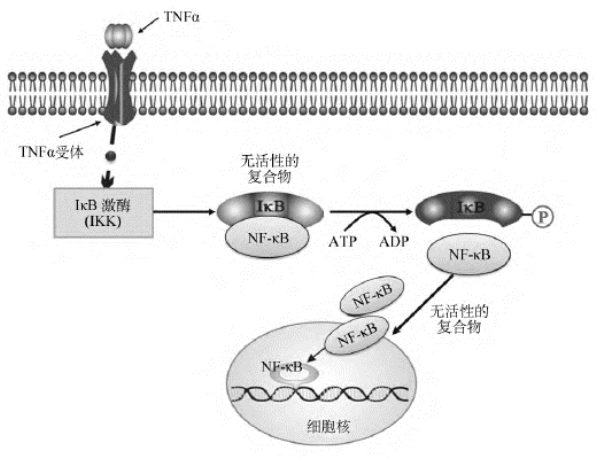
图12-21 NF-κB信号转导通路
2.主要生理功能
(1)Smad家族是最早被证实的TβR激酶的底物,其命名来自于果蝇的Mother against dpp(Mad)和线虫的Smad基因。高等生物中至少有9种不同的Smad蛋白,选择性地与两种TβR结合,发挥不同的功能。Smad蛋白有两个保守结构域,N-末端的MH1(Mad Homology)区和C-末端的MH2区。这两个保守结构域为球形结构,在静息状态时相互抑制,活化后与核内一些调节蛋白相互作用,调节转录。MH1区有一个富含赖氨酸的H2螺旋、β发夹结构及锌指结合区。H2螺旋是Smad1和Smad3的核定位信号(nuclear localization sequence,NLS)。β发夹突出表面,能与DNA双螺旋表面的大沟结合。所有Smad蛋白的MH2区高度保守,未磷酸化的Smad蛋白MH2区C-末端是SSXS模体,其中的两个丝氨酸残基磷酸化后能使Smad蛋白激活,在受体作用下能形成同源或异源二聚体。MH1区和MH2区之间是连接区,含有多个磷酸化位点,能与其他信号转导通路发生交互作用。另外,MAPK能使某些Smad的连接区磷酸化,抑制其向核内转移和积聚。
(2)TGF-β是一种分泌型多功能多肽,许多疾病包括癌症都涉及TGF-β调节过程的异常。当TGF-β结合跨膜受体时,与TGF-βⅠ、Ⅱ受体形成异源三聚体,TβRⅡ通过磷酸化TβRⅠ的GS区而激活TβRⅠ,TβRⅠ再磷酸化并激活Smad蛋白,后者进入细胞核,和其他核内转录调节因子结合,调节目的基因的转录(图12-22)。
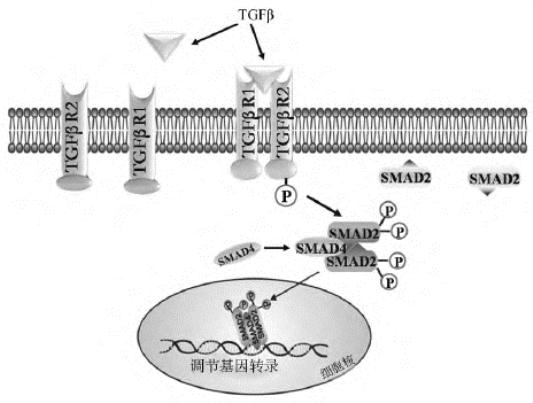
图12-22 TGF-β信号转导通路
TGF-β信号转导通路与JAKs-STAT信号转导通路具有一定的相似性。在这两种通路中,胞质转录因子通过磷酸化反应被激活,从而以低聚体复合物形式转移到细胞核内与DNA作用。另外,从胞外信号产生至达到转录水平的间隔都很短。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














