组织工程支架材料的很多生物相容性评价都是在动物体内进行的,动物实验经常提供非常重要的数据。所以进行体内评价试验时,应采用适当性别和种属的动物,并根据组织工程支架材料的大小选择大小适宜的健康成年动物,并至少适应实验室环境7d。本节主要介绍ISO-10993及国标中常见的体内评价试验。
在进行生物相容性评价时,如果无法采用试验组织工程支架材料进行,可采用浸提液作为试验用品,但是所得结果是有一定局限性的。制备浸提液的浸提介质要与临床的使用情况相适用,并在洁净和化学惰性的封闭容器中进行,浸提介质包括:生理盐水、无血清液体培养基、植物油等,浸提温度与时间可根据试验样品性能和临床使用情况进行选择:37±1℃,24±2h;37±1℃,72±2h;50± 2℃,72±2h;70±2℃,24±2h;121±2℃,1±0.2h。试样大小见表7-6。
表7-6 试验样品表面积或重量和浸提介质的比例

一、致 敏 试 验
根据ISO-10993-1的定义,致敏作用及迟发性接触超敏性是一种变态反应,涉及先前接触已被激活的免疫系统。本试验的目的是评价组织工程支架材料对生物体的潜在致敏性,目前国际上主要采用两种方法:最大剂量法和封闭斑贴法,前者是最敏感和首选方法,本文主要对其进行叙述。
【试验动物】 豚鼠体重300~500g,1~3个月龄。每组(包括阴阳对照组)至少10只,试验前24h,剔除豚鼠背部4cm×6cm毛发。
【试验组织工程支架材料】
试验样品的生理盐水浸提液:5%(V/V)甲醛溶液或2,4-二硝基氟苯作为阳性对照生理盐水阴性对照。含浸提介质的完全弗氏佐剂:将浸提介质或组织工程支架材料浸提液与完全弗氏佐剂等体积混合,用力搅拌数分钟至完全乳化为止。
【试验步骤】
(1)诱导
①皮内注射:用70%(V/V)乙醇清洁暴露区域,在每只去毛区作6点对称的皮内注射,各点相距1~2cm(图7-1)。
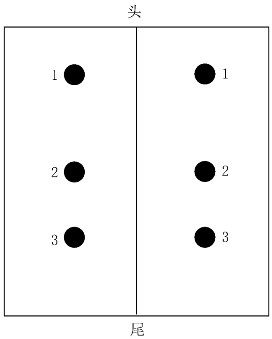
图7-1 过敏试验注射剂型与注射位置
②局部斑贴:皮内注射后1周,在去毛区再剔毛,用70%(V/V)乙醇清洁。若未出现刺激反应,每一试验区用10%十二烷基硫酸钠石蜡液(SLS)预处理,在局部斑贴前24h用玻璃棒涂抹,按摩,使SLS进入皮肤,以加强致敏作用。24h后,用试液饱和2cm×4cm滤纸,将其敷贴于豚鼠背部的注射部位,用3.75cm长的外科棉纱封闭固定48h。
(2)激发:于末次致敏后14~28d,在豚鼠左右腹侧未实验处剃毛,用70(V/V)乙醇清洁,按以上描述的试样制备的方法,将滴有被试液饱和的滤纸(2cm×2cm)贴于剃毛区,封闭保留24h。
【结果观察与评定标准】 将敷贴物取下后1、24和48h,分别观察该处红斑和水肿,按表7-7和表7-8给各点记分并分级。按1、24和48h情况列表,若试样分级2或大于2,则认为致敏。如阴性对照的部分动物(超过50%)的记分为1,则另用10只动物重复试验。如60%阳性对照动物的反应不是2或不大于2,则重复试验。
表7-7 致敏反应和记分标准
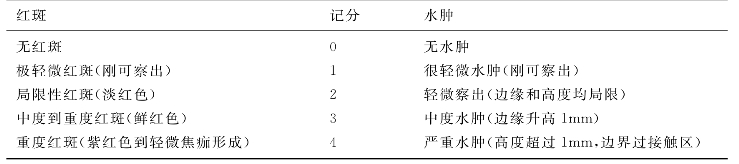
表7-8 致敏反应率

二、刺 激 试 验
根据ISO-10993-1的定义,刺激是不涉及免疫学机制的一次、多次或持续与试验组织工程支架材料接触引起的局部炎症反应,炎症主要表现为细胞的变质、渗出和组织细胞增生。
组织工程支架材料应根据使用方式、使用部位、使用剂量、接触组织持续时间等选择标准中规定的相应试验方法,如与软组织接触的产品可选择皮肤刺激试验,而眼刺激试验仅用在其他方法不能获得安全性评价时才考虑,而且仅限于接触眼或眼睑的组织工程支架材料。其他如体内刺激试验、口腔、直肠等部位刺激试验等,本文重点介绍皮肤刺激试验。
【试验动物】 新西兰白兔,体重>2kg,每组动物至少3只,试验前24h背部去毛。
【试验组织工程支架材料】 组织工程支架材料浸提液0.5ml,或液态组织工程支架材料0.5ml或适于贴敷的固体或粉末组织工程支架材料0.5g。
阳性对照:3%~5%甲醛溶液;阴性对照:生理盐水。
【试验步骤】 在脊柱两侧各选2个2~3cm2面积的去毛区将试验样品斑贴,用4层25mm×25mm纱布覆盖,包扎固定。4h后,除去斑贴物,并标记斑贴部位,用温水或70%乙醇清洁后吸干。若组织工程支架材料预期长期与皮肤接触,则需每日进行重复试验,但是时间不要超过3周。
【结果观察与评定】 按表7-9计分标准,在移去斑贴物后24h、48h和72h后对试验部位的红斑和水肿反应计分。
表7-9 皮肤反应计分标准

根据计算结果,0~0.4分为无刺激,0.5~1.9为轻度刺激,2.0~4.9为中等刺激,5.0以上为强刺激。
三、热 原 试 验
本试验是采用兔法进行,即将一定量试验组织工程支架材料的浸提液由静脉注入兔体内,观察兔体温的变化,以确定浸提液中所含热原含量是否符合人体应用要求的一种方法。
【试验动物】 健康成年新西兰兔,体重2.5~3kg,雌兔应无孕。而且在测量7d内体温均在38.3~38.6℃,选用的家兔至少在2周内不能做第二次检查用。
【试验组织工程支架材料】 组织工程支架材料生理盐水浸提液。
【试验步骤】 每种组织工程支架材料浸提液选用3只符合要求的家兔,避免兔躁动并停止给食2h以上,选用肛温计测量直肠温度,插入深度各兔各次应相同(一般约为6cm),或用其他同样精确测量装置亦可。每隔30~60min测量1次,一般测量2~3次,两次体温不得超过0.2℃。以此两次的平均值作为该兔的正常体温。测定其正常体温后15min内,自耳静脉缓慢注入试验组织工程支架材料浸提液,剂量为10ml/kg,液体温度为37℃。注射后每隔1h测量体温1次,共测3次,以3次中体温最高的一次减去正常体温,即为该兔的升高度数。
【结果判断】 在初试的3只家兔中,体温升高均在0.6℃以下,并且体温升高度数在1.4℃以下;或在复试的5只家兔中,体温升高0.6℃或0.6℃以上的总数仅有1只,并且初复试的8只家兔的体温升高数不超过3.5℃时,均应认为试验组织工程支架材料浸提液符合热原检查要求。
四、体内植入试验
采用动物植入试验可从宏观和微观水平来评价组织工程支架材料对组织的局部反应。组织工程支架材料的理化性质(如形状、密度、硬度、表面光洁度、酸碱度等)、植入部位或体内负荷。移动都可能影响局部组织的反应性。根据组织工程支架材料类别和用途等,可选择不同的试验周期和试验部位。肌肉植入为常规试验方法。
【试验动物】 埋植于肌肉或皮下组织的短期试验可选择小鼠、大鼠、仓鼠、豚鼠或者兔;埋植于肌肉或骨骼组织的长期试验可选择兔、狗、绵羊、山羊或其他生命周期较长的动物。
【试验组织工程支架材料】 对照组织工程支架材料:医学上已经接收的生物组织工程支架材料以及证实没有或仅有极小的组织反应性的组织工程支架材料,优先选择已经采用和试验样品有相同应用范围的组织工程支架材料。
【试验步骤】
(1)肌肉植入试验:将组织工程支架材料(1mm×10mm圆柱形,表面光滑,边缘平整)植入家兔或犬背部深层肌肉,定期采集标本和周围组织,肉眼及显微镜下观察接触部位组织反应。
以家兔为例,选用符合要求的健康家兔不少于10只,剪去背毛,常规消毒,在脊柱两侧旁1.5cm处等距离各选四个埋植点,每点间距为2cm,一侧植入试样4条,另一侧植入对照样品4条,深度为1~2cm,缝合肌筋膜和皮肤切口。植入后的7、15、30、60、90d分别以气栓法或2.5%戊二醛血管注入法人道处死动物,每个时间组不少于2只,仔细切取样品周围0.5~1.0cm厚的肌肉,置入10%甲醛溶液中固定,作石蜡包埋,伊红—苏木精和VG染色。组织修整后,每块肌肉做两周染色,每种染色各做2张组织学切片,显微镜下作组织学观察。
(2)皮下植入试验:常规背部皮下植入,植入试样组织工程支架材料形状为推荐为圆柱体,大小根据所选择动物大小设计。常规消毒,切开皮肤,钝性分离皮下组织形成空腔,腔底应比切口线长10mm,植入体放入腔底,每个空腔植入一个试验样品。缝合皮下组织及皮肤。
(3)骨内植入试验:对不能吸收的非降解组织工程支架材料,以测定植入部位骨组织生物反应。这种试验也可以用来测定同种组织工程支架材料,不同表面形态和结构的生物学反应,或者评价治疗方法和组织工程支架材料改良效果。植入组织工程支架材料也推荐为圆柱体形状,大小根据试验动物大小设计。
暴露股骨和胫骨外侧骨皮质,钻骨洞,骨洞内径应和组织工程支架材料外径相匹配。兔预钻3洞,大动物预钻6洞。将组织工程支架材料紧密嵌入。
【结果观察与评定】
(1)炎性细胞反应分级
Ⅰ级:试样周围未见或仅见极少量淋巴细胞;
Ⅱ级:试样周围可见少量淋巴细胞;
Ⅲ级:试样周围有少量嗜中性粒细胞、淋巴细胞浸润和巨细胞反应;
Ⅳ级:试样周围可见以嗜中性粒细胞浸润为主的炎性反应,可见吞噬细胞。
(2)纤维囊形成
Ⅰ级:囊壁厚度稳定且小于等于0.03mm,无继续增生现象;
Ⅱ级:纤维化囊壁致密,壁的厚度比形成初期要薄;
Ⅲ级:试样周围可见纤维母细胞与胶原纤维,并已形成纤维囊腔结构;
Ⅳ级:试样周围可见小血管与纤维母细胞增生,开始形成疏松囊壁。
(3)结果评定合格标准
植入7d后,炎症细胞反应程度≤Ⅳ级,无囊壁形成;
植入15d后,炎症细胞反应程度≤Ⅲ级,囊腔形成至少为Ⅳ级;
植入30d后,炎症细胞反应程度≤Ⅱ级,囊腔形成至少为Ⅲ级;
植入60d后,炎症细胞反应程度≤Ⅰ级,囊腔形成至少为Ⅱ级;
植入90d后,囊腔形成状况为Ⅰ级;
植入180、360d后,两种反应均小于Ⅰ级。
五、体内末梢静脉血栓形成试验
本试验是评价植入组织工程支架材料直接接触血液时血栓形成的情况。血栓形成试验方法包括堵塞百分率、流速降低、重量分析(血栓重量)、光学显微镜、扫描电子显微镜(SEM)、组织工程支架材料产生的压降、组织工程支架材料的剖检、远侧器官的剖检、血管造影术等。试验过程中测量血液流速,试验完后将组织工程支架材料取出进行血栓重量分析,堵塞可能是因为血栓形成或者内膜增生引起的,所以定量测定堵塞百分率后,须用显微镜来识别堵塞性质,并可获得有关细胞密度、细胞聚集和纤维蛋白附着的情况以及表面沉积物的几何分别情况。
【试验动物】 成年羊或者犬。
【试验组织工程支架材料】 将试验样品涂于直径1mm,长13mm的尼龙丝或者手术缝线外面,制成试材丝线,试验前乙醇消毒后,生理盐水冲洗。
对照丝线:未经涂敷组织工程支架材料的丝线。
【试验步骤】 动物麻醉后,用18号针头穿刺其两侧头静脉及股静脉四条静脉,分别将试材丝线和对照丝线通过针头送入各侧静脉内约100mm,然后将针头退出,丝线末端用敷料包裹黏牢。2h或4h后,颈静脉注射肝素1支。颈动脉放血处死动物,将植入试材丝线的动脉剖开,用肉眼、显微镜、扫描电镜观察及透射电镜等观察血栓形成情况。
【结果观察与评定】
(1)肉眼观察
无血栓 Macro(-)
部分有血栓 Macro(+)
全部有血栓 Macro()
血栓闭塞 Macro()
(2)光镜观察
无血栓 LMS(-)
血小板、纤维蛋白黏附LMS(+)
部分血栓形成 LMS()
全部血栓形成 LMS()
(3)扫描电镜观察
无血栓 SEM(-)
血小板变形 SEM(+)
纤维蛋白黏附 SEM()
血栓附着 SEM()(
4)透射电镜观察
无血栓 TEM(-)
血小板变形、形态变化TEM(+)
纤维蛋白析出 TEM()
血栓形成 TEM()
六、遗传毒性、致癌性和生殖毒性
与生物相容性评价标准中的其他各种风险评价相比,遗传毒性、致癌性和生殖毒性的评价方法不那么完善,对组织工程支架材料进行检验的有效性也未得到很好的确认。
一般认为致癌的是指组织工程支架材料显示能引起恶性肿瘤形成几率升高;诱变的是指组织工程支架材料能引起细胞中遗传编码发生变化;致肿瘤的指组织工程支架材料显示能引起恶性肿瘤或良性肿瘤形成概率升高。从原理上讲,一诱变物通常必须诱导一早期的DNA损伤,该损伤通常会被DNA修复酶所修复,但当这些系统不足、不存在或者超负荷时,该损伤将留在DNA中,当细胞分裂时,可能导致诱变。
相关的ISO10993标准提供了以下相关试验。
1.遗传毒性试验 用哺乳动物或非哺乳动物细胞、细菌、酵母菌或真菌测定组织工程支架材料或组织工程支架材料浸提液是否引起基因突变、染色体结构畸变以及其他DNA或基因变化。自从致癌性和Ames试验诱变效益之间的关系被证实,动物长期致癌试验与短期诱变试验之间的相关性被确定在50%~70%的范围内,然而这种相关性随着化学种类的不同而不同。按照国际标准,基因突变和染色体作用的研究是强制实施的,同时也建议至少要在一种哺乳动物身上做体内研究(表7-10)。
表7-10 所选著名突变试验的分类

2.致癌性试验 在试验动物的寿命期间,经一次或多次接触试验组织工程支架材料,测定潜在致癌性,这些试验可以设计成在一次试验研究中既测定慢性毒性又测定致肿瘤性。大多数生物组织工程支架材料能促使啮齿动物肿瘤的形成,它们中含有多种或来源于成分或降解产生的、已知是化学致癌物的成分。化学致癌作用是一个复杂的现象,与致癌剂进入到适当的细胞内结构,一般认为是DNA(但也可能是其他靶)有关。然而因组织工程支架材料植入后形成肿瘤的临床证据很少,要求对组织工程支架材料进行这项试验的主要是那些没有植入人体足够长时间的新组织工程支架材料。
动物模型推荐使用Fischer 344大鼠和其他品系,每组动物的数目应足以进行可记录的风险统计分析评价及常规用途,全国性的毒性学项目要求化学品研究要用60只动物/性别/组,其中10只在2年内处死,对照动物作为阴性对照。
3.生殖及发育毒性试验 评价试验器械、组织工程支架材料或浸提液对生殖功能、胚胎发育(致畸性)以及胎儿和早期婴儿发育潜在影响的试验。受精前组织工程支架材料要植入一段时间使得任何腐蚀、可溶出或降解产物得以扩散,要模拟人的接触途径而且要避免压迫怀孕期的动物,受精能力和生殖能力要等同于适当高的人体接触水平进行评价。每天都要观察动物毒性临床症状,记录每组动物的平均食量和体重,20d后处死并检查母性的肝脏和子宫重量、植入部位、幼仔重量、性和形态学的发育,比较受孕大鼠的对照组和试验组。
(暨南大学化学系 周长忍 罗丙红 李立华)
参 考 文 献
1 田 莳 .组织工程支架材料物理性能 .北京:北京航空航天大学出版社,2001
2 马如璋,徐祖雄 .组织工程支架材料物理现代研究方法.北京:冶金工业出版社,1997
3 刘振海 .热分析导论 .北京:化学工业出版社,1991
4 于伯龄 .实用热分析 .北京:纺织工业出版社,1990
5 余 焜 .组织工程支架材料结构分析基础 .北京:科学出版社,2000:170-240
6 吴 刚 .组织工程支架材料结构表征及应用.北京:化学工业出版社,2002
7 左演声,陈文哲,梁 伟 .组织工程支架材料现代分析方法.北京:北京工业大学出版社,2000
8 张美珍,柳百坚,谷晓昱 .聚合物研究方法 .北京:中国轻工业出版社,2000
9 殷敬华,莫志深 .现代高分子物理学(下册).北京:科学出版社,2001
10 薛 奇 .高分子结构研究中的光谱方法 .北京:高等教育出版社,1995
11 裘绍文,裴奉奎 .核磁共振波谱 .北京:科学出版社,1992
12 何曼君,陈维孝,董西侠 .高分子物理 .上海:复旦大学出版社,1990
13 刘世宏,王当憨,潘承璜编著.X射线光电子能谱分析.北京:科学出版社,1988
14 常铁军,祁 欣,刘喜军,等 .组织工程支架材料近代分析测试方法 .哈尔滨:哈尔滨工业大学出版社,1999
15 黄惠忠,吴念祖,于广华,等 .论表面分析及其在组织工程支架材料研究中的应用 .北京:科学技术文献出版社,2002
16 和 平,奚廷斐,卜长生编 .医疗器械监督管理和评价.中国医药科技出版社,2000
17 杨志明主编组织工程 .化学工业出版社,2003.1
18 田 莳 .组织工程支架材料物理性能 .北京:北京航空航天大学出版社,2001
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















