实验17 离子选择性电极法测定水中氟含量
实验目的
(1)掌握离子选择性电极法测定离子含量的原理和方法;
(2)掌握标准曲线法和标准加入法测定水中微量氟的方法;
(3)了解使用总离子强度调节缓冲溶液的意义和作用;
(4)熟悉氟电极和饱和甘汞电极的结构和使用方法;
(5)掌握酸度计的使用方法。
实验原理
饮用水中氟含量的高低对人体健康有一定影响,氟的含量太低易得龋齿,过高则会发生氟中毒现象,适宜含量为0.5mg·L-1左右。因此,监测饮用水中氟离子含量至关重要。氟离子选择性电极法已被确定为测定饮用水中氟含量的标准方法。
离子选择性电极是一种电化学传感器,它可将溶液中特定离子的活度转换成相应的电位信号。氟离子选择性电极的敏感膜为LaF3单晶膜(掺有微量EuF2,利于导电),电极管内装有0.1mol·L-1NaF和0.1mol·L-1NaCl组成的内参比溶液,以Ag-AgCl作内参比电极。当氟离子选择性电极(指示电极)与饱和甘汞电极(参比电极)插入被测溶液中组成工作电池时,电池的电动势E在一定条件下与F-离子活度的对数值成线性关系,即
![]()
式中:K值在一定条件下为常数;s为电极线性响应斜率,其理论值为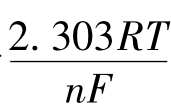 ,25℃时为0.059V。当溶液的总离子强度不变时,离子的活度系数为一定值,工作电池电动势与F-离子浓度的对数成线性关系,即
,25℃时为0.059V。当溶液的总离子强度不变时,离子的活度系数为一定值,工作电池电动势与F-离子浓度的对数成线性关系,即
![]()
为了测定F-的浓度,常在标准溶液与试样溶液中同时加入相等的足够量的惰性电解质以固定各溶液的总离子强度。
试液的pH值对氟电极的电位响应有影响。在酸性溶液中H+与部分F-形成HF或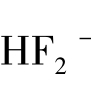 等在氟电极上不响应的形体,从而降低了F-的浓度。在碱性溶液中,OH-在氟电极上与F-产生竞争响应,此外OH-也能与LaF3晶体膜产生如下反应
等在氟电极上不响应的形体,从而降低了F-的浓度。在碱性溶液中,OH-在氟电极上与F-产生竞争响应,此外OH-也能与LaF3晶体膜产生如下反应
![]()
该反应的干扰电位响应使测定结果偏高。因此,测定需要在pH=5~6的溶液中进行,常用缓冲溶液HOAc-NaOAc来调节。
氟电极的优点是对F-响应的线性范围宽(1~10-6mol·L-1),响应快,选择性好。但能与F-生成稳定配合物的阳离子(如Al3+、Fe3+等)以及能与La3+形成配合物的阴离子会干扰测定,通常可用柠檬酸钠、EDTA、磺基水杨酸或磷酸盐等加以掩蔽。
使用氟电极测定溶液中氟离子浓度时,通常是将控制溶液酸度、离子强度的试剂和掩蔽剂结合起来考虑,即使用总离子强度调节缓冲溶液(TISAB)来控制最佳测定条件。本实验的TISAB的组成为NaCl、HOAc-NaOAc和柠檬酸钠。
仪器和药品
仪器:pHS—2C酸度计、氟离子选择性电极、饱和甘汞电极、电磁搅拌器、塑料烧杯、移液管、吸量管、容量瓶。
药品:药品及其配制方法如下。
1)100μg·mL-1氟标准溶液
准确称取于120℃干燥2h并冷却的分析纯NaF0.221g于烧杯中,加入少量水使之溶解并定量地转移至1000mL容量瓶中,稀释定容,摇匀。贮存于塑料瓶中。
2)10.0μg·mL-1氟标准溶液
将上述储备液定量稀释10倍。
3)总离子强度调节缓冲溶液(TISAB)
于1000mL烧杯中加入500mL去离子水、57mL冰醋酸、58gNaCl及12g柠檬酸钠(Na3C6H5O7·2H2O),搅拌至溶解。将烧杯置于冷水浴中,缓缓滴加6mol·L-1NaOH溶液,直至溶液的pH值为5.0~5.5(用酸度计测定),冷却至室温,转入1000mL容量瓶中,用去离子水稀释定容并摇匀。
实验步骤
1.酸度计的调试
参阅酸度计的使用方法。
2.标准曲线法测氟离子含量
1)氟标准溶液系列的配制
准确移取10.0μg·mL-1氟标准溶液1.00、4.00、7.00、10.00、13.00mL分别放入5个100mL容量瓶中,各加入TISAB10mL,用去离子水稀释定容,摇匀,即得到氟离子质量浓度分别为0.10、0.40、0.70、1.00、1.30μg·mL-1的标准溶液。
2)标准曲线的绘制
将上述配好的标准溶液分别倒入50mL小塑料烧杯中,将准备好的氟离子选择性电极①和饱和甘汞电极②浸入溶液中③,在电磁搅拌下,读取平衡电位值④。测量的顺序由稀到浓,在转换溶液时,用水冲洗电极,再用滤纸吸去附着溶液。
在半对数坐标纸上作mV-[F-]图,即得标准曲线,或在普通坐标纸上作mV-pF图。
3)试样中氟含量的测定
准确吸取含氟量小于10.0μg·mL-1的水样50.00mL于100mL容量瓶中,加入10mLTISAB,用去离子水稀释定容,摇匀。
将氟离子选择性电极和饱和甘汞电极置于盛有去离子水的小塑料烧杯中,用磁子搅拌溶液以清洗电极,直至所测电位与起始的空白电位值接近时,拿出电极。用滤纸吸干电极表面的水,再插入盛有未知水样的塑料烧杯中,在电磁搅拌下读取平衡电位值E1,根据E1从工作曲线上查得氟含量并计算出水样氟的质量浓度(μg·mL-1)。
3.标准加入法(请思考标准加入法与标准曲线法的应用条件)
(1)准确吸取50.00mL水样于100mL容量瓶中,再准确加入1.00mL100μg·mL-1氟标准溶液、10mLTISAB,并用去离子水稀释定容,摇匀。
(2)将氟离子选择性电极和饱和甘汞电极插入盛有上述溶液的小塑料烧杯中,在电磁搅拌下测其平衡电位值E2,再根据E1和E2计算出原水样中的氟的质量浓度,即
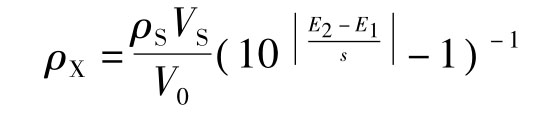
式中0为待测溶液体积S为加入标准溶液的体积,mL;ρS为加入标准溶液的质量浓度,μg·mL-1;s为电极线性响应斜率。
注释
①氟离子选择性电极使用前需用去离子水浸泡活化过夜,或在10-3mol·L-1NaF溶液中浸泡1~2h,再用去离子水洗至空白电位值为300mV左右,方可使用。电极的单晶膜切勿与坚硬物碰擦,晶片上如粘有油污,用脱脂棉依次以酒精、丙酮轻拭,再用去离子水洗净。电极使用后,应清洗至空白电位值,然后浸泡在水中。长久不用时,风干后保存。电极内装有电解质溶液,为防止晶片内附着气泡而使电路不通,在电极使用前,让晶片朝下,轻击电极杆,以排除晶片上可能附着的气泡。
②饱和甘汞电极在使用前应拔去加KCl溶液小口处的橡皮塞,以保持足够的液压差,使KCl溶液只能向外渗出,同时检查内部电极是否已浸于KCl溶液中,否则应补加。电极下端的橡皮套也应取下。饱和甘汞电极使用后,应再将两个橡皮套分别套好,装入电极盒内,防止盐桥液流出。
③安装电极时,两只电极不要彼此接触;电极下端离杯底应有一定的距离,以防止转动的搅拌磁子碰击电极下端。
④在稀溶液中,氟电极响应值达到平衡的时间较长,需等待电位值稳定后再读数。
思考题
(1)标准加入法为什么要加入比欲测组分浓度大很多的标准溶液?
(2)氟电极在使用前应该怎样处理?使用后应该怎样保存?
(3)TISAB溶液包含哪些组分?各组分的作用是什么?
(4)氟离子选择性电极测得的是F-的浓度还是活度?如果要测定F-的浓度,应该怎么办?
(5)测定F-浓度时为什么要控制在pH≈5,pH值过高或过低有什么影响?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















