实验94 易挥发物质摩尔质量的测定
实验目的
用维克托-梅耶(Victor Meyer)法测定乙酸乙酯的摩尔质量,掌握质量、温度、压力、体积测量的基本操作。
实验原理
在温度不太低、压力不太高的条件下,可近似地把实际气体看作理想气体,其状态方程为
![]()
式中:p、V、T、m和M分别为气体的压力、体积、温度、质量和摩尔质量。R为摩尔气体常数。
将一定质量的易挥发液态物质在保持温度(通常较该物质沸点高20~30℃)及压力(通常为大气压力)恒定的容器底部汽化,此蒸气将把容器中与该蒸气同温、同压力和同体积的空气排挤出来,排出的空气在常温常压下不会液化,容易测出它的p、 V、T,从而算出其物质的量,其值与液体蒸气物质的量相等。已知液体的质量m,即可算出被测物质的摩尔质量。
物质在汽化时需防止蒸气扩散至汽化管上部低温区冷凝而使排出空气的体积减少。同理,实验前汽化管中不应含凝结的蒸气。
实验用品
仪器 维克托-梅耶法蒸气密度测定仪;温度计(0~100℃);小玻璃泡;酒精灯;电炉;分析天平等。
实验步骤
(1)按图6-16装好测定装置。将三通活塞6通大气,接通电炉电源,将外管中的盐水加热至沸腾(水中加少量沸石)。
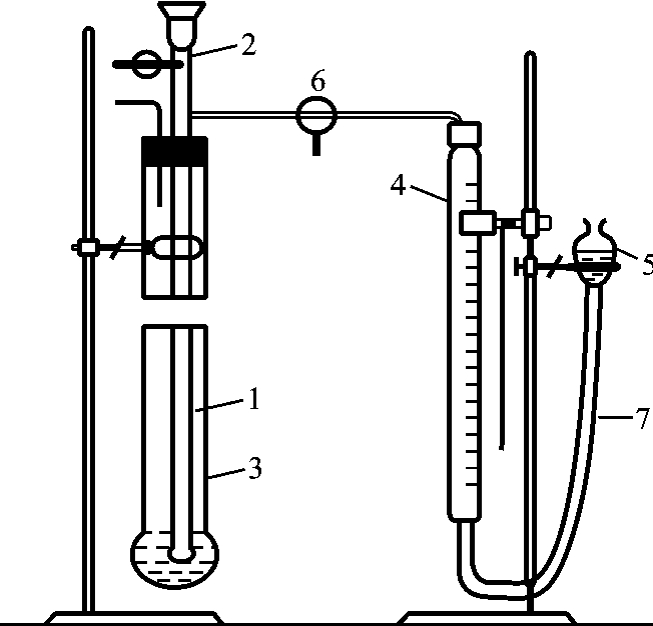
图6-16 维克托-梅耶法蒸气密度测定仪
1—汽化管;2—小玻璃泡;3—外套管;4—量气管;5—水位瓶;6—三通活塞;7—橡皮管
(2)取一干净小玻璃泡在分析天平上精确称量(准确至0.0002g)。将小玻璃泡用酒精灯加热后,迅速将玻璃泡的毛细管端插入待测液体中,玻璃泡冷却后,液体即被吸入(如待测液体为乙酸乙酯,吸入的质量应在0.1~0.2g之间;如为乙醇,则为0.08~0.1。过多或过少都不适宜)。大致称量使质量适合后,于酒精灯上熔封玻璃泡毛细管尖端。然后重新准确称量,两次质量之差即为待测液体的质量。
(3)将小玻璃泡小心地放入汽化管上部的玻璃棒上,塞紧管口塞子,检查体系是否漏气:转动三通活塞,使汽化管与量气管相连,提高或降低水位瓶后观察一段时间,若量气管液面上升或下降一定程度后不再变化,则表明不漏气;若量气管液面不断上升或下降,则表明漏气,应重新检查装置。
(4)确认装置不漏气后,加热使外管水沸腾约5min,检查汽化管内温度是否恒定:转动三通活塞,使量气管与大气相通。将水位瓶慢慢往上提,使量气管与水位瓶的液面平齐,再旋转三通活塞,使汽化管和量气管相连,若管内液面并不上下移动,表明温度已达稳定。
(5)汽化管内温度恒定后,使三通活塞与大气相通,提高水位瓶,使量气管中水面升至顶点附近(注意勿使液体进入横向连接管),然后旋转三通活塞,使内管与量气管相连,保持量气管与水位瓶液面等高,记下此时量气管的读数作为初始体积。轻轻拉长玻璃棒套(注意勿使装置漏气),使玻璃棒外移,小玻璃泡失去支撑落入汽化管的底部而破碎,小泡内部的液体立即汽化而将内管上部空气排入量气管中。移动水位瓶,保持水位瓶与量气管两个水平面等高,至液面不再下降,记下该处读数作为终了体积。并记录靠近量气管的温度及大气压力。
(6)转动三通活塞,通大气,停止加热。将内管取出,倒出碎玻璃,干燥汽化管,赶出残存的液体。
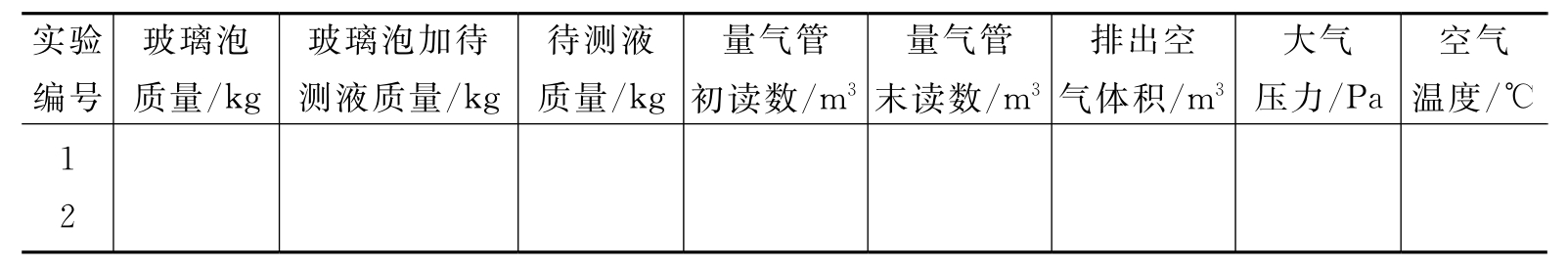
重复以上步骤,再做一次平行实验。将实验数据记录于表6-3中。
表6-3 实验数据记录
实验结果与数据处理
(1)查出在量气管的温度下,水的饱和蒸气压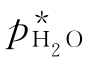 ,求出量气管内空气(不含水蒸气)的分压p:
,求出量气管内空气(不含水蒸气)的分压p:
![]()
(2)根据所测得的V、T、m等数据,利用理想气体状态方程,求出所测物质的摩尔质量。
(3)将实验算得的M与计算式的摩尔质量比较,求出误差。
思考题
(1)汽化管与量气管温度不同,为什么可以通过测量在量气管中被排出气体的V、T来计算汽化管内液体的摩尔质量?
(2)样品太多或太少有什么不好?
(3)每次实验完毕为什么要把内管中样品排净?
(4)汽化管中气体上、下存在温度梯度,会影响实验结果吗?
(5)读量气管读数时为什么水位瓶要与量气管内水面平齐?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















