6.1.2 土颗粒的胶体表面物理化学性质
黏土颗粒的表面包括[3]:硅氧四面体片连接组成的硅氧表面;铝氧八面体片连接组成的表面;层状硅酸盐矿物边面断键形成的,或铁(铝)氧化物和氢氧化物,以及非晶形铁、铝、硅等化合物的―Si―OH或―Al―OH组成的表面。
1.扩散双电层理论
带有电荷的土胶体表面,吸引相邻液相中的反号离子,在土粒周围形成带反号电荷的离子层,它与土粒表面的电荷层一起构成了双电层,即土颗粒表面的双电层。具体为:黏土矿物表面带有负电荷,把黏土放入溶液中,溶液中的阳离子就会被吸附到黏土矿物的表面以保持电中性。由于黏土矿物表面对阳离子的吸附,黏土矿物的阳离子浓度将比主体溶液的阳离子浓度大。同时,由于有阳离子浓度梯度的存在,阳离子就趋向于从黏土矿物表面向主体溶液扩散。结果是黏土矿物表面对阳离子的静电吸引和阳离子自黏土矿物表面向外扩散最终达到平衡。包裹黏土矿物颗粒的这一平衡带具有一定的厚度,这一厚度是扩散的,在这个厚度内阳离子浓度随着离黏土矿物表面距离的增大而减少,直至与主体溶液的阳离子浓度相等。在这个扩散层中,有两个电性电荷层存在,即带有负电荷的黏土矿物表面和紧邻于黏土矿物表面的带正电荷的阳离子扩散层,两者构成了“双电层”。由于扩散层间的静电排斥力,所以黏土矿物颗粒就会相互排斥。随着水分不断减少,结果就增加了水的阳离子浓度。在较大的阳离子浓度下,阳离子自黏土矿物表面向外扩张的趋势变小了,因此扩散层就被压缩。此时扩散层的静电斥力变小,黏土矿物颗粒就可以互相紧密靠近。当靠近到一定程度时,静电引力就会使黏土矿物颗粒靠近,黏土矿物颗粒增大,或絮凝、或聚合,最终紧固在一起。通常,双电层可分成两部分:一部分为接近黏土矿物表面的紧密层——Stern层;留下的一部分为包含一个Gouy-Chapman扩散层。
黏土矿物带电有以下几种可能[4,5]。
(1)黏土矿物形成时附近有镁离子,蒙脱土晶格中的铝离子往往有一部分被二价的镁离子取代。取代结果使黏土晶体带负电,由于晶格空间是有限的,不可能在晶格中多装一个一价正离子来补足,于是只好在晶格表面吸附正离子来维持黏土的电中性。所以晶格取代使黏土的晶层间及表面上会吸附有正离子,而这种正离子在水中会水化而稍离开表面,致使黏土颗粒带负电。
(2)次生的二氧化硅表面与水作用形成一层偏硅酸(H2 SiO3),后者在水中能解离为H+和SiO2,晶体不能分离,故表面带负电荷。
(3)在扁平的黏土矿物颗粒边缘处是晶体破碎的断口,断口处破坏了硅(或铝)和氧(或氢氧)之间的化学键,产生不饱和的过剩电荷,断口两边的电荷正负号正好相反。
(4)选择性的吸附作用,如方解石(CaCO3)置于NaCO3水溶液中,则方解石吸附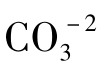 而带负电。
而带负电。
土中最活跃的部分一般是次生矿物,它们构成了土中的黏土颗粒,存在有大量的表面自由能。土颗粒的表面特性,也就是土和结合料之间相互作用过程的倾向性,基本取决于黏土的矿物成分。黏土矿物表面常常带有未补偿的电荷,它们被处在游离状态的离子所饱和。当土中的孔隙被水充满时,所吸附的离子部分地处在液相中,能与对矿物表面具有较大亲和力的离子进行当量吸附交换。所以土颗粒吸水的根本原因是由于矿物表面存在未补偿的电荷,主要是未补偿的氧原子的羟基团。水对土的膨胀作用分为两个阶段:水合能引起的膨胀阶段与双电层的排斥引起的渗透膨胀阶段。前者是干黏粒表面吸附单层水分子,有4个单层水分子进入蒙脱石晶层间使其体积增加一倍;在黏粒表面有相当于4个单层水分子后,双电层的排斥力成为黏粒之间的主要斥力,相应的膨胀即为渗透膨胀。可见双电层电位在土的膨胀与收缩中起着极为重要的作用。
土中的化学反应主要发生于胶体表面与水溶液之间的界面或与之相邻的溶液之间。土中胶体颗粒所带的表面电荷是土具有一系列化学、物理化学性质的根本原因。土颗粒表面电荷数量决定着土颗粒所能吸附的离子数量,而由土颗粒表面电荷数量与土颗粒的表面积所确定的表面电荷密度,则影响着对这些离子的吸附强度。水与土粒表面未补偿的原子相互作用形成水分子初始吸附层,然后逐渐加厚。因此减薄土颗粒双电层厚度是降低土粒吸湿性的一种有效途径。
2.黏土矿物的水化作用
阳离子与其伴生水分子使得阳离子有效半径比其没有伴生水分子时要大得多。水化阳离子的半径取决于阳离子的表面电荷密度(阳离子的表面电荷密度等于其电荷数被其未水化离子半径所除的值)。因此,二价阳离子一般具有比一价阳离子大得多的水化半径。在给定价态的阳离子系列中,阳离子的选择吸附与水化半径有关,水化半径越小的阳离子,靠近黏土矿物颗粒表面的程度越高,即水化半径越小,越靠近黏土矿物颗粒表面。部分阳离子的结晶半径和水化半径见表6.1。
3.黏土矿物的吸附性
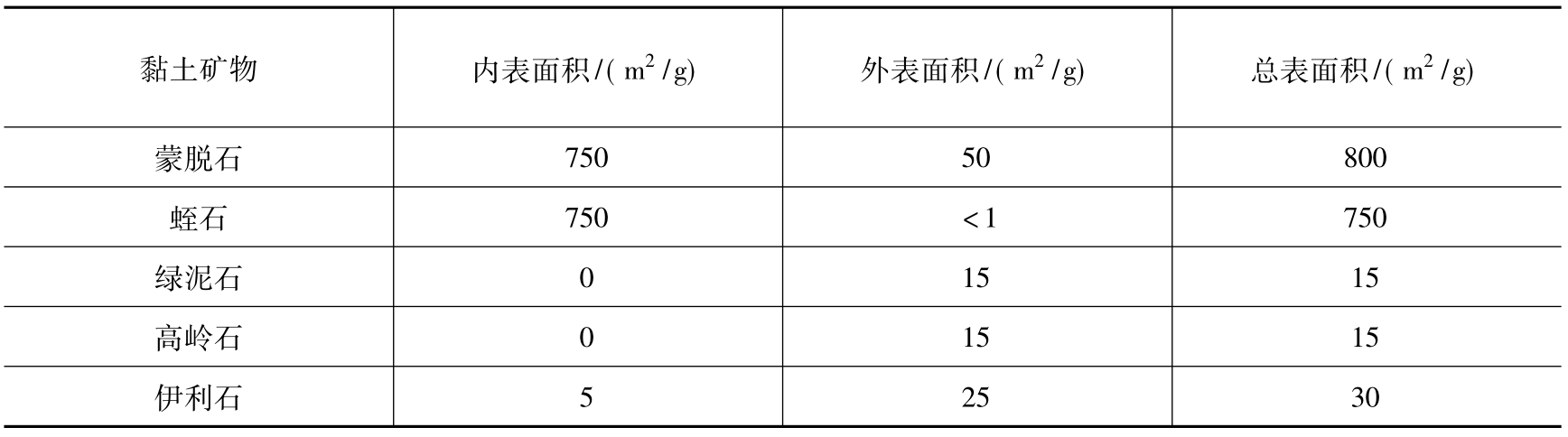
因为黏土矿物的板、片状结晶习性和一些黏土矿物具有大的内表面积,所以黏土矿物的表面积均很大。部分黏土矿物的内表面积、外表面积和总面积见表6.2。
表面积是影响黏土吸附性的重要因素。按照引起吸附的原因不同可以分为三类,即物理吸附、化学吸附和离子交换吸附。
表6.1 部分阳离子的结晶半径和水化半径
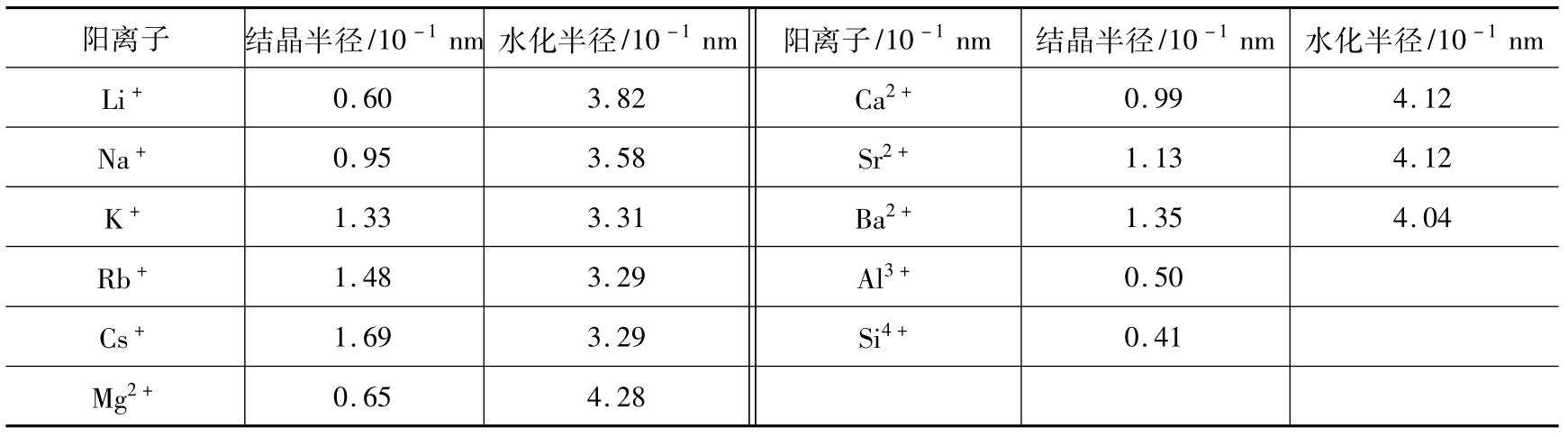
表6.2 部分黏土矿物的内表面积、外表面积和总面积
(1)物理吸附是指由吸附剂与吸附质之间的分子间引力而产生的吸附,由氢键产生的吸附也属于物理吸附。物理吸附是可逆的,吸附速度和解吸速度在一定的温度、浓度条件下呈动态平衡。产生物理吸附的原因是由于黏土矿物的表面分子具有表面能。
(2)化学吸附是指由吸附剂与吸附质之间的化学键力而产生的吸附。阴离子聚合物可以靠化学键吸附在黏土矿物表面上,吸附方式可以有两种情形:①黏土矿物晶体带正电荷,阴离子基团可以靠静电引力吸附在黏土矿物的边面上;②介质中有中性电介质存在时,无机阳离子可以在黏土矿物和阴离子型聚合物之间起“桥接”作用,使髙聚物吸附在黏土矿物的表面上。
(3)离子交换吸附是指因为黏土矿物通常带有不饱和电荷,根据电中性原理,必定会有等量的异号离子吸附在黏土表面上以达到电性平衡。通常,吸附在黏土矿物表面上的离子可以和溶液中的同号离子发生交换作用,这种作用即为离子交换作用。最常见的与黏土矿物结合的交换性离子是Ca2+、Mg2+、H+、K+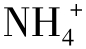 、Na+和Al3+等阳离子,及
、Na+和Al3+等阳离子,及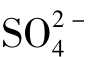 、Cl-和
、Cl-和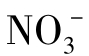 等阴离子,根据交换性离子的电性不同,可以把交换性吸附分为阳离子交换性吸附和阴离子交换性吸附两种。
等阴离子,根据交换性离子的电性不同,可以把交换性吸附分为阳离子交换性吸附和阴离子交换性吸附两种。
影响阳离子可逆交换性吸附的因素有以下种类。
(1)离子价数对吸附强弱的影响。一般情况下,在溶液中离子浓度相差不大时,离子价态越高,与黏土表面的吸附力越强,即交换到黏土表面上的能力越强;反之,如果已经吸附到黏土表面上,则价态越高的离子,越难从黏土表面上被交换下来。
(2)离子半径对吸附强弱的影响。当价态相同的不同离子在溶液中的浓度相近时,离子半径小的,水化半径大,离子中心离黏土表面远,吸附弱;反之,离子半径大的,水化半径小,离子中心离黏土表面近,吸附强。
(3)离子浓度对吸附强弱的影响。离子浓度对吸附强弱的影响符合质量作用定律,即离子交换受每一相中的不同离子的相对浓度的制约。
(4)介质的影响。碱性介质的交换量比酸性介质的交换量髙,这主要与黏土矿物端面电荷和黏土矿物的表面电荷电性有关。
(5)粒度的影响。黏土矿物样品研磨后颗粒变细,端面破键增多,阳离子交换容量稍显增加,但长时间的研磨容易引起黏土矿物晶格破坏,使交换量减少直到交换作用消失,成为无定形凝胶状物质。
(6)温度的影响。温度对交换容量有一定的影响,适当的温度可加大扩散系数,加大交换作用,但温度过高也会使黏土矿物的溶解度增大,交换量反而会下降。
影响黏土矿物阳离子交换容量大小的因素有3种,即黏土矿物的类型、黏土矿物的分散程度和溶液的酸碱性条件。常见阳离子交换容量为:蒙脱石70~130 mmol/100 g,伊利石10~40 mmol/100 g,高岭石3~15 mmol/100 g。
同阳离子交换性吸附一样,阴离子交换性吸附的特点也是等电量交换。阴离子交换具有以下规律。
(1)与表面羟基结合的Al3+、Fe3+,将吸附阴离子。
(2)阴离子吸附受溶液的pH值影响,低pH值时有最大的吸附。
(3)阴离子吸附性大小顺序为: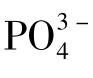 >
>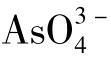 >
>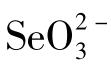 >
>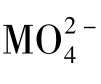 >
>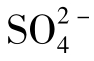 >F->Cl->
>F->Cl->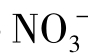 。
。
(4)其他类型的阴离子存在,将引起吸附位置的竞争;有时像Ca2+、Al3+这样一些交换性阳离子的存在可以导致不溶产物的形成。
常见阴离子交换容量为:蒙脱石20~30 mmol/100 g,伊利石4~17 mmol/100 g,高岭石7~20 mmol/100 g,绿泥石5~20 mmol/100 g,蛭石4 mmol/100 g。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















