10.3.2 SOR催化作用的特点
滴定结果显示,SOR中心Ⅱ(Fe2+)的标准还原电位是+201mV,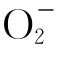 还原为H2O2的相应值为+890mV,可见SOR能够还原
还原为H2O2的相应值为+890mV,可见SOR能够还原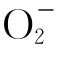 顺磁共振和可见光谱,结果证明,SOR的中心Ⅰ的Fe2+还原
顺磁共振和可见光谱,结果证明,SOR的中心Ⅰ的Fe2+还原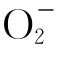 后自身被氧化为Fe3+,该反应的速率常数在108~109L·mol-1·s-1,与Cu,Zn-SOD和Fe-SOD歧化
后自身被氧化为Fe3+,该反应的速率常数在108~109L·mol-1·s-1,与Cu,Zn-SOD和Fe-SOD歧化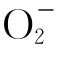 的速率常数相当,而远大于
的速率常数相当,而远大于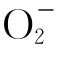 自发歧化、
自发歧化、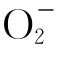 还原细胞色素c以及H2O2氧化中心Ⅱ(Fe2+)的速率常数(分别为5×105、2.6×105和45或120L·mol-1·s-1)。与
还原细胞色素c以及H2O2氧化中心Ⅱ(Fe2+)的速率常数(分别为5×105、2.6×105和45或120L·mol-1·s-1)。与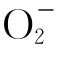 相比O2仅少一个电子,但O2却不能氧化SOR中心Ⅱ的Fe2+。这些说明SOR还原
相比O2仅少一个电子,但O2却不能氧化SOR中心Ⅱ的Fe2+。这些说明SOR还原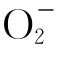 是高效的,具有特异性。
是高效的,具有特异性。
在黄嘌呤、黄嘌呤氧化酶的细胞色素c(过氧化氢酶)的组成的反应体系中,分别加入SOR和SOD,均能够抑制细胞色素c的还原。但SOR在加入后,细胞色素c的还原在开始一段时间出现停滞期(A550不上升),随后升高;并且随着加入量增大该停滞期也延长,A550升高的幅度也减小;而当SOR与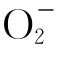 预先孵育或被氧化后再加入则不出现停滞期,说明停滞期的出现是由于SOR还原
预先孵育或被氧化后再加入则不出现停滞期,说明停滞期的出现是由于SOR还原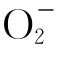 的结果。在上述反应体系中的细胞色素c被乙酰化后,SOD的作用基本不受影响,SOR却几乎不再能抑制细胞色素c的还原,表明SOR还原
的结果。在上述反应体系中的细胞色素c被乙酰化后,SOD的作用基本不受影响,SOR却几乎不再能抑制细胞色素c的还原,表明SOR还原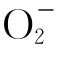 需要与细胞色素c直接接触。若用还原型红氧还蛋白取代该反应体系中的细胞色素c,加入SOD抑制其氧化,而加入SOR则加速其氧化,说明SOR催化
需要与细胞色素c直接接触。若用还原型红氧还蛋白取代该反应体系中的细胞色素c,加入SOD抑制其氧化,而加入SOR则加速其氧化,说明SOR催化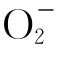 还原的同时有还原型红氧还蛋白的氧化发生。还原型红氧还蛋白可能是还原
还原的同时有还原型红氧还蛋白的氧化发生。还原型红氧还蛋白可能是还原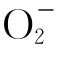 所需电子的供体。大肠杆菌胞浆或细胞膜组分加入NADH或NADPH时,能够还原氧化型SOR。说明大肠杆菌存在依赖于NAD(P)H的还原酶系统,可还原被氧化的SOR,从而使SOR能够重复使用。
所需电子的供体。大肠杆菌胞浆或细胞膜组分加入NADH或NADPH时,能够还原氧化型SOR。说明大肠杆菌存在依赖于NAD(P)H的还原酶系统,可还原被氧化的SOR,从而使SOR能够重复使用。
用SOR转化SOD大肠杆菌突变体后,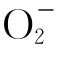 浓度下降,并且恢复有氧条件下的生长。普通脱硫弧菌同时具有SOR和SOD,缺失SOR时厌氧生长不受影响,若有氧暴露或在培养基中加入白草枯(paraquat)产生
浓度下降,并且恢复有氧条件下的生长。普通脱硫弧菌同时具有SOR和SOD,缺失SOR时厌氧生长不受影响,若有氧暴露或在培养基中加入白草枯(paraquat)产生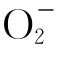 ,则厌氧生长明显受到抑制;而在相同条件下缺失SOD时生长抑制较轻,野生型普通脱硫弧菌随着有氧暴露时间的增加,细胞内的SOR蛋白逐渐减少。这些说明,在有氧环境中,SOR是普通脱硫弧菌清除
,则厌氧生长明显受到抑制;而在相同条件下缺失SOD时生长抑制较轻,野生型普通脱硫弧菌随着有氧暴露时间的增加,细胞内的SOR蛋白逐渐减少。这些说明,在有氧环境中,SOR是普通脱硫弧菌清除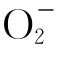 抵御氧毒性的主要机制。
抵御氧毒性的主要机制。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















