实验技术十三 乙酰乙酸乙酯的制备
【实验目的】
(1)了解乙酰乙酸乙酯的制备原理和方法。
(2)掌握无水操作及减压蒸馏操作。
【仪器及药品】
1.仪器
减压油泵、标准磨口仪。
2.药品
乙酸乙酯、二甲苯、金属钠、50%醋酸、饱和氯化钠溶液、无水硫酸钠。
【实验原理】
含α-活泼氢的酯在强碱性试剂(如金属钠、NaNH2、三苯甲基钠或格氏试剂)存在下,能与另一分子酯发生Claisen酯缩合反应,生成β-羰基酸酯。乙酰乙酸乙酯就是通过这一反应制备的。虽然反应中使用金属钠作缩合试剂,但真正的催化剂是钠与乙酸乙酯中残留的少量乙醇作用产生的乙醇钠。其反应方程式如下所示。

乙酰乙酸乙酯与其烯醇式是互变异构(或动态异构)现象的一个典型例子,它们是酮式和烯醇式平衡的混合物,在室温时含92%的酮式和8%的烯醇式。单个异构体具有不同的性质并能分离为纯态,但在微量酸碱催化下,迅速转化为二者的平衡混合物。
【实验装置】
见图5-10。

图5-10 乙酰乙酸乙酯制备实验装置
(a)无水干燥回流装置;(b)减压蒸馏装置
【实验步骤】
1.熔钠
在表面皿上迅速将金属钠切成薄片,立即放入带干燥管的回流瓶中(内装12.5mL二甲苯),加热熔之。塞住瓶口振摇使之成为钠珠。回收二甲苯。
2.加酯回流
迅速放入27.5mL乙酸乙酯,反应开始。若慢可温热。回流1.5h至金属钠基本消失,得橘红色溶液,有时析出黄白色沉淀(均为烯醇盐)。
3.酸化
加50%醋酸,至反应液呈弱酸性(固体溶完)。
4.分液
反应液转入分液漏斗,加等体积饱和氯化钠溶液,振摇,静置。
5.干燥
分出乙酰乙酸乙酯层,用无水硫酸钠干燥。
6.精馏
水浴蒸去乙酸乙酯,剩余物移至25mL克氏蒸馏瓶,减压蒸馏,收集馏分。
【注意事项】
(1)金属钠遇水即燃烧、爆炸,故使用时应严格防止与水接触,在称量或切片过程中应当迅速,以免空气中水汽侵蚀或被氧化。
(2)用醋酸中和后,如尚有少量固体未溶解,可加少许水使溶解,但应避免加入过量的醋酸,否则会增加酯在水中的溶解度。
(3)乙酰乙酸乙酯在常压蒸馏时,很易分解而降低产量。
【考核评分】
见表5-4。
表5-4 乙酰乙酸乙酯的制备操作考核评分表
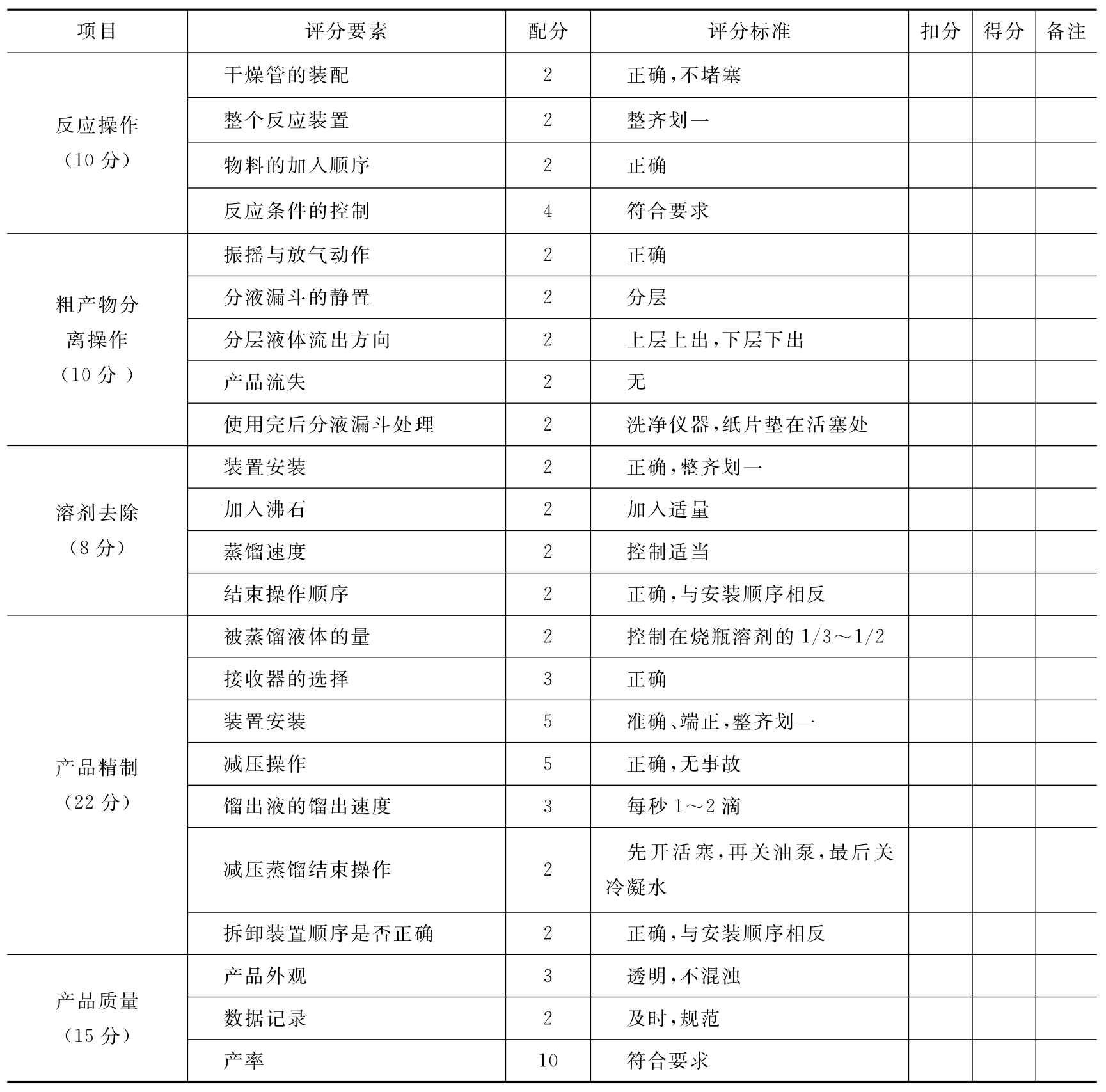
续表

免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















