S.Karim1,2 M.Aoyama1著
刘毓芳3 吴云彬4 赵瑞华3 张彩凤4 译
(1 弘前大学农业和生命科学学院 弘前 日本 036-8561 2 岩手大学农业科学联合研究院 盛冈 日本 020-8550 3 晋中学院化学化工学院 晋中 山西 0306002 4 太原师范学院化学系 太原 山西 030006)Separation of Humic Acid Constituents by Polyacrylamide Gel Electrophoresis in the Presence of Concentrated Urea Using a Preparative Electrophoresis System
摘 要:本实验采用制备型电泳体系在高浓度的尿素存在下进行聚丙烯酰胺凝胶电泳分离水溶性腐植酸中的不同成分。在聚丙烯酰胺凝胶电泳中,根据水溶性腐植酸中深色成分分子大小的不同能够将它们彼此分离开来,同时还可以通过酸沉淀的方法将这些深色物质重新回收。水溶性腐植酸中大部分的荧光物质分子尺寸都很小,这使得它们可以溶于酸,并且被酸溶解的荧光物质可以通过吸附在DAX-8树脂上而重新获得。但是,水溶性腐植酸中的非荧光物质则会在电泳过程中丢失。而那些被认为是小分子的荧光物质则会通过氢键的断裂和7 M尿素的疏水作用得到分离。漫反射傅里叶变换红外光谱的测量结果表明腐植酸中不同成分的化学性质是不同的。而实验结果表明在高浓度尿素存在下聚丙烯酰胺凝胶电泳是分离和收集水溶性腐植酸中各组分的一种很有用的方法。
关键词:荧光 腐植酸 腐殖化程度 制备电泳 聚丙烯酰胺凝胶电泳(PAGE) 尿素
S.Karim1,2, M.Aoyama1 write
Liu Yufang3, Wu Yunbin4 Zhao Ruihua3, Zhang Caifeng4 translate
(1 Faculty of Agriculture and Life Sciences, Hirosaki University, Hirosaki 036-8561, Japan 2 The United Graduate School of Agricultural Sciences, Iwate University, Morioka 020-8550, Japan 3 Department of Chemistry and Chemical engineering, Jinzhong University, Jinzhong, 0306002. 4 Department of Chemistry, Taiyuan Normal University, Taiyuan, 030006)
Abstract:To separate Humic Acid(HAs)into their constituents, Polyacrylamide Gel Electrophoresis(PAGE)was carried out in the presence of 7 M urea using a preparative electrophoresis system.Upon PAGE the dark-colored constituents of HAs were separated by their molecular sizes and recovered by precipitation with acid.Considerable parts of the fluorescent constituents of HAs with the lowest molecular size were rendered soluble in acid and the acid soluble fluorescent constituents were recovered by adsorption onto DAX-8 resin.However, the colorless constituents of HAs were lost during the electrophoresis.These constituents were considered as the low molecular sizes constituents separated due to disruption of the hydrogen bonding and hydrophobic interaction by 7 M urea.The measurement of diffuse reflection infrared Fourier transform spectra indicated that the chemical properties of HA constituents were different from each other.The results show that preparative PAGE in the presence of concentrated urea is a useful method for fractionating and collecting the constituents of HAs.
Key words: fluorescence; humic acid; humification degree; preparative electrophoresis; polyacrylamide gel electrophoresis(PAGE); urea
最新研究表明腐殖质是由一系列相对较小的分子结合而成的一种不均匀的物质,它来自于已死生物体的分解和降解,并且通过弱的化学作用力如氢键和疏水键连接在一起。自从知道高浓度尿素可以使腐殖质中的氢键和疏水键断裂后,在高浓度的尿素存在下进行聚丙烯酰胺凝胶电泳就成为分离水溶性腐植酸成分的一种有效方法。而通常情况下采用的是垂直板式聚丙烯酰胺凝胶电泳。但一般却很难收集到足够量的样品来描述被分离出的成分的性质。因此,在这里我们采用制备型电泳体系在高浓度尿素的存在下进行聚丙烯酰胺凝胶电泳分离水溶性腐植酸中的不同成分。
1 材料和方法
从新成土(Fujisaki 土壤)和火山灰土(Chitose土壤)中提取腐植酸备用。
采用Nativen制备电泳体系进行聚丙烯酰胺凝胶电泳,制备电泳体系由以下三部分组成—上凝胶柱、下凝胶柱和位于两柱之间的收集部分。对水溶性腐植酸进行电泳时,上下凝胶柱均用含7 M尿素的6%的聚丙烯酰胺凝胶灌注,而中间的收集部分则用pH=8.8的含10%蔗糖的硼酸盐缓冲溶液作为回收液。将腐植酸样品溶于含7 M尿素(浓度为20 mg/mL)的pH=8.3的Tris-硼酸缓冲液中,并取出1 mL加入到上凝胶柱(长50 mm,直径为16 mm)中。然后在15 mA的恒定电流下进行电泳。每两分钟用馏分收集器将回收液收集到2 mL的聚丙烯管中,而刚刚收集过回收液的部分则要继续灌注新的回收液,以上过程要重复进行60次。被收集到的回收液总共可以分为8部分,根据它们迁移率的递减顺序依次标为F1~F8。而残留在上凝胶柱中的水溶性腐植酸则用0.1 M的氢氧化钠溶液提取,并标为F9。然后用盐酸对各部分进行酸化得到深色沉淀物,将这些沉淀用稀盐酸重复清洗四次后用纯水洗涤,最后低温干燥。用盐酸进行沉淀时,F1~F3的上清液是棕色的,因此,F1~F3的上清液中这些有颜色的组分在凝胶柱中会吸附到DAX-8树脂上,接着可以用稀盐酸和纯水对其进行洗涤。而后将吸附在DAX-8树脂上的棕色沉淀用0.1 M的氢氧化钠溶液进行洗脱,得到的氢氧化钠洗脱液则需立即通过阳离子(由氢离子组成)交换树脂。紧接着将交换所得的氢离子饱和溶液倒入旋转蒸发器中浓缩至适当的体积后进行低温干燥。最后将F2和F3的悬浮液混合起来以待下一步分析。
将低温干燥组分的一部分溶于0.1 M的氢氧化钠溶液中,然后进行有机碳含量分析并测量其在400 nm和600 nm处的吸光度,计算A600/C和A400/C的值,这里的C指的是碳的浓度(mg/mL),A400 和A600指的是400nm和600nm处的吸光度值。
用高效排阻色谱(HPSEC)将低温干燥样品在280 nm紫外光下进行吸收检测,在Ex=460 nm和Em=520 nm下进行荧光探测,然后再用漫反射傅里叶变换红外光谱对其进行测量。
2 结果与讨论
F1~F3中的快速迁移部分在蓝光(470 nm处)下显现出绿色的荧光,而且迁移速度越快,荧光越强(图1),一般来说Chitose土壤中腐植酸的绿色荧光强度要比Fujisaki土壤中的腐植酸的绿色荧光强度强。

图1 在蓝光下6~12号收集管中回收液被观察到的绿色荧光(Chitose土壤中的腐植酸)
Fig.1 Green fluorescence observed for the recovery solutions collected in the tubes No.6-12 under blue light(Chitose HA)
注:6~12管中的组分组合成F1部分
图1(Chitose土壤中的腐植酸)显示的是在蓝光下No.6~12管中收集的回收液,它们都可观察到绿色荧光, No.6~12管中的组分则一起组成了F1部分。
有机碳含量的分析表明F1中的大多数组分用盐酸酸化时不会被沉淀下来(图2),而在F2、F3中用盐酸酸化不产生沉淀的部分所占的比例比F1中的小。Fujisaki腐植酸中的成分主要分布在F5~F9之间,而Chitose腐植酸中的成分则主要分布在F2~F7之间。电泳部分的HPSEC表明在聚丙烯酰胺凝胶电泳中水溶性腐植酸中的各组分能够得到分离主要是因为它们的分子大小不同,而一般来说,Fujisaki腐植酸中深色组分的分子要比Chitose腐植酸中深色组分的分子大。
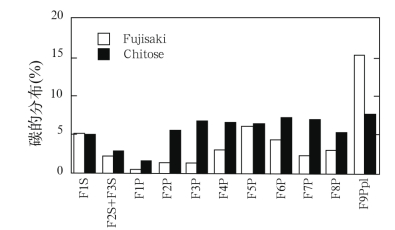
图2 电泳各馏分中碳的分布
Fig.2 Carbon distribution among the electrophoretic fractions
注:S:上清液;P:沉淀物。
HPSEC的荧光探测结果表明荧光探测峰值的位置与洗脱所用的洗脱液的体积有关,而与是何种组分无关。荧光探测峰最强的是F1的上清液,然后是F1的沉淀物和F2、F3的上清液,相反的,F4~F9的沉淀物荧光探测峰值却很弱,因此,可以判断,大部分的荧光物质都集中在F1的上清液中。一般来说Chitose腐植酸的荧光探测峰值要比Fujisaki腐植酸的荧光探测峰值强,而这一点和将提取出的物质在蓝光下观察所得的结果是一致的。
相比于未进行分离的腐植酸样品,F1~F8组分呈现出更高的A600/C值和更低的log(A400/ A600)数值(图3)。而A600/C值的增加和log(A400/ A600)值的减小均表明了腐植酸中腐殖化程度的增加。观察进行过电泳的部分,其腐殖化程度有所增加,这表明在高浓度的尿素存在下,对水溶性腐植酸进行凝胶电泳时,腐殖化程度低的荧光组分会从深色沉淀中分离出来。因此,F1、F2、F3的上清液的腐殖化程度要比未进行分离的腐植酸样品低。而这个事实又表明被分离出来的腐殖化程度相对较低的小分子组分可以溶于酸。另外,检测到在上凝胶柱中残留的腐植酸组分(F9)的腐殖化程度也较低。
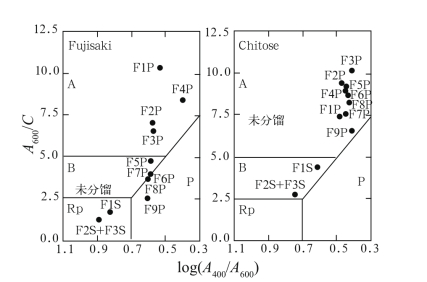
图3 已分馏和未分馏腐植酸的A600/C~log(A400/A600)图
Fig.3 log(A400/A600)versus A600/C diagram of fractionated and unfractionated HAs
注:S:上清液;P:沉淀物。
对Fujisaki腐植酸来说有机碳的回收率达45%,而对Chitose腐植酸来说有机碳的回收率为63%,低的碳回收率表明在电泳时腐植酸中的相当一部分碳都丢失了。Piccolo指出在高浓度的尿素存在下水溶性腐植酸中分子较小的无色组分可以通过HPSEC被分离出来。因此,通过电泳从水溶性腐植酸中分离出来的组分可以认为其是分子较小的无色物质。而傅里叶变换红外光谱的测量结果表明腐植酸中各组分的化学性质是不同的,对Chitose腐植酸来说,它的F1~F3上清液中所含的羧基类物质较多,而对Fujisaki腐植酸来说,除有羧基类物质外,还有更多的脂肪类和多糖类物质。在F1~F9的沉淀物中,随着分子的增大,它们当中羧基类物质的含量会减少, 而蛋白质、脂质和糖类物质的含量会增加。将电泳过的样品和未分离的腐植酸样品都通过红外光谱,再将所得的结果进行比较可知,在聚丙烯酰胺凝胶电泳中,水溶性腐植酸中的芳香类成分都丢失了。
因此,在高浓度尿素的存在下采用制备型电泳体系进行聚丙烯酰胺凝胶电泳是分离水溶性腐植酸成分的一种很有用的方法,但是腐植酸中所含有的各种成分的化学性质则需要更详尽的研究。
参考文献(略)
译自:Function of Natural Organic Matter in Changing Environment,2011,75~77。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















