【ICD-10编码】 E76.301
黏多糖贮积症(mucopolysaccharidosis,MPS)是一组由于溶酶体内酸性水解酶缺乏造成酸性黏多糖分子不能降解的溶酶体贮积病,根据酶缺陷的种类及临床表现不同,临床上分为Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅵ、Ⅵ及Ⅸ共7型,涉及11种水解酶,其中任何一种酶缺陷都会造成黏多糖(glycosaminoglycan,GAG)的分解障碍而沉积在溶酶体内,导致细胞及脏器功能损伤,尿黏多糖排出增多。除Ⅱ型为Ⅹ-连锁隐性遗传外,其余均为常染色体隐性遗传。黏多糖贮积症总体发病率约1/2 5000,其中,以Ⅱ型及ⅣA型多见,Ⅰ型及Ⅵ型次之,Ⅶ及Ⅸ型罕见。随着酶替代疗法和造血干细胞移植的逐步开展,黏多糖贮积症成为可治疗的遗传病,早期诊断和早期干预治疗是改善预后的关键。
【病因】
黏多糖贮积症属于单基因遗传病,基因缺陷导致酶的缺陷,引起黏多糖不能降解积聚在细胞溶酶体内,黏多糖在各系统器官内累积导致了这些器官的病理改变和临床症状。
【临床表现】
绝大多数患儿出生时正常,常在1岁左右发病,逐渐出现生长迟缓,骨骼、关节、面容等改变,进行性加重,常累及多个系统。Ⅰ、Ⅱ、Ⅵ、Ⅶ型黏多糖贮积症外貌较明显,主要表现为矮小、面容丑陋粗糙,关节活动受限、爪形手、脊柱后凸或侧弯、膝外翻等。ⅣA型患儿以矮小、严重骨骼畸形、鸡胸、关节松弛为主,常合并有寰椎关节不稳定及颈髓受压表现。Ⅶ型可表现为非免疫性胎儿水肿,外周血白细胞胞质Alder-Reilly颗粒。Ⅲ型又分为A、B、C、D 4个亚型,以A、B亚型多见,常于2—6岁起病,以进行性神经系统退行性变为特征,伴轻度的黏多糖贮积症外貌,轻型者可仅有精神行为异常。Ⅵ型及ⅣA型患儿智力正常。黏多糖贮积症患儿常有角膜浑浊、肝脾大、疝、反复呼吸道感染等,晚期常合并梗阻性呼吸困难及慢性心脏瓣膜病等。
【辅助检查】
1.X线检查:包括脊柱正侧位X线片、胸部X线片、髋关节正位X线片、单侧长骨X线片、颅骨X线片。具有特征性的改变有骨质疏松,颅骨增大,蝶鞍浅长,脊柱后凸、脊柱侧弯,椎体呈楔形,胸、腰椎椎体前下缘呈鱼唇样前凸,肋骨的脊柱端细小而胸骨变宽,呈飘带状,尺、桡骨粗短,尺、桡骨关节面呈“V”形,掌骨基底变尖,指骨远端窄圆。
2.心脏超声检查:常见瓣膜病。
3.颈椎、头颅、肝脾MRI检查(必要时)。
4.尿黏多糖(GAG)定量:采用1,9-二甲基亚甲蓝比色法定量测定尿GAG,并计算尿GAG/Cr(mg/mmol)比值,正常人尿GAG<70mg/L,GAG/Cr比值随年龄增长,快速下降。黏多糖贮积症患者尿GAG/Cr比值与同龄儿比较明显增高,仅少数ⅣA型患者尿GAG排泄基本正常。
5.尿黏多糖电泳:分双向醋酸纤维薄膜电泳及单向琼脂糖凝胶电泳,可协助分型诊断。
6.酶活性测定:采用底物-荧光分析法检测外周血白细胞或培养的成纤维细胞酶活性可明确诊断,患者缺陷酶活性常仅及正常人的1%~10%。
7.基因突变分析:主要用于遗传咨询及产前诊断,已可用于轻型疑难病例的确诊。
【诊断】
根据临床表现和辅助检查便可确诊。
【鉴别诊断】
1.各型黏多糖贮积症的鉴别诊断 常见黏多糖贮积症的缺陷酶、基因及临床表现见表5-5。
2.先天性甲状腺功能减低症 面容容易与黏多糖贮积症ⅠH型混淆,但该病一般无胸廓及脊柱畸形,无肝脾大,有骨龄落后,进行甲状腺功能检查可鉴别。
3.软骨发育不全 表现为矮小、头大、前额突出、鼻梁扁平,与黏多糖贮积症相似,但前者躯干长,四肢短,智力正常,X线检查有特征性表现。
4.其他 某些疾病临床表现似黏多糖贮积症,但尿黏多糖定量阴性者,应注意黏脂病、寡糖病(岩藻糖病、甘露糖病、神经节苷脂病等),可进行相应的酶学检查鉴别。
【治疗】
1.一般治疗
(1)护理:保持呼吸道通畅,防治感染。
(2)营养管理:由护士对患儿的营养状况进行初始评估,若有营养不良的风险,护士向主管医师报告后通知营养科医师会诊,临床营养医师完成营养专业评估,与主管医师、患者、家属及其他与患者饮食营养服务的有关人员共同制订营养治疗方案,按照已制订的营养治疗方案对患者进行营养治疗,同时进行与营养治疗相关的健康教育。
(3)心理治疗:关心体贴患儿,向家属讲解疾病的知识,解除其思想顾虑,积极配合治疗护理工作。
表5-5 常见黏多糖贮积症的缺陷酶、基因及临床特征
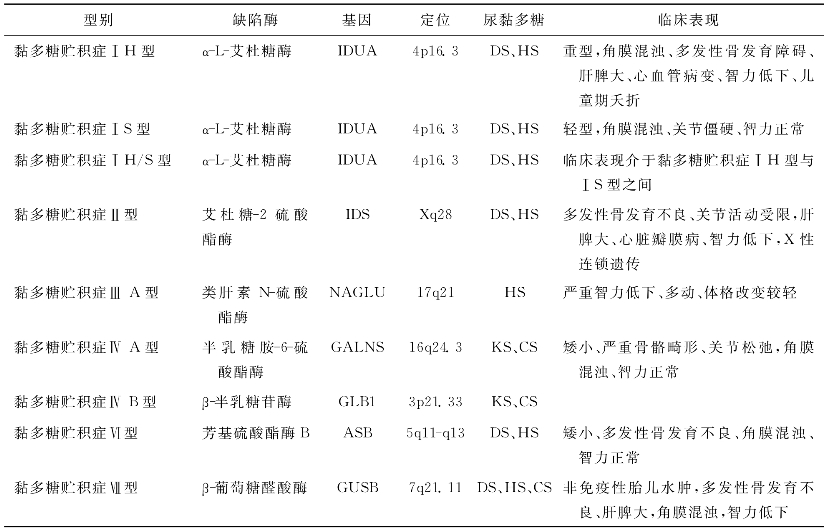
DS.硫酸皮肤素;HS.硫酸类肝素;CS.硫酸软骨素;KS.硫酸角质素
2.酶替代治疗 目前黏多糖贮积症Ⅰ型、Ⅱ型、Ⅵ型可进行酶替代治疗。Ⅰ型,rhIDU(Alaronidase)100U/kg;Ⅱ型,rh Idursulfase(Elaprase?)单次剂量为0.5mg/kg;Ⅵ型,rh ASB(Naglazyme?)单次剂量为1.0mg/kg,分别加入生理盐水中缓慢静脉滴注,每周1次。治疗3~6个月,肝、脾体积缩小,6min步行试验、3min爬楼梯试验改善,尿GAG接近正常水平。黏多糖贮积症ⅠH型患儿进行造血干细胞移植前、后辅助酶替代治疗,可提高移植成功率及疗效。
3.造血干细胞移植 黏多糖贮积症ⅠH型、Ⅵ型、Ⅶ型可进行造血干细胞移植,包括同胞骨髓移植、非血缘相关脐血移植,一般2岁前进行移植治疗,预后较好。
4.其他治疗
(1)对症支持治疗:多学科联合管理,改善黏多糖贮积症患者生活质量。建议由遗传代谢科牵头,联合普外科(疝修补)、骨外科(骨关节手术)、神经外科(脑积水分流术)、耳鼻喉科(睡眠障碍、腺样体、扁桃体肥大等)、麻醉科(呼吸道管理)、眼科、造血干细胞移植及神经康复科等,组成黏多糖贮积症专家队伍,规范临床诊疗工作。
(2)底物合成减少治疗、小分子伴侣治疗和基因治疗,尚处于研究阶段。
【并发症及处理】
1.梗阻性呼吸困难 因黏多糖分子沉积在呼吸道,黏多糖贮积症患儿常合并不同程度的呼吸道梗阻,早期表现为睡眠呼吸暂停,后期常合并慢性心肺功能衰竭。治疗原则:①合并感染时积极抗感染治疗;②合并腺样体及扁桃体肥大时可考虑手术摘除术;③合并睡眠呼吸障碍者给予面罩吸氧或正压通气治疗。
2.寰枢关节发育不良 以ⅣA型、Ⅵ型黏多糖贮积症患者多见,可出现寰枢关节不稳定综合征,严重时可致高位截瘫,可选择预防性颈椎C1、C2融合术。
【分级及诊治指引】
黏多糖贮积症分级及诊治指引见表5-6。
表5-6 黏多糖贮积症分级及诊治指引

【入院标准】
1.出现并发症:心肺功能不全、寰枢关节不稳定综合征、感染等。
2.酶替代治疗和造血干细胞移植前评估。
【特殊危重指征】
1.呼吸困难。
2.截瘫。
【会诊标准】
1.若出现睡眠呼吸暂停请耳鼻咽喉科医师会诊。
2.若出现呼吸循环衰竭,需要气管插管、机械通气请PICU医师会诊。
3.若出现寰枢关节不稳定综合征需要行颈椎融合术时请骨科医师会诊。
4.若需要造血干细胞移植治疗请血液科医师会诊。
【谈话要点】
1.黏多糖贮积症是一组由于溶酶体内酸性水解酶缺乏造成酸性黏多糖分子不能降解的先天性遗传代谢病,造成多器官系统功能损害。
2.需要进行X线检查、尿黏多糖电泳及定量分析、酶活性测定、基因分析等。
3.确诊靠各型黏多糖贮积症的酶活性测定。
4.目前黏多糖贮积症Ⅰ型、Ⅱ型、Ⅵ型可进行酶替代治疗,黏多糖贮积症ⅠH型、Ⅵ型、Ⅶ型可进行造血干细胞移植,一般2岁前进行移植治疗。
5.可合并梗阻性呼吸困难、寰枢关节发育不良等合并症。
6.预后不良,酶替代治疗费用昂贵,造血干细胞移植需要合适的供体,部分型别无有效的治疗方法。
7.此次入院的预计费用和天数。
【出院标准】
1.诊断明确,病情稳定,无严重并发症。
2.完成黏多糖贮积症健康教育。
【出院指导】
1.出院后每6个月定期到内分泌代谢专科门诊随访。随访内容包括体格发育指标、体格检查、心肺功能评估、睡眠评估、听力和视力评估等。
2.若出现以下紧急情况需及时返院或到当地医院治疗:①呼吸困难。②截瘫。
3.健康指导
(1)家属应学会正确的功能锻炼方法,包括肌肉按摩、关节的伸屈运动、保持肢体的功能位置和适当的理疗,以减轻关节和骨骼的畸形。
(2)对先证者家庭成员进行遗传咨询,通过产前诊断预防新患者出生,于孕早期(孕11~14周)取绒毛膜细胞直接酶活性测定及基因突变分析,培养的羊水细胞亦可进行酶活性测定。
【门急诊标准流程】
黏多糖贮积症门急诊标准流程见图5-9。

图5-9 黏多糖贮积症门急诊标准流程
※专科评估根据表5-6进行
【住院标准流程】
黏多糖贮积症住院标准流程见图5-10。

图5-10 黏多糖贮积症住院标准流程
※住院护理初评估根据《病人入院护理评估记录》进行,使用疼痛、营养等评估工具,详见附录D;※※专科评估根据表5-6进行
(黄永兰 张 文 刘 丽)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















