室内质量控制(internal quality control,IQC)是由实验室工作人员,采用一定的方法和步骤,连续评价实验室工作的可靠性(包括精密性和准确性),旨在监控本实验室常规工作的精密度,提高本实验室常规工作中批内、批间样本检测的一致性,保证每个患者样本测定结果的稳定性。
室内质量控制的目的是监控测定过程是否稳定,目前实验室最常用的是Levey-Jennings质控图,是一种具有质控界限的图形,质控界限通常由受控方法对质量控制品种重复测定获得的均值(x-)和标准差(s)来确定。
一、定量测定的室内质量控制
(一)设定质控图的均值和标准差
1.稳定性较长的质量控制品种 对稳定性较长的质量控制品种首先使用实验室内现行的测定方法对新批号的质量控制品种(无论非定值或定值质量控制品种)的各个测定项目确定均值和标准差,建立质控图的均值(即质控图的中心线)。定值质量控制品种的标定值只能作为均值的参考,不可以作为质控图的均值。
(1)暂定均值和标准差的确定:将新批号的质量控制品种与当前使用的质量控制品种一起至少测定20次,对测定的质控结果数据进行离群值检验(剔除超过3个标准差的数据),计算出均值和标准差,作为暂定均值和标准差。以此作为下一个月室内质控图的均值和标准差进行室内质控;当第二个月结束后,将该月的在控结果与前20个质控测定结果汇集在一起,计算累积均值和标准差,以此累积的均值和标准差作为下一个月质控图的均值和标准差。
重复上述操作过程,连续3~5个月。
(2)常规均值和标准差的建立:以最初20个数据和3~5个月在控数据汇集的所有数据计算的累积均值作为质量控制品种有效期内的常规均值,并以此作为以后室内质控图的均值和标准差。对个别在有效期内浓度水平不断变化的项目,则需不断调整均值和标准差。
2.稳定性较短的质量控制品种 对稳定性较短的质量控制品种在3~4d,每天分析同一水平质量控制品种3~4瓶,每瓶进行2~3次重复测定。收集数据后,对数据进行离群值检验(剔除超过3个标准差的数据),计算均值、标准差和变异系数,以此均值作为质控图的均值。计算标准差使用的数据量越多,标准差估计值才更好,因此不推荐使用上述重复数据来建立新的标准差。考虑到检测过程中更多的变异,建议采用以前变异系数(CV)乘以计算的均值作为新的标准差。
(二)设定质控图的质控限
质控限的设定取决于选择的质控规则,通常是以标准差的倍数表示。
(三)绘制质控图及记录质控结果
根据质量控制品种的均值和质控限绘制Levey-Jennings质控图,将原始质控结果记录在质控图标上,保留原始质控记录。
二、定性测定的室内质量控制
定性分析室内质控目前尚无通用的质控方法,一般根据具体的临床检验项目特点来确定。最常用方法是在每一次检测临床标本的同时,加上阳性和阴性对照质量控制品种,用于判断每次实验的有效性,但不能作为室内质量控制品种使用,只能在同批号的试剂盒中使用。只有在阳性或阴性质量控制品种得到预期的结果时,才能发出患者检测的报告。如果内部对照结果无效,必须重新试验。
室内质量控制品种是判断该批临床样品检测的有效性和监控检测的重复性,同时可以了解各批试剂盒的批间或孔间差异,包括强阳性、弱阳性和阴性质控血清。也可以只设置一个弱阳性质控,以该试剂盒临界值(Cut-off值)的2~3倍为宜。室内质量控制品种可以是商品或实验室自行制定,室内质量控制品种的管间或瓶间变异必须小于监测系统预期的变异(CV<20%),并且质量控制品种应稳定、无菌,不含有影响试剂反应的防腐剂。
ELISA实验质量控制品种的均值和标准差的建立时应使用实验室常规方法对质量控制品种不同批次检测至少20个数据;或至少做5个批次的检测,每个批次中不少于4个质控血清测定结果,采用x-+2s至少20次(天)所测得的质控血清S/CO值结果计算出平均值(x-)、标准差(s)、变异系数(CV),确定控制限以建立一个临时性的均值和标准差,当达到20批次数据后,替代临时性的均值和标准差。
在定性测定的室内质量控制中,应考虑检测能力和特异性两方面的质控。检测能力质控是为了保证能检出最小量的分析物,避免出现假阴性。如检测病原体抗原和抗体的定性免疫测定,重要的是所用方法的测定下限,即能检出分析物的最小量。对一个方法的测定下限的评价,可通过系列稀释阳性质控血清来进行。
还需要注意的是定性分析中区别阴性、阳性的“判断值”。在采用某一方法或试剂盒时,一定要了解此“判断值”是否符合临床诊断需要,避免临床诊断中的“漏诊”或“误诊”。当“判断值”确定后,应保证检测结果的稳定性。在定性免疫测定中使用弱阳性质控血清,不但能监测到同一质量控制品种在不同批次测定中反应信号的变化,且能灵敏地反映测定下限的改变是否会导致假阴性结果的发生。
有些临床定性测定没有明确的测定下限,对其检测能力的监测可通过采用最大检测能力的判断标准来进行。例如选择新批号琼脂培养基时,要检查培养基分离微生物能力,接种相应细菌后,如果菌落计数及形态没有接近期望的结果,则表明培养基的检测能力发生了改变。
当进行血液细胞、免疫组化染色时,可观察相应细胞的染色情况,判断染色液或染色过程是否正常,选用质量控制品种的制备应与被检标本制备条件相同,如抗凝剂、涂片厚度等以免影响染色效果。当进行细菌染色时,可用相应的阳性菌和阴性菌作质控。
综上所述,定性分析的室内质量控制方法一定要根据该检测项目特点而定。应注意的是细胞学、细菌学、病原寄生虫等形态学识别,单凭上述方法不能保证检测结果的正确,还必须依靠实验室人员的业务水平和经验。
三、室内质控其他方式——“即刻法”质控
“即刻法”质控方法是在对同一批质控血清连续测定3次后,即可对第3次检验结果进行质控。具体计算方法如下:将质控血清的测定值从小到大排列:X1,X2,X3……Xn(X1为最小值,Xn为最大值)。计算x-和s及SI上限值和SI下限值。

将SI上限、SI下限与SI值表(表1-1-1)中的数字进行了比较。
表1-1-1 S I值表
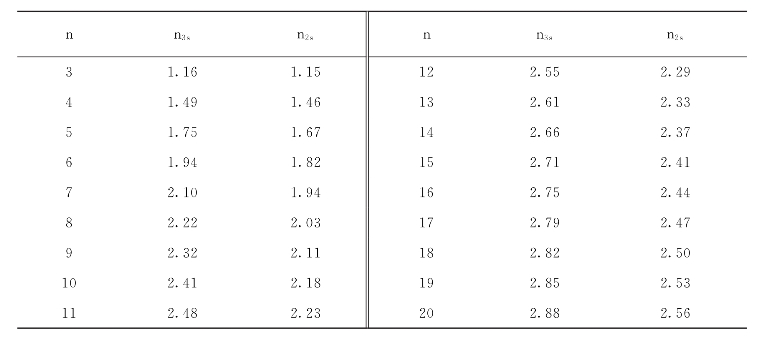
当SI上限和SI下限<n2s时表示处于控制范围内,可以继续测定。继续重复以上各项计算。
当SI上限和SI下限有一值处于n2s~n3s值之间时说明该值在2~3s范围,处于“告警”状态。
当SI上限和SI下限有一值>n3s值时说明该值已在3s范围之外,属“失控”。
“即刻法”只能在前20次内使用,超出即可采用L-J质控图方法。
四、使用患者数据的分析进行质量控制
通过使用患者数据,与临床医师沟通了解临床症状、体征、治疗效果、其他检查结果等有关信息,进行相关性分析,辅助判断检验结果的可靠程度。当某一检验项目或新开展的检验项目使用一段时间后,临床医师可能提出结果存在的问题,虽然所提的问题不十分准确可靠,但能帮助识别实验室的问题。一项检验结果应与其他多项检验结果、以往检验结果结合起来,检查是否存在问题。双份平行测定对难以取得稳定性好的质量控制品种的实验也是不错的选择。
大量患者检验结果对检出随机误差没有意义,对检出系统误差很有价值,是对基本质控方法的补充,但不可代替。如果每日标本量大于100个,MCV、MCH、MCHC可采用移动均值法又称Bull算法进行质控,控制界限一般为3%。
此外,也可以结合患者治疗上的改变做回顾性分析,这是长期质控的有效方法。总之,使用患者数据进行质量控制可能获得额外有用的信息,也是近几年提倡与临床多沟通、多交流的需要。
五、质控规则
(一)常用质控规则
将质控规则应用于质控数据,判读每一分析批在控或失控。质控规则以符号AL表示,其中A代表超过质控界限的质控测定值的个数或统计量,L代表质控界限。Westgard多规则中常用的质控规则含义如下。
12s:一个质控结果超过均值±2s,仅用作“警告”规则,并启动由其他规则来检验质控数据。
13s:一个质控结果超过均值±3s,判断失控,该规则主要对随机误差敏感。
22s:两个连续的质控结果同时超过均值+2s或-2s,判断失控,该规则对系统误差敏感。
R4s:一个质控结果超过均值+2s,另一个质控结果超过均值-2s,判断失控,该规则对随机误差敏感。
41s:四个连续的质控结果同时超过均值+1s或-1s,判断失控,该规则对系统误差敏感。
10X-:10个连续的质控结果落在均值的一侧(高或低于均值,对偏离的大小没有要求),判断失控,该规则对系统误差敏感。
(二)注意事项
1.分析质控规则至少有20d的质控结果,单个质量控制品种或两个不同浓度的质量控制品种均可,建议用两个质量控制品种。
2.选择的质控规则应既能体现随机误差又能体现系统误差。设置的浓度范围应包括均值±4s。
3.当两个质控结果落在2s质控界限之内时,接受分析批,报告患者结果。有一个质控结果超过2s质控界限时,保留患者结果,然后用1s、22s、R4s、41s和10X-规则检查质控结果。当这些规则其中之一指示该分析批失控,则判断该分析批失控,不能报告患者结果。当所有这些规则指示分析批在控,接受分析批,报告患者结果。
4.R4s规则仅应用于批内,因此批间的系统误差不能错误地解释为随机误差。但应注意此规则可应用于不同的质量控制品种,即一个质控结果可以是低浓度的质量控制品种,另一个质控结果可以是高浓度质量控制品种,只要它们是在同一批就适用R4s规则。22s、41s和10X-规则可应用于不同的批和质量控制品种。
5.质量控制品种检测结果较长时间出现在中心线一侧,提示有可能是质量控制品种发生了变化,需要重新建立质控图的中心线及质控界限,并可与定值质量控制品种同时测定,以进一步确证是否质量控制品种本身变化了。
6.发生失控时,失控数据和纠正后的在控数据应同时体现在质控图上。
7.使用新批号的质量控制品种时,应在“旧”批号质量控制品种使用结束前,将新批号质量控制品种与“旧”批号质量控制品种同时进行测定,重复上述过程,设立新质控图的中心线(均值)和质控线。
六、质控图的图形分析
检验工作中的误差有随机误差、系统误差和过失误差三种类型,对随机误差要严密监测和控制,使其限制在临床允许的范围之内,并逐渐使之缩小,对系统误差则要求尽快发现、及时纠正,但各种类型的误差绝不是以单一的、典型的形式存在,因此分清误差类型、误差的大小及其变化十分重要,要设法减少随机误差的掩盖作用,及时发现非随机误差,并进一步分析发生的原因,及时采取有效措施排除非随机误差,发挥质控的预防和指导作用。
通过观察质控图形的规律性变化进行误差分析,凡出现规律性图形变化,均提示有非随机误差因素存在,应注意分析。常见的规律性变化有以下几种(常用质控规则图形见第三篇技能操作二)。
1.曲线漂移 “漂移”现象提示存在系统误差,准确度发生了一次性的向上或向下的改变。这种变化往往是由于一个突然出现的新情况引起的,如更换校准品的生产厂家及批号、重新配制试剂及操作人员的变换等。在寻找原因时,应重点注意“漂移”现象的前后发生了哪些变动的因素。
2.趋势性变化 向上或向下的趋势性变化表明检测的准确度发生了渐进性的变化,这种变化往往是由于一个逐渐改变着的因素造成的,如试剂的挥发、蒸发、吸水、沉淀析出、分光光度计的波长逐渐偏移、光电池老化及质量控制品种本身的变质等。更换校准品、试剂或操作者则不大可能造成趋势性变化。
3.连续多点分布在中心线一侧 目前一般认为质量控制品种的检测结果连续9d以上出现在中心线同一侧,则应迅速查找原因,争取尽快使之恢复围绕中心线随机分布的状态。因为按照统计学原理由纯随机误差造成这种情况的可能性很小,连续9d以上出现在中心线同一侧的可能性小于0.38%。因此,凡出现连续9d以上在中心线同一侧者均应考虑有可能存在非随机误差因素。遇到这种情况,应积极查找原因。但如果结果与中心线偏离并不太大,不会给临床使用带来很大影响时,一般化验报告可以照常填发。
质量控制品种检测结果较长时间出现在中心线一侧,提示有可能是质量控制品种发生了变化,需要重新建立质控图的中心线及质控界限,可与定值质量控制品种同时测定,以进一步确证是否质量控制品种本身发生了变化。
4.其他规律性变化 有周期性或隔天规律性变化两种。
通过图形的资料对比进行误差分析,每个月的月底将该月全部的质量控制品种检测结果的x-和s与该批质量控制品种所有在控测定结果所求得的x-和s进行比较。如果当月x-与质控图中心线的均值发生了偏离,则说明准确度发生了变化,提示有非随机误差存在。如果当月s与该批质量控制品种所有在控测定结果所求得的s不同,则表明检测的精密度发生了变化。
将同一批质量控制品种在数月中使用所得的月份x-和s按月份顺序列出,进行分析。如果x-逐月上升或下降(特别是酶及与微生物代谢密切相关的一些项目,如糖、磷等),应考虑有可能质量控制品种稳定性欠佳或变质。如果各月份x-基本一致,而s逐月加大,则主要提示常规工作的精密度下降,应重点从试剂、仪器及管理等方面去查找原因。
在数年中把每个月的CV和失控规律列成表,可用于对该项目检测质量的历史回顾及趋势分析。
七、失控情况处理及原因分析
1.失控后的不当做法 失控后的不当做法常见的有两种。一种是重做质量控制品种,认为只要重做的结果“在控”,失控问题就解决了。这种重复检测质量控制品种的做法,实际是不信任质控方法能控制误差,结果将延误解决误差时机;另一种错误观念认为结果失控一定是“质量控制品种有问题”而更换新的质量控制品种,这样的做法说明实验室没有在真正解决失控问题上下工夫,只是通过简单的步骤,侥幸发现问题。
解决问题和排除失控原因两者既是技能,也是对待失控的认识和态度,依赖于检验人员的基础知识、技术水平和工作经验。
2.解决失控较好的做法 解决失控较好的做法是检查质控图,判断失控违背了哪条质控规则,确定误差的类型,分析原始数据及初步估计失控原因。对具体检测过程进行回顾,通过选择性复查进一步分析判断失控原因和决定处理方法,确认解决问题,做好记录。
误差类型是误差来源的线索,因为随机误差和系统误差来自不同的原因。
产生系统误差的问题较产生随机误差的问题常见,而且较易解决。造成系统误差的因素,如使用不同批号的试剂、不同批号的校准品、校准值设定错误、需要自行完成试剂预配制中发生错误的问题、试剂的质量问题或使用不当造成变质的问题、校准品过期或保存不妥造成校准值变化、因加样器或加液器的校准或调试错误使样品或试剂体积变化、孵育箱或反应加热块的温度变化、光电比色光源老化造成光强不足的问题、检验人员的变动等。
造成随机误差因素多变,如试剂瓶或试剂管道中有气泡、试剂没有充分混匀、恒温部分温度不稳定、电源电压不稳、检验人员操作不熟练、重现性差(表现在加样重复性差和对反应时间控制差)等。随机误差的性质不像系统误差那样可以预计或确定。在自动分析仪上发生失控的随机误差原因大多是:试剂瓶内或试剂管道中以及取样器或试剂加样器中的气泡、试剂未充分溶解或混匀、加样器上的取样头不密封、因机械故障使加样动作重复性差、电压不稳等。不少随机误差的原因可在检测系统运行时,对各分析项目的目视观察予以检查出来。仔细观察试剂和取样中的吸样品、吸试剂、加样品、加试剂动作,也许可以找出问题的原因。如果查不出问题,参照厂商排除故障的指导和建议去寻找原因。
特别要注意的是,刚发现失控立即重复检测,希望证实失控表现,重做的质量控制品种又“在控”了,没有做任何失控原因的处理,失控就已经“消除”了,此时要确定分析仪重复精密度是否有问题,可以用患者标本连做10次重复检测,了解患者标本检测的真实批内精密度,往往可以从这些结果的不稳定反映随机误差已经明显增大,确认失控的判断。因此在平时检测中,对于出现不正常结果的患者标本再做一次检测,对比前后两次结果的差异,容易发现随机误差的失控表现。
八、室内质控数据的管理
1.每月室内质控数据统计处理 每个月末,应对当月的所有质控数据进行汇总、统计和处理,至少包括:
(1)当月每个测定项目原始质控数据的均值、标准差和变异系数。
(2)当月每个测定项目在控数据的均值、标准差和变异系数。
(3)当月及以前每个测定项目所有质控数据的累积均值、标准差和变异系数。
(4)当月及以前每个测定项目所有在控数据的累积均值、标准差和变异系数。
2.每月室内质控数据的保存 包括当月所有项目原始质控数据、当月所有项目的质控图、所有计算的数据(包括均值、标准差和变异系数及累积均值、标准差和变异系数)、当月的失控报告单(包括违背了哪一项失控规则、失控原因、采取的纠正措施)。
3.每月上报的质控数据图表 将当月所有测定项目质控数据汇总表和失控情况汇总表上报实验室负责人。
4.室内质控数据的周期性评价 每个月的月末,都要对当月室内质控数据的均值、标准差和变异系数及累积均值、标准差和变异系数进行评价,查看与以往是否有明显不同,如有显著性变异,需要分析原因,对质控图的均值、标准差进行修改,并对质控方法重新进行设计。
(李贵霞 冯志山 武湘云)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















