临床实验室常采用血浆脂蛋白电泳、脂蛋白中胆固醇含量测定,对血浆脂蛋白进行分析。
(一)血浆脂蛋白电泳
不同脂蛋白因所含载脂蛋白的种类、等电点、颗粒大小及分子量不同,故可用电泳方法进行分离。目前常用的电泳支持介质有醋酸纤维素薄膜、琼脂糖凝胶或聚丙烯酰胺凝胶等。临床主要采用琼脂糖凝胶电泳测定血浆脂蛋白。
【原理】 以琼脂糖凝胶为支持介质分离血浆脂蛋白。由于血浆中各种脂蛋白的分子大小、分子形状、带电量不同,故在同一电场中泳动速度不同,从而得以分离。在p H8.6的电泳缓冲液中,血浆脂蛋白带负电荷,在电场中向正极移动。血浆脂蛋白琼脂糖凝胶电泳自阴极起,位于加样原点处的是CM,依次为β-脂蛋白、前β-脂蛋白和α-脂蛋白。电泳结束后,固定干燥,用脂溶性染料染色,观察脂蛋白图形;光密度计扫描,对脂蛋白组分定量。
【器材与试剂】
1.器材 电泳仪、电泳槽、加样器、恒温水浴箱、样品梳、载玻片、光密度计。
2.试剂
(1)巴比妥缓冲液(p H8.6,离子强度0.045):溶解巴比妥7.13g于500ml蒸馏水中,以浓盐酸校正p H至8.6,加蒸馏水定容至1L,4℃保存。
(2)4g/L琼脂糖凝胶:用巴比妥缓冲液稀释,沸水浴加热溶解。
(3)固定液:无水乙醇110ml,蒸馏水80ml,甘油2ml,混匀。
(4)脂肪红7B染液:①贮存液。225mg脂肪红7B溶于946ml无水乙醇中,过夜后使用,室温保存。②应用液。200ml贮存液中加入0.1mmol/L NaOH 40ml,混匀后,加入8滴Triton X-100,使用时需新鲜配制。
(5)洗脱液:75%乙醇。
【操作】
1.制备琼脂糖凝胶板:将已配制好的4g/L的琼脂糖凝胶置沸水浴中加热融化,用吸管吸取凝胶溶液约3ml浇注于载玻片上,装好样品梳以形成加样槽,静置30min后凝固。
2.加样:将10μl预染好的血浆加入槽内。
3.电泳:将点样的凝胶板平行放于电泳槽中,点样端置于阴极侧,凝胶板两端分别用4层于电泳缓冲液浸透的纱布搭桥,接通电源,电压按8V/cm,电泳30~40min。
4.固定:电泳后的琼脂糖凝胶板放入固定液中20min,于80℃烤箱中80min至干燥。
5.染色:脂肪红7B染色10min。
6.脱色:用洗脱液脱色至背景无色。
7.自然干燥。
【结果】 观察并记录脂蛋白图形;以光密度计570nm处扫描得各脂蛋白相对百分比。
【参考区间】 血浆脂蛋白琼脂糖凝胶电泳:β-脂蛋白0.50~0.60;前β-脂蛋白0.13~ 0.25;α-脂蛋白0.30~0.40;乳糜微粒:阴性。
【质量保证】
1.保证血浆新鲜,采血后2h内测定,可提高前β-脂蛋白的分离效果。
2.应根据具体情况确定电泳时的电压和时间,一般α-脂蛋白距离原点2~3cm为宜。
【应用评价】 血浆脂蛋白电泳常用于高脂蛋白血症分型分析。琼脂糖凝胶电泳法因操作简便、区带稳定及基质透明等特点广泛应用。聚丙烯酰胺凝胶电泳分辨率高,广泛用于脂蛋白亚组分的临床研究。因为分子筛效应,聚丙烯酰胺凝胶电泳所得β-脂蛋白和前β-脂蛋白区带与琼脂糖凝胶电泳法相反。
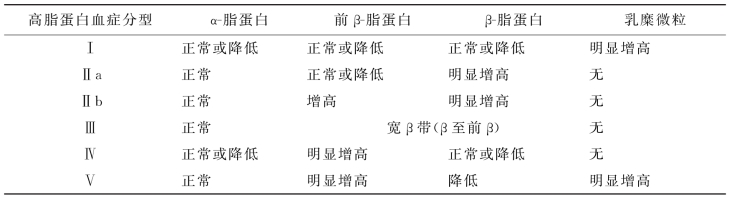
【临床意义】 血浆脂蛋白电泳对高脂蛋白血症的分型具有十分重要的意义,见表7-7。
表7-7 血浆脂蛋白电泳检测的临床意义
(二)高密度脂蛋白胆固醇测定
脂蛋白定量目前尚无理想的方法。由于脂蛋白中胆固醇含量较为稳定,故通常以脂蛋白中胆固醇含量代表脂蛋白水平。HDL、LDL和VLDL中的胆固醇分别称为高密度脂蛋白-胆固醇(HDL-C)、低密度脂蛋白-胆固醇(LDL-C)和极低密度脂蛋白-胆固醇(VLDL-C)。
由于所有脂蛋白都含胆固醇,因此必须从其他脂蛋白中分离出HDL再行测定。超速离心结合ALBK法为HDL-C测定的参考方法。由于需超速离心机,操作复杂且严格,一般实验室难以开展。临床HDL-C的测定方法大致分为两大类,即化学沉淀法和均相测定法。
化学沉淀法 采用多聚阴离子与二价阳离子结合除HDL以外的脂蛋白[CM、VLDL、IDL、LDL和Lp(a)],形成复合物沉淀,HDL则留在上清液中,测定上清液中胆固醇含量,即为HDL-C含量。
HDL-C测定主要有4类沉淀剂:肝素-锰、硫酸葡聚糖-镁、聚乙二醇(PEG)和磷钨酸-镁。肝素-锰法,易受高TAG干扰,使沉淀后的上清呈浑浊状,且干扰酶法测定胆固醇; PEG6000-Mn2+法沉淀效率高,但精密度较差,此两种方法目前已很少采用。硫酸葡聚糖-镁沉淀法(DS法)和磷钨酸-镁沉淀法(PTA-Mg2+法)测定结果比较接近,对分离HDL有较好特异性。DS法结合ALBK法被美国胆固醇参考方法实验室网络作为指定的比较方法。1995年中华医学会检验分会曾在国内推荐磷钨酸-镁沉淀(PTA-Mg2+法)作为HDL-C测定的常规方法。
【原理】 磷钨酸-镁可沉淀血浆中含ApoB的脂蛋白,而HDL不含ApoB,故留在上清液中,此上清液只含有HDL,用酶法测定上清液中的胆固醇含量,即为HDL-C含量。
【器材与试剂】
1.器材 恒温水浴箱、低速离心机、分光光度计、微量加样器。
2.试剂
(1)沉淀剂:称取AR级磷钨酸钠0.44 g和氯化镁(MgCl2·6 H 2 O)1.10g,溶于蒸馏水80ml,以1mmol/L NaOH调p H至6.15,加蒸馏水定容至100ml。此试剂可稳定1年。
(2)胆固醇酶试剂:同胆固醇氧化酶法测定血浆总胆固醇。
(3)参考血浆:使用低浓度胆固醇的准确定值血浆,或将测定TC使用的定值血浆进行1∶2或1∶3倍稀释后再用。
【操作】 取血浆和沉淀剂各0.2ml,充分混匀,室温放置10 min后,3000r/min离心15min,取上清液测定胆固醇,按表7-8进行操作。
表7-8 PTA-Mg2+法测定高密度脂蛋白-胆固醇

混匀后,37℃水浴5min,用分光光度计于500nm波长比色,以空白管调零,分别读出各管吸光度值。
【计算】 HDL-C(mmol/L)= 参考血浆胆固醇浓度
参考血浆胆固醇浓度
【参考区间】 成年男性1.16~1.42mmol/L;女性1.29~1.55mmol/L。我国的血脂异常防治建议HDL-C≥1.04mmol/L为合适水平,≤0.91mmol/L为减低。
【质量保证】
1.血浆在室温条件下,各类型脂蛋白之间发生脂质交换,游离胆固醇会不断酯化,所以要及时测定,否则应冰冻保存。血浆标本不能反复冻融。
2.PTA-Mg2+法对温度和p H改变很敏感,离心过程中温度升高使沉淀不完全;室温应控制在15~25℃,且离心后应立即吸取上清液进行测定,否则使结果偏高。
3.血浆严重浑浊时,可以将血浆用生理盐水进行1∶1稀释后沉淀,结果乘以稀释倍数。
【应用评价】 磷钨酸-Mg2+法无需昂贵的仪器,标本用量少,操作简便易行,结果稳定,高TAG血浆不影响沉淀剂的沉淀效果,且不干扰酶法分析。批内CV<1.87%,批间CV< 2.93%。本法的主要缺点是标本需预先离心处理,不适合自动化分析;且对温度和p H改变很敏感,沉淀离心后放置时间不宜过长,应于4h内进行检测,否则使结果偏高。
【临床意义】 众多流行病学研究证实,HDL-C水平与动脉粥样硬化呈负相关。低HDLC(<0.9mmol/L)是冠心病的主要危险因素,而高HDL-C(≥1.55mmol/L)被认为是负危险因子,具有保护性。此外,在脑血管疾病、糖尿病、肝炎、肝硬化HDL-C下降。高三酰甘油血症和吸烟者HDL-C常偏低,但饮酒和长期体力活动会使之升高。
HDL-C含量过高(超过2.6mmol/L)也属于病理状态,常被定义为高密度脂蛋白血症,分为原发性和继发性两类。原发性高密度脂蛋白血症可能有胆固醇酯转移蛋白(CETP)缺损、肝脂酶(HL)活性降低或其他不明原因。继发性高密度脂蛋白血症可能有运动失调、饮酒过量、原发性胆汁性肝硬化、治疗高脂血症的药物引起及其他不明原因。
均相测定法 该法免去标本的预处理(沉淀),便于自动化,为及时、快速、准确测定HDLC提供了条件,中华医学会检验分会建议均相法作为测定HDL-C的常规方法。
可供选择的方法有:①清除法,包括反应促进剂-过氧化物酶清除法(synthetic polymer/ detergent HDL-C assay,SPD法)和过氧化氢酶清除法(catalase HDL-C assay,CAT法);②PEG修饰酶法;③选择性抑制法(掩蔽法);④免疫分离法,包括PEG/抗体包裹法和抗体免疫分离法。
这些方法基本采用化学试剂或特异性抗体消除LDL、VLDL和CM对HDL-C测定的干扰,使酶试剂直接与HDL-C进行反应。
以SPD法为例说明该类方法的检测原理。
【原理】 利用脂蛋白与表面活性剂的亲和性差异进行测定。加入试剂1,在反应促进剂(合成的多聚物/表面活性剂)的作用下,血浆中CM、VLDL及LDL与试剂形成可溶性复合物,其表层的游离胆固醇在胆固醇氧化酶的催化下生成H 2 O2,后者在过氧化物酶的作用下被清除;加入试剂2,在一种特殊的选择性表面活性剂作用下,只与HDL颗粒形成可溶性复合物,HDL中的胆固醇与胆固醇酯酶、胆固醇氧化酶反应,生成H 2 O2,并作用于4-AAP色原体产生颜色反应。其颜色的深浅与HDL-C的含量成正比。主要反应式如下
CM、VLDL、LDL+反应促进剂→CM、VLDL、LDL的可溶性复合物,CM、VLDL、LDL的可溶性复合物表层FC+CHOD→H 2 O2;H 2 O 2+POD→H 2 O+O 2
HDL+选择性表面活性剂+CHE+CHOD→△4-胆甾烯酮+H 2 O2
H 2 O2+4-AAP+DSBm T+POD→显色
【器材与试剂】
1.器材 恒温水浴箱、分光光度计、微量加样器。
2.试剂 针对同一反应原理有不同的配方,具体组成及含量见说明书或相关文献。
(1)试剂1
反应促进剂 适量
偶联剂DSBm T 0.5mmol/L
胆固醇氧化酶 1.0 U/ml
过氧化物酶 3.0 U/ml
缓冲液 p H 6.0
注:DSBm T为N,N-双(4-磺丁基)-间甲苯胺二钠
(2)试剂2
4-AAP 1.0mmol/L
胆固醇酯酶 0.2 U/ml
表面活性剂 适量
缓冲液 p H 6.0
(3)标准物:定值人血浆。
【操作】 取试管3支,按表7-9操作。
表7-9 反应促进剂-过氧化物酶清除法测定HDL-C的操作步骤

【计算】

【参考区间】 同磷钨酸-镁沉淀法测定高密度脂蛋白-胆固醇。
【质量保证】
1.试剂选择原则:准确度和精密度应达到美国胆固醇教育计划(NCEP)对HDL-C测定规定的分析目标,即总误差≤13%,不精密度要求CV≤4%,不准确度要求偏差≤5%;特异性要高,高LDL-C、高VLDL-C应对测定结果无明显影响,回收率为90%~110%;最小检测水平至少为0.01mmol/L,可检测上限达2.59mmol/L(100mg/dl);抗干扰能力强,当TAG< 5.65mmol/L(500 mg/dl)、胆红素<513μmol/L(30 mg/dl)、Hb<5g/L时,对测定结果基本无干扰。采用美国疾病控制与预防中心(CDC)胆固醇参考方法实验室网络(CRMLN)验证认可的均相测定法试剂,使HDL-C测定更加方便、准确。
2.常规应用要严格按仪器和试剂盒说明书采用双试剂、双波长测定,根据反应进程曲线确定读数时间。
3.应注意使用试剂盒配套的校准物。
【应用评价】 反应促进剂-过氧化物酶清除均相测定法操作简便,易于自动化。特异性高,高LDL-C、高VLDL-C对测定结果基本无明显影响,回收率为90%~110%。最小检测水平为0.01mmol/L,线性上限可达2.59mmol/L(100mg/dl)。TAG<5.65mmol/L(500 mg/ dl)、胆红素<513μmol/L(30 mg/dl)、Hb<5g/L对测定结果基本无干扰。
(三)低密度脂蛋白胆固醇测定
与HDL-C测定相似,超速离心结合ALBK法为LDL-C测定的参考方法。临床实验室通常采用计算法和测定法获得LDL-C含量。
1.Friedewald公式计算法 此法是目前应用较广的估测LDL-C的方法,以VLDL组成恒定(VLDL-C/TAG=0.2,以mg/dl计)的假设为前提,计算公式为
LDL-C=TC-HDL-C-TAG/2.2(以mmol/L计)
或LDL-C=TC-HDL-C-TAG/5(以mg/dl计)
应用此公式计算LDL-C常受TC、TAG和HDL-C变异的影响,如某项测定值误差较大,会导致计算结果不准确。
下列情况不宜采用Friedewald公式法计算:①空腹血浆存在CM;②血浆TAG> 4.52mmol/L;③血浆中存在异常β脂蛋白(Ⅲ型高脂血症)。
2.测定法 血浆LDL-C测定主要有化学沉淀法和均相测定法两大类。
(1)化学沉淀法:常用肝素-枸橼酸钠法、聚乙烯硫酸盐沉淀法(PVS法)和多环表面活化阴离子法等。1995年中华医学会检验分会推荐PVS法作为LDL-C测定的常规方法。PVS法测定血浆LDL-C的原理:空腹血浆中主要含有HDL、LDL、VLDL,用聚乙烯硫酸盐(PVS-K)选择性沉淀LDL,上清液中存有VLDL和HDL,同时测定血浆和上清液中的胆固醇含量,以TC减去上清液中的胆固醇即为LDL-C含量。
在化学沉淀法中,聚乙烯硫酸盐沉淀法条件要求不高,在p H 3~8内均可完全沉淀,且PVS不干扰酶法测定胆固醇。主要缺点是TAG水平较高(>4.52mmol/L)会因LDL沉淀不完全而使结果偏低,且不能进行自动化分析。
(2)均相测定法:中华医学会检验分会建议均相法作为测定血浆LDL-C的常规方法,可直接测定LDL-C,在反应体系中有选择地使LDL-C显色测定。可供选择的方法主要有表面活性剂清除法、过氧化氢酶清除法、可溶性反应法、保护性试剂法等。
其中表面活性剂清除法目前在临床上广泛应用。
【原理】 其检测原理分为两步。①第一反应:试剂1中的表面活性剂1能改变LDL以外的脂蛋白(HDL、CM和VLDL等)结构并使脂蛋白解离,释放出来的微粒化胆固醇分子与胆固醇酶试剂反应,产生的H 2 O2在缺乏偶联剂时被消耗而不显色;②第二反应:加入试剂2,表面活性剂2使LDL颗粒解离释放胆固醇,参与Trinder反应显色。因非LDL在第一反应中被清除,故第二反应中呈色深浅与LDL-C的含量呈比例。主要反应式如下
CM、VLDL、HDL+表面活性剂1→微粒化胆固醇+CHE+CHOD→H 2 O 2
H 2 O2+4-AAP+POD→不显色
LDL+表面活性剂2→微粒化胆固醇+CHE+CHOD→H 2 O 2
H 2 O2+4-AAP+POD+DSBm T→显色
【器材与试剂】
1.器材 恒温水浴箱、分光光度计、微量加样器。
2.试剂 具体组成及含量见试剂盒说明书或相关文献。(1)试剂1
4-AAP 0.5mmol/L
胆固醇氧化酶 1.2U/ml
胆固醇酯酶 3.0 U/ml
过氧化物酶 0.5 U/ml
GOOD缓冲液 p H 6.3
表面活性剂1 适量
(2)试剂2
偶联剂DSBm T 1.0mmol/L
表面活性剂2 适量
GOOD缓冲液 p H 6.3
(3)标准物:定值人血浆。
【操作】 取试管3支,按表7-10操作。
表7-10 表面活性剂清除法测定血浆LDL-C的操作步骤
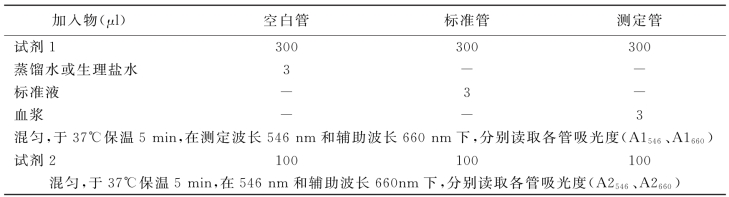
【计算】
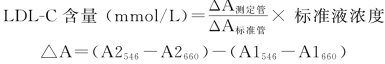
【参考区间】 随着年龄升高,LDL-C水平呈上升趋势。成年人血浆LDL-C水平为2.07~3.11mmol/L。目前我国血脂异常防治建议将LDL-C分3个水平:≤3.11mmol/L为合适范围;3.13~3.60mmol/L为边缘升高;≥3.63mmol/L为升高。
【质量保证】
1.试剂选择原则:准确度和精密度应达到NCEP对LDL-C测定规定的分析目标,即总误差≤12%,不精密度要求CV≤4%,不准确度要求偏差≤4%;特异性要好,高HDL-C、高VLDL-C应对测定结果基本无明显影响,回收率为90%~110%;最小检测水平至少为0.01mmol/L,可检测上限应达7.77mmol/L(300mg/dl)。抗干扰能力强,当TAG< 5.65mmol/L(500 mg/dl)、胆红素<513μmol/L(30 mg/dl)、血红蛋白<5g/L对测定结果基本无干扰。
采用CDC CRMLN验证认可的均相测定法试剂,使LDL-C测定更加方便、准确。
2.常规应用时应严格按仪器和试剂盒说明书采用双试剂、双波长测定,根据反应进程曲线确定读数时间。
3.应注意使用试剂盒配套的校准物。
【应用评价】 该法测定血浆LDL-C标本用量少,不需沉淀处理,操作简便,易于自动化分析。特异性好,高HDL-C、高VLDL-C对测定结果无明显影响,回收率为90%~110%。最小检测水平为0.01mmol/L,线性上限可达7.77mmol/L(300mg/dl)。抗干扰能力强,TAG< 5.65mmol/L(500 mg/dl)、胆红素<513μmol/L(30 mg/dl)、血红蛋白<5g/L对结果基本无干扰。
【临床意义】 LDL-C水平与TC一样,是判断高脂血症、预防动脉粥样硬化的重要指标, LDL-C水平与冠心病发病率呈正相关,通常以高LDL-C作为冠心病的首要致病因素。
血浆LDL-C水平随年龄增加而升高。高脂、高热量饮食、运动少和精神紧张等也使LDLC水平升高。病理性LDL-C升高见于家族性高胆固醇血症、家族性ApoB缺陷症、混合性高脂血症、肾病综合征、糖尿病、甲状腺功能减退、梗阻性黄疸、慢性肾衰竭等。
LDL-C降低见于家族性无β或低β-脂蛋白血症、营养不良、消化吸收不良、甲状腺功能亢进、肝硬化、慢性消耗性疾病、恶性肿瘤等。
(四)脂蛋白测定
电镜下Lp(a)呈圆球形,电泳多位于前β带,其脂质组成和LDL相似,但与LDL不同,并不是由VLDL转化而来,也不能转化成其他脂蛋白,是一类独立由肝合成的脂蛋白。Lp(a)结构蛋白中既有ApoB,又有特征性Apo(a)。Apo(a)是Lp(a)的特异性抗原,与纤溶酶原(plasminogen,PLG)具有高度同源性,大约80%的氨基酸序列同源。Lp(a)易沉积于血管壁,并促进平滑肌细胞生长,抑制纤维蛋白溶解,这可能是促进动脉粥样硬化和血栓形成的机制。
Lp(a)测定有两类方法,一类是以免疫化学原理测定所含的Apo(a),以Lp(a)质量表示;另一类采用超速离心法、麦胚血凝素法和琼脂糖凝胶电泳法等测定血浆Lp(a)中的胆固醇含量,以Lp(a)-C表示。目前临床主要采用免疫学方法测定。
临床实验室测定Lp(a)含量的免疫学方法主要有酶联免疫吸附试验和免疫浊度法。免疫浊度法包括免疫透射比浊法(immunoturbidimetry,ITA)和免疫散射比浊法(immunonephelometry,INA)。INA与ITA的区别在于测定光路不同,对仪器要求也不同,INA法需要光散射测定仪,ITA法可用精密的分光光度计或生化自动分析仪测定。临床上以ITA应用最广泛,免疫透射比浊法测定Lp(a)实验如下。
【原理】 利用Apo(a)的单克隆抗体与Lp(a)发生抗原抗体反应并产生浊度,在一定范围内浊度大小与血浆Lp(a)浓度成正比。
【参考区间】 健康人群中血浆Lp(a)水平多呈高度偏态分布,个体差异很大。Lp(a)水平主要取决于遗传因素,基本不受环境、饮食、药物等影响。同一个体的Lp(a)值极其恒定,新生儿血浆Lp(a)约为成年人的1/10,出生后6个月达成人水平。目前一般以300mg/L为临界值,超过300mg/L为病理性升高。
【应用评价】 中华医学会检验分会建议免疫浊度法作为临床实验室测定血浆Lp(a)的常规方法,首选ITA法,其次为INA法。目前尚无公认的Lp(a)测定参考方法。ITA法灵敏度高,便于自动化批量分析。
【临床意义】 众多临床及流行病学研究显示,Lp(a)是心脑血管疾病的独立危险因素,其在动脉粥样硬化与血栓形成中起着重要的桥梁和纽带作用。Lp(a)升高还见于急性时相反应,如急性心肌梗死、外科手术、急性风湿性关节炎等。此外,肾病综合征、胰岛素依赖型糖尿病、糖尿病肾病、妊娠、服用生长激素、血透析、腹腔透析、肾移植等,Lp(a)有可能升高。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















