实验三十 乙酸异戊酯的制备(微型实验)
一、实验目的
1.通过乙酸异戊酯的制备,进一步掌握回流加热、萃取、干燥等实验基本技术。
2.巩固普通蒸馏操作、分液漏斗的使用、液态有机化合物的洗涤、干燥等基本操作。
3.掌握液态有机化合物折射率的测定方法。
二、基本原理
乙酸异戊酯是一种有机酸酯,因为其具有香蕉的香味,故又称为香蕉水。它可以用乙酸和异戊醇直接酯化的方法合成。反应式如下:
![]()
由于酯化反应是可逆的,为了使反应进行得比较完全,通常使其中某一种反应物过量,或者不断移去某一种生成物,促使反应向右移动,以利于产物的生成。由于乙酸比异戊醇的价格便宜,而且易从反应混合物中除去,实验中通常使乙酸过量。
三、仪器和试剂
1.仪器
5mL、10 mL圆底烧瓶 微型球形冷凝管
微型直形冷凝管 微型蒸馏头
微型接液管 150℃温度计
15 mL分液漏斗 5 mL干燥锥形瓶
5 mL量筒 50 mL烧杯
阿贝折射仪
2.试剂
异戊醇 冰醋酸
浓硫酸 5%NaHCO3
无水 MgSO4 饱和NaCl溶液
3.其他
红色石蕊试纸
四、实验步骤
l.制备
如图5-10所示装置,在10 mL干燥圆底烧瓶中加入18 mL(0.017mol)异戊醇和2.4 mL(0.04 mol)冰醋酸,摇匀。小心加入4滴浓H2SO4(边滴加边轻轻旋动圆底烧瓶),加入2粒碎瓷片(或少量的人造沸石)。装好回流装置。隔着石棉网用酒精灯加热,回流40分钟。
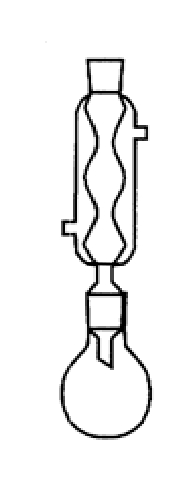
图5-10 微型回流装置
2.提纯
停止加热,待反应物冷却至室温,将它转入分液漏斗中。先用5mL蒸馏水荡洗圆底烧瓶,再用1 mL蒸馏水荡洗,并依次倒入分液漏斗中。盖好盖子,轻轻振荡几次,静置分层。上层为有机层,下层为水层。待其完全分离后,弃去水层,保留有机层。
为进一步除去有机层中的酸,向分液漏斗中加入约3 mL 5%NaHCO3溶液。用玻璃棒不断搅动,直至CO2气体放出量很少,盖好盖子,振荡1~2次,打开活塞排出气体,重复几次,直至CO2气体几乎排完。静置分层后分出水层。然后再加入3mL 5%NaHCO3溶液于分液漏斗中,盖好盖子,振荡,排气,静置,分出水层,直至水层呈碱性[1](用红色石蕊试纸检验)。加入2 mL蒸馏水洗涤有机层,用玻璃棒慢慢搅动混合物(不要振荡!),再加入0.5 mL饱和NaCl溶液帮助分层,静置,小心分出水层。
从分液漏斗上口将有机层倒入干燥的锥形瓶中,加入约0.1g无水MgSO4,盖好盖子,振荡,静置干燥10分钟[2]。将有机物倒入干燥的5 mL圆底烧瓶中,加入2粒沸石,安装好蒸馏装置[3]。
如图5-11所示。通入冷凝水后点火,隔石棉网加热,收集沸程为134℃~142℃的馏分,称取质量,计算产率。
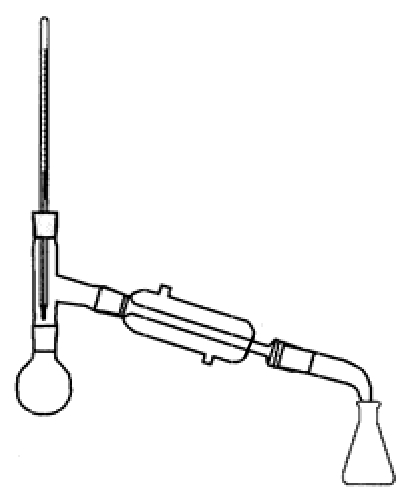
图5-11 微型蒸馏装置
3.产品纯度检验
测产品的折射率[4]。
思考题
1.酯化反应是可逆反应,本实验采用什么方法提高酯的产率?
2.为什么从反应混合物中除去过量的乙酸比除去过量的异戊醇容易些?
3.根据上述实验步骤,从中归纳出分离、提纯乙酸异戊酯的程序(用方框表示)。
注 解
[1]用5%NaHCO3洗涤时,若水层仍不显碱性,则需补加5%NaHCO3溶液洗涤,直到从分液漏斗下口分出的水层呈碱性。
[2]若液体仍是浑浊的,可再添加少许无水MgSO4,直到液体透明。
[3]蒸馏仪器必须预先干燥。将锥形瓶干燥,称取质量后,再作接受瓶使用。
[4]有关的物理常数:纯乙酸异戊酯为无色液体,沸点142℃,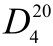 =0.8674,
=0.8674,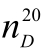 =l.4003;水
=l.4003;水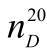 =1.3330;异戊醇
=1.3330;异戊醇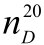 =1.4085。
=1.4085。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














