第二节 补体系统的激活与调节
一、补体系统的激活
补体固有成分以非活化形式存在于体液中,在某些激活物质的作用下,各补体成分按一定顺序,以连锁的酶促反应方式依次活化,并表现出各种生物学活性。
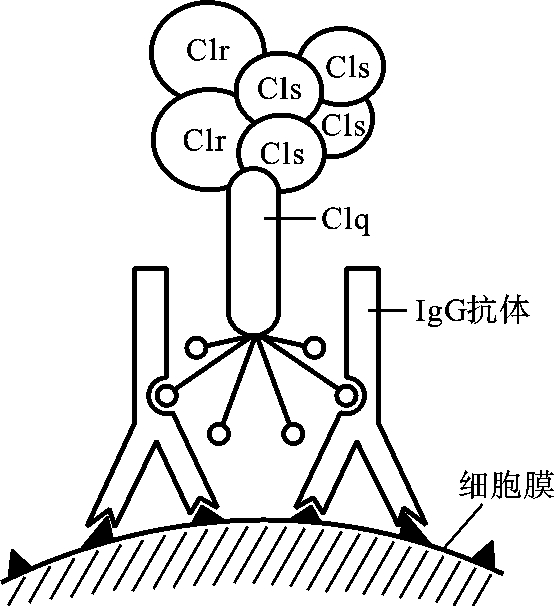
图4-1 C1q结合IgGFc段示意图
补体的激活分为三条途径:由抗原-抗体复合物结合C1q启动激活的途径称经典(传统)激活途径;由MBL(甘露糖结合的凝集素)结合至微生物启动激活的途径称MBL激活途径;由病原微生物等提供接触表面,而从C3开始激活的途径称为旁路(替代)激活途径(图4-1)。
(一)经典激活途径
经典激活途径又称传统激活途径。IgG(IgG1、IgG2、IgG3)或IgM类抗体与相应抗原结合形成的复合物是主要激活物,此复合物与C1q结合开始,依次激活补体各成分直至C9,其反应顺序为C1、C4、C2、C3、C5……C9。经典机激活途径分为识别阶段、活化阶段和膜攻击阶段三个阶段。
1.识别阶段
抗原和抗体结合后,抗体发生构象改变,使Ig的Fab段的补体结合部位暴露出来,补体C1与之结合并被激活。
C1是由三个单位Clq、Clr和Cls依赖Ca2+结合成的牢固的非活性大分子。Clq分子量最大,为六聚体,具有6个能与免疫球蛋白分子上的补体结合点相结合的部位。当两个以上的结合部位与免疫球蛋白分子结合时,即Clq桥联免疫球蛋白之后,其构型发生改变,导致Clr和Cls的相继活化。Clr在C1大分子中起着连接Clq和Cls的作用。Clq启动后可引起Clr构型的改变,在活性的Clr,后者可使Cls活化。在经典途径中,一旦形成Cls,即完成识别阶段,并进入活化阶段。
2.活化阶段
C1s作用于后续的补体成分,形成C3转化酶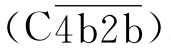 和C5转化酶
和C5转化酶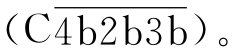
在Mg2+存在下,C1s使C4裂解为C4a和C4b两个片段。C1s与C4反应之后能更好地显露出C1s作用于C2的酶活性部位。C2在Mg2+存在下被C1s裂解为两个片段C2a和C2b。当C4b与C2a结合成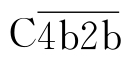 (简写成C42)即为经典途径的C3转化酶。
(简写成C42)即为经典途径的C3转化酶。
C3被C3转化酶裂解为C3a和C3b两个片段。C3b通过结合部位与具有C3b受体的细胞相结合。C3b与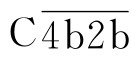 结合产生的
结合产生的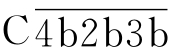 (简写成C423)为经典途径的C5转化酶。补体裂解过程中生成的小分子C4a、C2a、C3a释放到液相中,发挥各自的生物学活性。
(简写成C423)为经典途径的C5转化酶。补体裂解过程中生成的小分子C4a、C2a、C3a释放到液相中,发挥各自的生物学活性。
3.膜攻击阶段
C5转化酶裂解C5并作用于后续的其他补体成分,形成膜攻击复合物(MAC),最终导致细胞受损、细胞裂解。
C5转化酶裂解C5产生出C5a和C5b两个片段。C5a游离于液相中,具有过敏毒素活性和趋化活性。C5b可吸附于邻近的细胞表面,与C6结合成C5b6复合物。C5b6与C7结合成三分子复合物C5b67并吸附于已致敏的细胞膜上,也可吸附在邻近的、未经致敏的细胞膜上(即未结合有抗体的细胞膜上)。C5b67与细胞膜结合后,即插入膜的磷脂双层结构中。C5b67吸附C8形成C5b678。其中C8是C9的结合部位,通常与12~15个C9分子结合,共同形成C5b6789,即补体的膜攻击复合物(MAC),可使细胞膜穿孔受损(图4-2)。
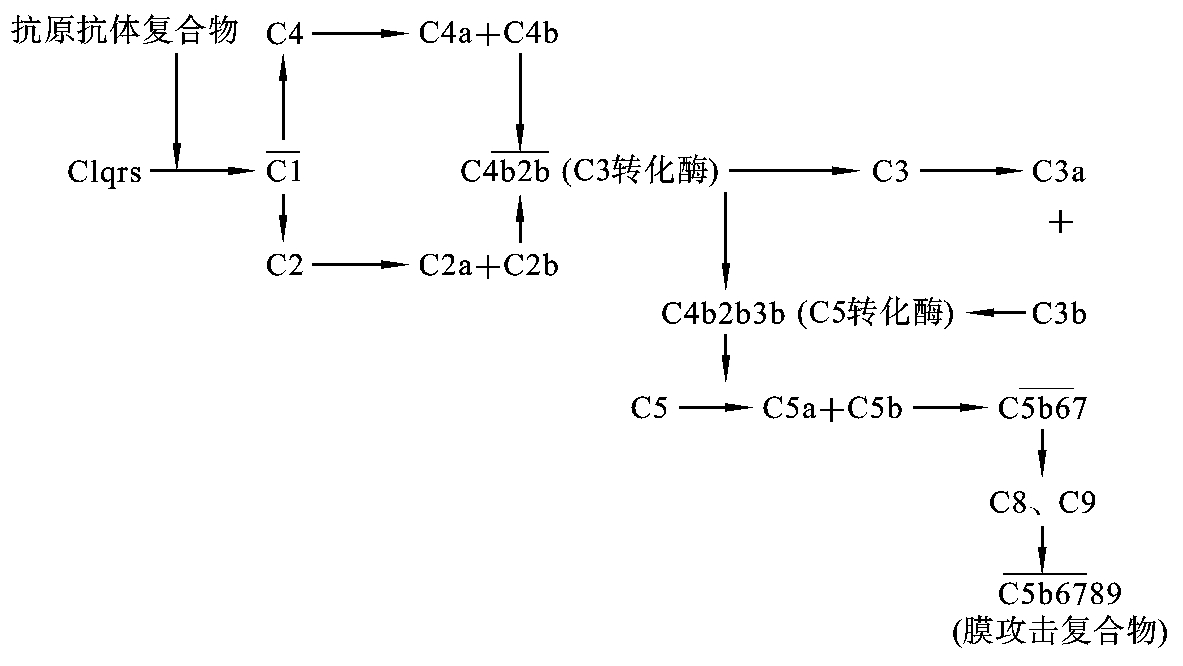
图4-2 补体经典途径激活示意图
(二)旁路激活途径
旁路激活途径又称替代途径,其不依赖于抗体,越过C1、C4、C2三种成分,直接激活C3,然后完成C5~C9的激活过程。细菌细胞壁成分(脂多糖、肽聚糖、磷壁酸)、酵母多糖、凝聚的IgA和IgG4是主要激活物。这些物质实际上提供了使补体激活的连锁反应得以进行的接触表面。
生理条件下,C3可受蛋白酶的作用,缓慢、持续地产生少量C3b。血清中的D因子可将结合状态的B因子裂解成Ba和Bb。大片段的Bb和C3b结合成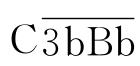 复合物,此即旁路途径的C3转化酶。
复合物,此即旁路途径的C3转化酶。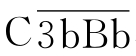 极易被迅速降解,而当旁路途径激活物存在时,可使
极易被迅速降解,而当旁路途径激活物存在时,可使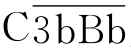 受到保护而不容易被降解。
受到保护而不容易被降解。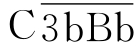 裂解C3生成C3a和C3b,后者沉积在颗粒表面并与
裂解C3生成C3a和C3b,后者沉积在颗粒表面并与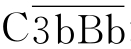 结合形成
结合形成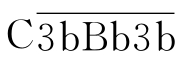 (也称
(也称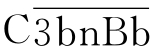 ),该复合物即旁路途径的C5转化酶,作用类似经典途径的
),该复合物即旁路途径的C5转化酶,作用类似经典途径的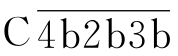 ,其后的激活过程与经典途径完全相同(图4-3)。在激活物存在的情况下,
,其后的激活过程与经典途径完全相同(图4-3)。在激活物存在的情况下,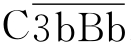 裂解更多的C3,产生更多的C3b,形成更多的C3转化酶,形成迅速放大的正反馈效应(图4-3)。
裂解更多的C3,产生更多的C3b,形成更多的C3转化酶,形成迅速放大的正反馈效应(图4-3)。
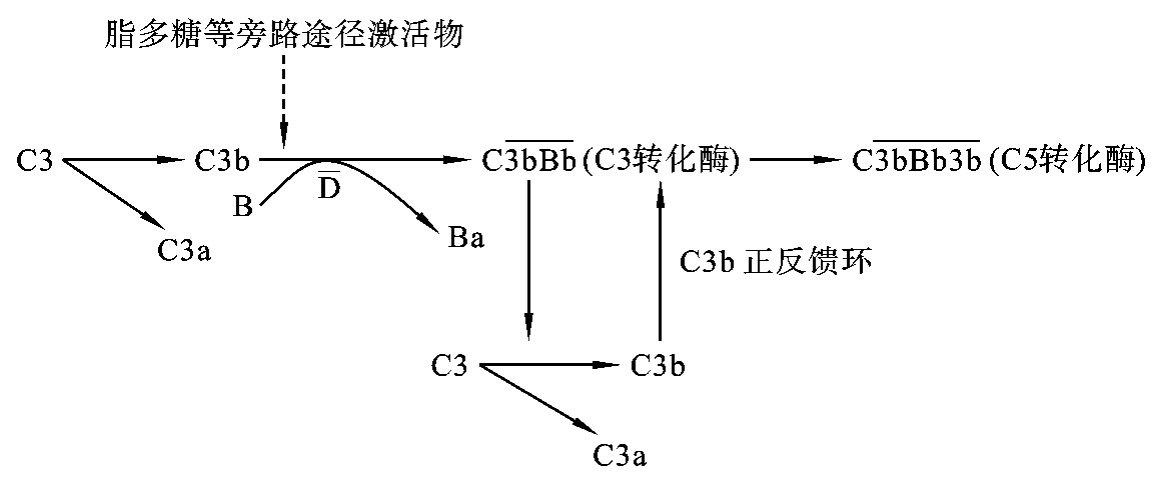
图4-3 补体旁路激活途径及C3b正反馈环示意图
(三)MBL激活途径
MBL激活途径又称凝集素途径,指由血浆中甘露糖结合的凝集素(mannose binding lectin,MBL)直接识别病原微生物表面的N氨基半乳糖或甘露糖,形成与经典激活途径基本相似的级联酶促反应过程。主要激活物为含N氨基半乳糖或甘露糖基的病原微生物。MBL分子类似于Clq分子,与病原微生物表面的N氨基半乳糖或甘露糖结合,构型发生改变,与丝氨酸蛋白酶结合1、2(MASP-1、MASP-2)并使之活化。活化的MASP-2类似于C1s的方式裂解C4和C2形成类似经典激活途径的C3转化酶,其后的反应过程与经典激活途径相同;MASP-1能直接裂解C3,形成旁路激活途径的C3转化酶,其后的反应过程与经典激活途径相同。因此MBL途径对经典途径和旁路途径活化具有交叉促进作用。
(四)补体三条激活途径的特点及比较
由于旁路激活途径和MBL激活途径活化不需要抗原抗体复合物的参与,故在病原微生物感染时,补体发挥作用的顺序依次是旁路激活途径、MBL激活途径、经典激活途径。三条途径起点各异,但相互交叉,并具有共同的终末反应过程。三条激活途径的比较见表4-1。
表4-1 补体三条激活途径的比较

二、补体系统的调节
补体系统的活化是一种高度有序的级联反应,机体通过一系列的复杂因素调节补体系统的激活过程,使之反应适度。补体系统若过度激活,不仅无益地消耗大量补体成分,反而使机体抗感染能力下降,而且在激活过程中产生的大量活性物质会使机体发生剧烈的炎症反应或造成组织损伤。补体系统精细的调控机制包括补体系统中某些成分的自发性衰变调节以及多种调节蛋白的调节。
(一)自发性衰变调节
某些补体成分的裂解产物极不稳定,易于自发性衰变,成为补体激活过程中的一种自控机制。例如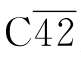 复合物中的C2b自发性衰变即可使
复合物中的C2b自发性衰变即可使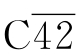 不再能持续激活C3,从而限制了后续补体成分的连锁反应。C5b也易于自发性衰变,影响到C6~C9与细胞膜的结合。此外,只有结合于固相的C4b、C3b及C5b才能触发经典激活途径,而旁路激活途径的C3转化酶则仅在特定的细胞或颗粒表面才具有稳定性,故人体血液循环中一般不会发生过强的自发性补体激活反应。
不再能持续激活C3,从而限制了后续补体成分的连锁反应。C5b也易于自发性衰变,影响到C6~C9与细胞膜的结合。此外,只有结合于固相的C4b、C3b及C5b才能触发经典激活途径,而旁路激活途径的C3转化酶则仅在特定的细胞或颗粒表面才具有稳定性,故人体血液循环中一般不会发生过强的自发性补体激活反应。
(二)调节蛋白的作用
目前已发现的可溶性或膜结合性补体调节蛋白有十余种,按其作用特点可分为以下三类。①防止或限制补体在体液中自发激活的抑制剂;②抑制或增强补体对底物正常作用的调节剂;③保护机体组织细胞免遭补体破坏作用的抑制剂。
1.经典激活途径的调控
(1)C1抑制物与C1结合 C1抑制物(C1inhibitor,C1INH)可与C1不可逆地结合,使后者失去酯酶活性,不再裂解C4和C2,从而阻断或削弱后续补体成分的反应。
(2)抑制C3转化酶形成 ①C4结合蛋白:C4结合蛋白(C4binding protein,C4bp)能竞争性地抑制C4b与C2b结合,因此能抑制C42(C3转化酶)的形成。②I因子:I因子又称为C3b灭活因子(C3binactivator,C3bINA),能裂解C3b,使其成为无活性的iC3b,因而使C42及C3bBb失去与C3b结合形成C5转化酶的机会。③膜辅助蛋白(membrane cofactor protein,MCP):MCP可促进I因子介导的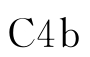 裂解,但其并不直接促进
裂解,但其并不直接促进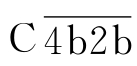 的分解。④衰变加速因子(decay accelerating factor,DAF):DAF可同C2竞争与C4b的结合,从而抑制C3转化酶形成并促进其分解。
的分解。④衰变加速因子(decay accelerating factor,DAF):DAF可同C2竞争与C4b的结合,从而抑制C3转化酶形成并促进其分解。
2.旁路激活途径的调控
(1)抑制旁路激活途径C3转化酶的组装 H因子可与B因子或Bb竞争C3b,进而使C3b被I因子酶解失活。此外,CR1和DAF也可竞争性抑制B因子与C3b结合。上述作用均干扰旁路激活途径C3转化酶的组装。
(2)抑制旁路激活途径C3转化酶的形成 I因子可将C3b水解为无活性的iC3b;H因子、CR1和MCP均可作为辅助因子,促进I因子裂解C3b的作用;CR1和MCP还可增强膜结合C3b与H因子的亲和力。上述调节机制均能降低C3bBb复合物的形成。
(3)促进已形成的C3转化酶解离 CR1和DAF可促进Bb从已形成的旁路激活途径C3转化酶中解离。
(4)对旁路激活途径的正性调节作用 备解素与C3bBb结合后发生构象改变,可使C3bBb半寿期延长10倍,从而加强C3转化酶裂解C3的作用。
3.膜攻击复合物形成的调节
C8结合蛋白(C8binding protein,C8bp)可干扰C9与C8结合;膜反应性溶解抑制物(membrane inhibitor of reactive lysis,MIRL)可阻碍C7、C8与C5b6复合物结合,从而抑制MAC形成。这两种调节蛋白是抑制MAC形成并保护自身正常细胞免遭补体攻击的重要因子。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。

















