第三节 补体活化的调控(Regulation of Complement System)
补体激活是一种高度有序的级联反应,发挥广泛的生物学效应。但如果补体系统活化失控,可形成过多的膜攻击复合物引起自身损伤,或生成过多的炎性介质引起病理反应。正常情况下,补体激活及其末端效应均处于严密调控之下,其主要机制包括:①补体的自身调控;②补体调节蛋白的作用。
一、补体的自身调控
补体激活过程中生成的某些中间产物非常不稳定,成为级联反应的重要自限因素。如,在经典和替代途径中的C3转化酶 和
和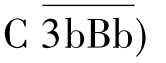 极易衰变,因此可限制C3裂解及其之后的酶促反应;与细胞膜结合的C4b、C3b及C5b也易衰变,可阻断级联反应。此外,只有当细胞表面形成抗原抗体复合物时,经典激活途径才会被启动,而替代途径的C3转化酶则仅在特定的细胞或颗粒表面才具有稳定性。
极易衰变,因此可限制C3裂解及其之后的酶促反应;与细胞膜结合的C4b、C3b及C5b也易衰变,可阻断级联反应。此外,只有当细胞表面形成抗原抗体复合物时,经典激活途径才会被启动,而替代途径的C3转化酶则仅在特定的细胞或颗粒表面才具有稳定性。
二、补体调节蛋白的作用
目前发现的可溶性或膜结合性补体调节蛋白有10余种,主要的调节蛋白如下:
1.C1抑制物(C1 inhibitor,C1 INH)
C1 INH不仅能与活化的C1r和C1s以共价键结合成稳定的复合物,抑制C1r和C1s酶活性,该抑制物还能有效防止C1qrs自发性活化。其次,C1 INH可有效地将与抗原抗体结合的C1大分子解聚,并可明显缩短C1的半衰期。最近的研究表明,C1 INH也可抑制MASPs的酶活性。
2.C4b结合蛋白(C4b-binding protein,C4bp)
这是经典激活途径中C3转化酶 的抑制物,同时也是C4b被I因子(C4b/C3b钝化因子)裂解的辅助因子。
的抑制物,同时也是C4b被I因子(C4b/C3b钝化因子)裂解的辅助因子。
3.补体受体I型(CR1,CD35)
CR1是C3b和C4b的受体。CR1对经典激活途径和替代激活途径中的C3以及C5转化酶的形成起抑制作用,同时它也是H因子裂解C3b和C4b以及iC3b进一步裂解为C3c和C3dg的协同因子。
4.I因子和H因子
I因子具有丝氨酸蛋白酶的活性,可将经典激活途径中C4b或替代激活途径中C3b降解,从而抑制C3转化酶的形成。H因子可与B因子或Bb竞争结合C3b,它对替代激活途径中的C3转化酶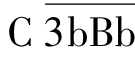 起抑制作用。
起抑制作用。
5.衰变加速因子(decay accelerating factor DAF,CD55)和膜辅助蛋白(membrane cofactor protein,MCP)
DAF可竞争性结合经典激活途径中的C4b或替代激活途径中的C3b,从而抑制C3转化酶的形成并促进其分解。MCP为辅助因子,促进I因子介导的C4b裂解。
6.MAC装配的调节蛋白同源限制因子(homologous restriction factor,HRF)
其也称C8结合蛋白(C8-binding protein,C8bp),可干扰C9与C8结合;膜反应性溶解抑制物(membrane inhibitor of reactive lysis,MIRL)即CD59,能抑制MAC在细胞膜上组装的最后一步,通过与C5b-8复合物的结合而限制C9的加入,从而阻止多聚C9复合物的形成。这两种调节蛋白可能是抑制MAC形成并保护正常细胞免受补体溶细胞作用的最重要因子。
补体调节物对补体激活途径的调节见图5-8。

图5-8 补体活化的调控
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














