(一)主要仪器和材料
WRS-1B数字熔点测定仪(未校正)、X4型显微熔点测定仪、Perkin-Elmer 983G红外光谱仪、Bruker ARX600核磁共振仪(TMS内标)、Autospec Ultima-TOF型质谱仪、制备高效液相色谱仪、中压液相色谱仪、旋转薄膜蒸发器、层析预柱。葡聚糖凝胶LH-20、聚酰胺、柱层析用硅胶G(100~200目)、硅胶H及薄层层析用硅胶G及石油醚、氯仿、乙酸乙酯等试剂。猫爪草正丁醇提取部位大孔吸附树脂30%乙醇、50%乙醇洗脱部位。
(二)方法
大孔吸附树脂30%乙醇的洗脱部分(65g),用硅胶拌样后经硅胶柱层析,氯仿-甲醇-水(8.0∶2.5∶0.5下层洗脱,洗脱液减压回收溶剂。以0.3%CMC-Na的硅胶G板,以CHCl3-MeOH-H2O(65∶35∶10)下层为展开剂展开,以5%磷钼酸试液、硫酸乙醇试液为显色剂显色,进行薄层层析检视,合并相同组分,得80份。其中20~50份合并,经反复中压柱层析,CHCl3-MeOH-H2O(75∶25∶10)下层洗脱,合并相同组分,得化合物Ⅰ(15mg);51~80份合并,经反复中压柱层析CHCl3-MeOH-EtOAc-H2O(2∶2∶4∶1)下层洗脱,合并相同组分,LH-20凝胶柱层析,50%甲醇洗脱,得化合物Ⅱ(23mg)和化合物Ⅲ(20mg)。
大孔吸附树脂50%乙醇的洗脱部分(35g),用硅胶拌样后经硅胶柱层析,氯仿-甲醇(95∶5~50∶50)梯度洗脱,洗脱液减压回收溶剂,得150份。以0.3%CMC-Na的硅胶G板,以CHCl3-MeOH-H2O(65∶35∶10)下层等为展开剂展开,以5%磷钼酸乙醇液、硫酸乙醇溶液为显色剂显色,进行薄层层析检视,合并相同组分,将量多的组分再进行柱层析。其中20~50份合并,经反复中压柱层析,CHCl3-MeOH-H2O(65∶35∶10)下层洗脱,得化合物Ⅳ(15mg);51~100份合并,经反复中压柱层析,氯仿-甲醇(含5%水)(95∶5)洗脱,得化合物Ⅴ(20mg)。
(三)结构鉴定与分析
化合物Ⅰ:无色胶状物(甲醇),经鉴定化合物Ⅰ为4-氧代-5-(-O-β-D-葡萄糖基)戊酸正丁基酯4-0-5-(-O-β-D-glucose)valeric acid-n-butylester,结构如下。

解析过程:mp 207~208℃,阳性EI-MS m/z 373.2!M+Na"+,189.2!M-162+H"+;阴性EI-MS m/z 349.3!M-H"+;HRFABMS m/z 373.1426[M+Na]+。1 HNMR(DMSO-d6,500MHz),13CNMR(DMSO-d6,125MHz),结果分析见表3-45。
表3-45 1HNMR(DMSO-d6,500MHz),13 CNMR(DMSO-d6,125MHz)
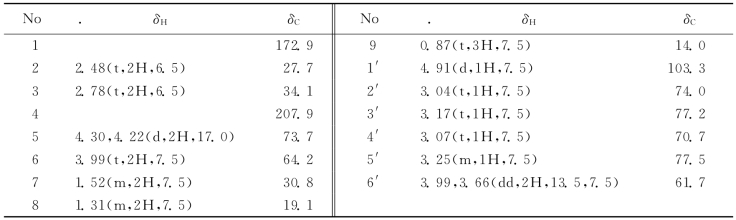
化合物Ⅱ:棕色胶状物(甲醇),经分析鉴定为:(R)-3-[3-羟基-4-(-O-β-D-葡萄糖基)-苯基-]-2-羟基丙酸-正丁基酯(R)-3-[3-hydroxyl-4-(-O-β-D-glucose)phenyl]-2-hydroxylacetic acid-n-butylester,其结构如下。

解析过程:mp 182~183℃,Molish反应呈阳性,Libermann-Burnchard反应呈阳性EI-MS m/z 439.2!M+Na"+,255.2!M-162+H"+;阴性EI-MS m/z 415.3!M-H"+;HRFABMS m/z 439.1551[M+Na]+1 HNMR(DMSO-d6,500MHz),13 CNMR(DMSO-d6,125MHz),见表3-46。
表3-46 1HNMR(DMSO-d6,500MHz),13 CNMR(DMSO-d6,125MHz)

化合物Ⅲ:白色结晶(MeOH),经分析鉴定为豆甾醇-3-O-β-D-葡萄糖苷,其结构如下。

解析过程:mp 182~184℃,Molish反应呈阳性,Libermann-Burnchard反应呈阴性。EIMS:588.9(M+),536.3,475.7,454.6,362.7,224.6,102.4,66.4,1 HNMR:0.56,0.75,0.94,0.94,1.01,1.03(6个CH3)3.6(1H,m,3-H),4.2(1H,d),5.0(2H,m,22-H,23-H),0.31(1H,6-H).13 CNMR:38.3,31.4,77.0,42.0,140.0,121.0,31.8,49.6,50.6,36.8,20.2,39.8,45.2,56.3,24.9,28.7,55.3,12.2,19.8,40.3,21.2,137.9,128.712,8.7,55.4,29.3,18.2,19.1,25.5,11.9,100.6,73.4,76.7,69.8,67.8,60.9,EI-MS:588.9(M+),536.3,475.7,454.6,362.7,224.6,102.4,66.4,1 HNMR,13 CNMR:葡萄糖基:1′:δH4.90(d,1H,7.5)δC101.6,2′:δH3.06(t,1H,7.5)δC77.7,3′:δH3.44(t,1H,7.5)δC77.5,4′:δH3.30(t,1H,7.5)δC74.2,5′:δH3.65(m,1H,7.5)δC70.9,6′:δH(dd,2H,13.5,7.5) δC61.9,豆甾醇基:基本骨架信息与葫芦烷一致。
化合物Ⅳ:无色胶状物,鉴定该化合物为4-氧代-5-(O-β-D-葡萄糖基)-戊酸甲酯。
解析过程:1 HNMR(D2O)D:2.55(2H,t,J=6.5Hz,H-2),2.74(2H,t,J=6.5Hz,H-3),3.57(3H,s,H-6),4.35(1H,d,J=7.5Hz,Glu-H-1),4.43,4.54(2H,d,J=17.5Hz,H-5)。13CNMR(D2O)D:27.3(C-2),33.4(C-3),52.4(C-6),60.7(Glu-C-6),69.6(Glu-C-4),73.1(C-5),73.5(Glu-C-2),75.6(Glu-C-3),76.1(Glu-C-5),102.2(Glu-C-1),175.9(C-1),208.9(C-4)。上述NMR数据与化合物Ⅶ比较,少了一组正丁基的信号,而多了一个甲氧基的信号,故而得出以上结论。
化合物Ⅴ:白色粉末,维太菊苷一致。解析过程为:mp 273~276℃,IR(KBr)cm-1:3 400(OH),2 960,2 930,1 660(C=C),1640(C=C),1 460,1 380,1 080,1 020。ESIMS m/ z(%):575(M++1),412(M+-162),394(M+-162-H2O),275,255,213,83,69,43。与维太菊苷对照品混合熔点不下降。
化合物Ⅵ:淡黄色粉末,该化合物为罗波斯塔黄酮-4′-甲醚。
解析过程:ESI-MSmz:551[M-H]-。1 HNMR(DMSO-d6)D:6.19(1H,d,J=2.0Hz,H-6),6.49(1H,d,J=2.0Hz,H-8),6.63(1H,s,H-8″),6.81(1H,s,H-3),6.86(1H,s,H-3″),6.93(2H,d,J=9.0Hz,H-3,5),7.23(1H,d,J=9.0Hz,H-5′),7.82(1H,d,J=2.5Hz,H-2′),7.95(2H,d,J=9.0Hz,H-2,6),8.07(1H,dd,J=2.5,9.0Hz,H-6′),3.79(3H,s,OCH3),12.9,13.2(各1H,s,5″,5,5-OH),10.4(1H,s,4-OH),10.8(2H,s,7,7″-OH)。13 CNMR(DMSO-d6)D:56.5(OCH3),94.1(C-8″),94.8(C-8),99.6(C-6),103.6(C-3),104.2(C-3″),104.2(C-10″),104.5(C-10),109.3(C-6″),112.4(C-5′),116.7(C-3,5),121.9(C-1),123.1(C-3′),123.3(C-1′),128.6(C-6′),129.2(C-2,6),131.0(C-2′),157.1(C-9″),158.1(C-9),159.6(C-4),161.4(C-5),161.9(C-5″),162.1(C-7″),162.6(C-4′),164.1(C-7),164.4(C-2),164.9(C-2″),182.4(C-4),182.6(C-4″)。上述NMR数据与罗波斯塔黄酮-4′-甲醚报道一致。
化合物Ⅶ:淡黄色粉末,为榧双黄酮。
解析过程:ESI-MSmz:579[M-H]-。1 HNMR(DMSO-d6)D:6.17(1H,d,J=2.0Hz,H-6),6.46(1H,d,J=2.0Hz,H-8),6.65(1H,s,H-6″),6.90(1H,s,H-3″),6.91(2H,d,J=9.0Hz,H-3,5),6.92(1H,s,H-3),7.33(1H,d,J=9.0Hz,H-5′),7.59(2H,d,J=9.0Hz,H-2,6),8.05(1H,d,J=2.5Hz,H-2′),8.16(1H,dd,J=2.5,9.0Hz,H-6′),3.76(3H,s,OCH3),3.80(3H,s,OCH3),3.82(3H,s,OCH3),12.9,13.2(各1H,s,5″,5-OH),10.8(1H,s,7-OH)。13 CNMR(DMSO-d6)D:55.5(OCH3),55.9(OCH3),56.5(OCH3),94.8(C-8),96.3(C-6″),99.7(C-6),103.9(C-3″),104.5(C-10″),104.5(C-3),104.8(C-10),105.3(C-8″),112.5(C-5′),115.2(C-3,5),121.9(C-3′),123.3(C-1′),123.4(C-1),128.6(C-2,6),129.0(C-6′),131.5(C-2′),154.1(C-9″),158.1(C-9),161.0(C-4′),162.1(C-5″),161.2(C-5),163.0(C-4),163.3(C-7″),163.9(C-2),164.2(C-2″),164.9(C-7),182.5(C-4),182.8(C-4″)。HMBC谱中3个OCH3上的氢分别和4′,4,7″位碳相关,2′位氢和8″位碳及6′位碳相关,说明OCH3连在4′;4,7″位,双黄酮的两部分通过3′,8″位连在一起。上述NMR数据与榧双黄酮文献报道一致。
化合物Ⅶ:淡黄色粉末,为罗汉松双黄酮A。
解析过程:ESI-MSmz:551[M-H]-。1 HNMR(DMSO-d6)D:6.07(1H,s,H-6″),6.14(1H,d,J=2.0Hz,H-6),6.20(1H,d,J=2.0Hz,H-8),6.70(2H,d,J=8.5Hz,H-3,5),6.74(1H,s,H-3),6.78(1H,s,H-3″),6.92(1H,d,J=9.0Hz,H-5′),7.75(2H,d,J=8.5Hz,H-2,6),7.88(1H,dd,J=2.5,9.0Hz,H-6′),8.22(1H,d,J=2.5Hz,H-2′),3.60(3H,s,OCH3),13.0,13.1(各1H,s,5″,5-OH)。13 CNMR(DMSO-d6)D:55.2(OCH3),93.9(C-8),98.6(C-6″),101.3(C-6),102.3(C-3),103.0(C-3″),103.0(C-10),103.5(C-10″),103.9(C-8″),114.1(C-3,5),118.4(C-5′),118.9(C-1),122.9(C-3′),123.3(C-1′),126.6(C-6′),126.9(C-2,6),131.4(C-2′),154.7(C-9),157.3(C-9″),160.5(C-4),161.4(C-5),161.7(C-5″),162.3(C-4′),163.7(C-7″),163.9(C-7),164.5(C-2″),164.5(C-2),181.5(C-4),181.6(C-4″)。HMBC谱中OCH3上的氢和4位碳相关,2′位氢和8″位碳及6′位碳相关,说明OCH3连在4位,双黄酮的两部分通过3′,8″位连在一起,上述数据与罗汉松双黄酮A文献报道一致。
化合物Ⅷ:淡黄色粉末,为去甲银杏双黄酮。
解析过程:ESI-MSmz:551[M-H]-。1 HNMR(DMSO-d6)D:6.11(1H,d,J=2.0Hz,H-6),6.27(1H,s,H-6″),6.39(1H,d,J=2.0Hz,H-8),6.70(2H,d,J=9.0Hz,H-3,5),6.69(1H,s,H-3″),6.81(1H,s,H-3),7.28(1H,d,J=9.0Hz,H-5′),7.47(2H,d,J=9.0Hz,H-2,6),HdJHzHHddJ2.5,9.0Hz,H-6′),3.75(3H,s,OCH3),12.9,13.1(各1H,s,5,5″-OH)。13 CNMR(DMSO-d6)D:56.4(OCH3),94.9(C-8),99.9(C-6″),99.9(C-6),102.9(C-8″),103.2(C-3″),103.9(C-3),104.1(C-10″),104.5(C-10),112.2(C-5′),116.5(C-3,5),121.9(C-3′),121.9(C-1),123.2(C-1′),128.4(C-2′),128.6(C-2,6),131.7(C-6′),155.1(C-9″),158.2(C-9),161.1(C-4),161.3(C-5″),161.9(C-7″),162.1(C-4′),162.1(C-5),163.7(C-7),163.9(C-2″),166.4(C-2),182.2(C-4″),182.3(C-4)。HMBC谱中OCH3上的氢和4′位碳相关,2′位氢和8″位碳及6′位碳相关,说明OCH3连在4′位,双黄酮的两部分通过3′,8″位连在一起,上述数据与去甲银杏双黄酮文献报道一致。
化合物Ⅸ:淡黄色粉末,确定该化合物为异银杏双黄酮。
解析过程:ESI-MSmz:565[M-H]-。1 HNMR(DMSO-d6)D:6.18(1H,d,J=2.0Hz,H-6),6.40(1H,s,H-6″),6.46(1H,d,J=2.0Hz,H-8),6.88(2H,d,J=8.0Hz,H-3,5),6.90(1H,s,H-3″),6.92(1H,s,H-3),7.33(1H,d,J=8.5Hz,H-5′),7.58(2H,d,J=8.0Hz,H-2,6),8.02(1H,d,J=2.5Hz,H-2′),8.16(1H,dd,J=2.5,8.5Hz,H-6′),3.73(3H,s,OCH3),3.77(3H,s,OCH3),12.9,13.0(各1H,s,5,5″-OH),10.8(2H,s,7,7″-OH)。13 CNMR(DMSO-d6)D:56.2(OCH3),56.6(OCH3),94.8(C-8),99.3(C-6″),99.6(C-6),103.3(C-8″),104.3(C-3″),104.4(C-3),104.4(C-10″),104.6(C-10),112.4(C-5′),115.2(C-3,5),122.3(C-3′),122.3(C-1),123.2(C-1′),128.5(C-2′),128.9(C-2,6),131.6(C-6′),155.0(C-9″),158.1(C-9),161.1(C-4′),161.3(C-5″),162.1(C-4),162.5(C-5),162.9(C-7″),163.8(C-7),164.0(C-2),164.9(C-2″),182.5(C-4″),182.8(C-4)。上述数据与异银杏双黄酮文献报道一致。
化合物Ⅹ:淡黄色粉末,易溶于丙酮,经解析过程确证该化合物为穗花杉双黄酮。
解析过程:ESI-MSmz:537[M-H]-。1 HNMR(DMSO-d6)D:6.18(1H,d,J=2.0Hz,H-6),6.40(1H,s,H-6″),6.46(1H,d,J=2.0Hz,H-8),6.71(2H,d,J=9Hz,H-3,5),6.78(1H,s,H-3″),6.82(1H,s,H-3),7.14(1H,d,J=9.0Hz,H-5′),7.56(2H,d,J=9.0Hz,H-2,6),7.98(1H,dd,J=2.5,9.0Hz,H-6′),8.00(1H,d,J=2.5Hz,H-2′),13.1,13.2(各1H,s,5,5″-OH),10.8,10.3(各1H,s,7,7″-OH)。13 CNMR(DMSO-d6)D:94.7(C-8),99.3(C-6″),99.5(C-6),103.3(C-3″),103.7(C-10),104.3(C-3),104.4(C-10″),104.6(C-8″),116.5(C-3,5),116.8(C-5′),120.7(C-3′),121.7(C-1′),122.1(C-1),128.5(C-6′),128.9(C-2,6),132.1(C-2′),155.2(C-9″),158.1(C-9),160.2(C-4′),161.2(C-5″),161.7(C-5),162.1(C-4),162.5(C-7″),164.4(C-7),164.5(C-2″),164.8(C-2),182.4(C-4),182.8(C-4″)。上述NMR数据与穗花杉双黄酮文献报道一致。
化合物Ⅺ:无色胶状物,鉴定该化合物为4-氧代-5-(O-β-D-葡萄糖基)-戊酸甲酯。
解析过程:1 HNMR(D2O)D:0.95(3H,t,J=7.5Hz,H-9),1.39(2H,m,J=7.5Hz,H-8),1.61(2H,m,J=7.5Hz,H-7),2.59(2H,t,J=6.5Hz,H-2),2.86(2H,t,J=6.5Hz,H-3),4.08(2H,t,J=7.5Hz,H-6),4.31(1H,d,J=7.5Hz,Glu-H-1),4.34,4.50(2H,d,J=17Hz,H-5)。上述NMR数据与文献报道一致。
化合物Ⅻ:无色胶状物,鉴定该化合物为4-氧代-5-(O-β-D-葡萄糖基)-戊酸甲酯。
解析过程:1 HNMR(D2O)D:2.55(2H,t,J=6.5Hz,H-2),2.74(2H,t,J=6.5Hz,H-3),3.57(3H,s,H-6),4.35(1H,d,J=7.5Hz,Glu-H-1),4.43,4.54(2H,d,J=17.5Hz,H-5)。13 CNMR(D2O)D:27.3(C-2),33.4(C-3),52.4(C-6),60.7(Glu-C-6),69.6(Glu-C-4),73.1(C-5),73.5(Glu-C-2),75.6(Glu-C-3),76.1(Glu-C-5),102.2(Glu-C-1),175.9(C-1),208.9(C-4)。根据上述NMR数据可确定为该化合物为4-氧代-5-(O-β-D-葡萄糖基)-戊酸甲酯。
化合物ⅫⅠ:无色结晶(甲醇),确证该化合物为苯甲醇O-β-D-葡萄糖苷。
解析过程:1 HNMR(D2O)D:7.17~7.35(5H,m),4.80,4.61(2H,d,J=11.5Hz),4.38(1H,d,J=8.0Hz,Glu-H-1)。13 CNMR(D3O)D:136.8(C-1),129.7(C-3,5),128.9(C-2,6),128.6(C-4),69.6(C-7),101.4(Glu-C-1),76.1(Glu-C-5),75.9(Glu-C-3),73.3(Glu-C-2),71.6(Glu-C-4),61.0(Glu-C-6)。
(四)小结
猫爪草正丁醇提取部位经大孔吸附树脂技术梯度洗脱,然后使用硅胶吸附层析、中压液相硅胶柱层析(MPLC)及羟丙葡聚糖凝胶柱层析(Sephadex LH-20)等多种层析分离技术进行分离,利用Mp[α],EI-MS,NMR,2DNMR等现代分析技术鉴定13个化合物,分别为4-氧代-5-(-O-β-D-葡萄糖基)-戊酸-正丁基酯和(R)-3-[3-羟基-4-(-O-β-D-葡萄糖基)-苯基-]-2-羟基丙酸-正丁基酯和豆甾醇-3-O-β-D-葡萄糖苷等。
近10年来虽然我国许多学者对猫爪草化学成分进行了较深入的研究,但分离得到苷类成分仅见有β-谷甾醇和豆甾醇二者D-葡萄糖苷的混合物及胡萝卜苷等。此实验分离鉴定的3个苷类成分均是首次从该类植物中得到,前2个为新化合物,后一个为已知成分。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















