心包是包绕在心脏和大血管根部的相对性无血管结构的纤维囊,由壁层和脏层心包构成,壁层心包为纤维结构,厚度<2mm,主要由胶原纤维和少量的弹性纤维构成。脏层心包由间皮细胞组成,黏在心外膜上(图65-1)。心包疾病是临床上的常见病,大多数患者能在一般的医疗机构进行处理,对于反复发作的和特定类型的病例,可能需要多学科协作处理或需要在特定的中心进行治疗。临床上心包疾病一系列争议的问题如下:①病因和分类;②诊断与鉴别诊断;③抗炎药物的使用;④复发与难治病例的处理;⑤心包穿刺和活检;⑥心包切除术、心包开窗术和其他干预技术。

图65-1 动物实验猪的正常心包解剖图
注:大体观察心包为半透明的薄膜,透过心包清晰可见心外膜冠状动脉,壁层心包外附着脂肪结缔组织(图A),切开壁层心包,可见壁层心包非常薄,透过壁层心包切口,可见心外膜的脏层心包更加菲薄(图B);PP,壁层纤维心包
一、病因与分类
心包疾病包括先天性心包缺损、心包炎(干性、积液性、积液缩窄性和缩窄性)、肿瘤和囊肿。心包炎的病因是多变的(表65-1),确定原因可能更加困难,特发性或病毒性心包炎可能是最常见诊断。
表65-1 心包炎的病因:简单的分为感染性和非感染性

二、诊断与鉴别诊断
心包炎的诊断标准包括典型的胸痛、心包摩擦音、提示性的心电图变化(典型的广泛性ST段抬高、PR压低)和新出现的或恶化的心包积液。所有的怀疑心包炎患者,基本诊断评价应该包括心脏听诊、心电图、经胸超声心动图;常规的血液检查包括炎症标记物[如,C反应蛋白和(或)血沉]和心肌损害指标(肌酸激酶同工酶、肌钙蛋白)、以及胸部X线检查。应该附加相关的可疑病因试验。超声心动图是心包积液诊断中最敏感和最准确的工具,诊断一般无困难。在诊断心包积液时,应注意判断有无心脏压塞,更重要的是超声心动图能引导心包穿刺。出现心脏压塞时,右心房和(或)右心室壁出现舒张期塌陷(图65-2),这是由于相对较高压力的心包积液容易压迫相对低压的心脏结构。右心房塌陷更敏感,但是右心室塌陷持续超过1/3舒张期是心脏压塞更特异性指标。必须注意,大量胸腔积液时,即使无心包积液和心脏压塞,也可出现右心室塌陷现象。由于心脏压塞时,左右心室的相互作用增强,多普勒超声心动图的心室充盈指标呼吸变化更加明显(图65-3)。虽然超声心动图能提供重要的信息,必须强调的是,心脏压塞是临床诊断,而不是超声诊断。
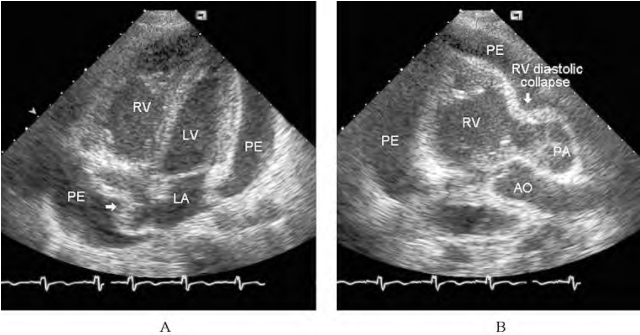
图65-2 超声心动图显示心脏压塞
心尖四腔心切面显示大量心包积液及舒张末期右心房塌陷(箭头所示)(图A),同一患者的另一切面显示右心室流出道舒张晚期塌陷(箭头所示)(图B),舒张期右心房和右心室塌陷与心脏压塞的生理表现一致;AO.主动脉;LA.左心房;PA.肺动脉;PE.心包积液;RA.右心房;RV.右心室
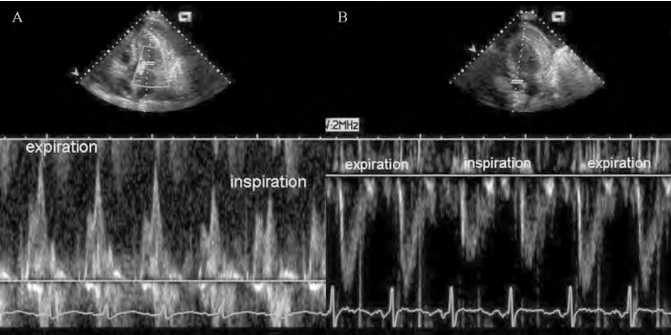
图65-3 心脏压塞时多普勒超声心动图的变化
正常人的二尖瓣和主动脉血流速度随呼吸变化的幅度较小,当出现心脏压塞时,这些指标的变化幅度明显增加,吸气时二尖瓣(图A)和主动脉瓣血流速度(图B)明显减低,严重的心脏压塞的病例,吸气时因为左心室容量太少,主动脉瓣未开放,因此,主动脉瓣口可记录不到收缩期血流频谱
超声心动图、CT和MRI能显示大多数缩窄性心包炎患者的心包增厚(≥2mm),X线胸片上显示心包钙化提示缩窄性心包炎的诊断。MRI也能显示心包粘连。然而,缩窄性心包炎可能无心包钙化,甚至无心包增厚。在143例外科证明的缩窄性心包炎中,18%的患者心包厚度正常(<2mm)。另外,也可能出现局限性心包缩窄。实验研究证实二维超声心动图大大地高估心包膜的厚度,经食管超声心动图是探查心包厚度更敏感和更准确的方法。
多普勒超声心动图对可疑缩窄性心包炎的评价有重要的意义(图65-4),左右心室常呈限制性充盈,左心室舒张早期充盈(E波)减速时间短,A波变小或缺乏。二尖瓣血流速度明显的呼吸变异(>25%),尽管呼吸系统疾病也有这种呼吸变异,但是伴有明显的上腔静脉血流速度的变化,然而,缩窄性心包炎上腔静脉血流速度的变化很小。组织多普勒超声心动图对识别缩窄性心包炎可能也有帮助。
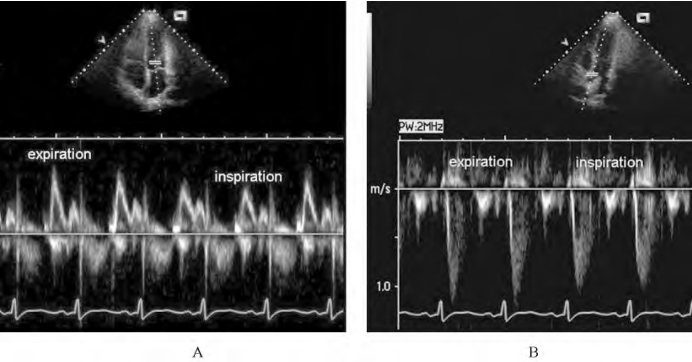
图65-4 缩窄性心包炎的多普勒超声心动图变化
A.二尖瓣血流速度呼吸变异常大于25%;B.主动脉瓣血流速度也存在呼吸变异;任何不可解释的体循环静脉淤血应该怀疑缩窄性心包炎,超声心动图对于识别三尖瓣病变和(或)合并的肺动脉高压有帮助,缩窄性心包炎的肺动脉压力一般正常或轻微升高(<50mmHg)。临床上最难鉴别的是缩窄性心包炎与限制性心肌病,因为两者的临床和超声心动图表现往往相似,尽管多普勒超声心动图和组织多普勒可能提供帮助
文献报道缩窄性心包炎患者B型利钠肽轻微升高(<200pg/ml),限制性心肌病患者则明显升高(>600pg/ml)。
在心导管实验室,缩窄性心包炎患者左右心腔的舒张末压几乎相等,右心室舒张末压常超过1/3右心室收缩压;而限制性心肌病患者左心室舒张末压超过右心室舒张末压,并常见肺动脉高压。然而,这些血流动力学标准鉴别诊断的特异性有限(24%~57%)。
上述这些指标都是通过间接的方法来识别缩窄性心包炎,理论上来说直接的方法应该优越于间接方法,因此,很多研究者试图使用无创性影像技术显示心包增厚的病理学变化来识别缩窄性心包炎,然而,18%的缩窄性心包炎患者心包厚度正常(<2mm),同时心包增厚不一定意味着有缩窄性心包炎的表现。因此,这些影像技术在临床实践中有明显的局限性,使得临床上部分患者需要通过开胸才能确定诊断。
三、抗炎药物的使用
(1)阿司匹林和非甾体类抗炎药:为心包炎的主要治疗药物。当使用非甾体类抗炎药物时,结果常不令人满意。失败的一些因素是由于剂量低和疗程太短,当疾病仍然处于活动期时中断了治疗,可通过持续性C反应蛋白升高来证明。应该使用适当剂量的非甾体类抗炎药物(如阿司匹林2~4g/d,吲哚美辛75~150mg/d,布洛芬1 600~3 200mg/d),直到C反应蛋白完全正常化,尤其是在皮质类固醇减量过程中。应该根据医生的经验和患者的病史(如,宁愿选择以前治疗有效的非甾体类抗炎药物)和合并症的情况,如合并缺血性心脏病的患者或者已经接受阿司匹林治疗或需要抗血小板治疗的患者,宁愿选择阿司匹林。吲哚美辛和其他的非甾体类抗炎药物应该避免在冠心病患者中使用。
最佳的治疗持续时间是有争议的,应该尽可能的参考C反应蛋白,不仅是心包炎的诊断,也是疾病处于活动期,指导治疗和治疗持续时间的指标,不过还没有很好确定何时需要逐渐减量的问题。
(2)秋水仙碱:开始提出的是秋水仙碱治疗复发的心包炎,少量的回顾性研究支持使用秋水仙碱治疗心包炎复发的病例,在2004年欧洲指南中,推荐秋水仙碱治疗复发的心包炎是有用的(Class I),在急性心包炎中选择使用可能有用(ClassⅡa),推荐的剂量是2mg/d使用1~2d,紧接着维持剂量1mg/d。在随机试验中,秋水仙碱明显减少心包炎的复发率,且在治疗过程中,没有观察到严重的药物副作用。不过秋水仙碱的治疗作用还有一些疑问,理由是秋水仙碱只能作为一种辅助药物,几乎是与非甾体类抗炎药物或皮质类固醇联合使用才能显示效果,单一的秋水仙碱治疗无效;同时,秋水仙碱也只能使心包炎的复发率减半,不能清除所有的复发。在C反应蛋白正常的慢性心包积液中,秋水仙碱一般无效;还有因胃肠不能耐受而停药的情况。在临床上也能适当的调整药物剂量来改善顺从性,开始使用低剂量,如果能耐受再逐渐增加剂量。
(3)皮质类固醇:虽然建议皮质类固醇用于阿司匹林和其他非甾体类抗炎药物无法忍受的、禁忌证或真正失败的患者,但是这类药物在临床上使用是相当普遍的,尤其是复发的心包炎患者。主要原因是皮质类固醇能快速控制和消除的症状。不过,治疗通常快速减量,因为担心可能的副作用,严重的副作用常与长期使用药物有关。此外,皮质类固醇可能是心包炎复发的一种危险因素,因为可能损害病毒的清除。因此,心包炎的复发与皮质类固醇依赖是心包炎患者比较棘手的问题。
近来的回顾性、非随机的研究挑战高剂量皮质类固醇的使用。100例复发的心包炎患者被分成2组,1组使用“低”剂量的泼尼松(每天0.2~0.5mg/kg),另1组使用泼尼松每天1.0mg/kg,维持4周,然后慢慢减量。在随访中,高剂量泼尼松组严重的副作用发生率高(23.5%对2.0%,P=0.004),复发率(64.7%对32.6%;P=0.003)和疾病有关的住院率(31.4%对8.2%;P=0.008)也高。观察到的严重并发症大多是骨折,因此长期使用皮质类固醇要预防骨质疏松。
在症状消除和C反应蛋白正常化后,小剂量的减少用量是治疗成功的关键,类似于风湿性多发性肌痛的处理。复发的关键阈值是10~15mg/d的泼尼松的量,在此剂量时,应该非常缓慢的减少泼尼松的用量,每2~6周减少1.0~2.5mg。如果在减量过程中症状复发,应该不增加剂量或重新制订皮质类固醇计划,应该开始或增加阿司匹林或非甾体类抗炎药物的剂量控制症状。在减量过程中,应该考虑使用秋水仙碱,开始时低剂量,即0.5~0.6mg。
四、复发与难治病例的处理
类固醇减量后复发的病例(很常见)不应该考虑为难治性,难治病例的定义应该是需要无法接受的高剂量和长时间的皮质类固醇才能控制的病例(即,泼尼松每天>25mg),可能占复发病例的5%以下。在这种情况下,文献报道已经使用了几种药物(咪唑硫嘌呤、环磷酰胺、环孢素、甲氨蝶呤、羟化氯喹、静脉内免疫球蛋白、白介素受体阻滞药),如果能耐受,优先选择咪唑硫嘌呤(常规剂量每天2~3mg/kg),但是应该意识到缺乏强烈的证据支持资料。应该优先选择较少毒性和较廉价的药物(如,咪唑硫嘌呤或甲氨蝶呤),剂量的个体化和医生的经验以及知情同意是重要的。很多病例可考虑皮质类固醇、阿司匹林或一种非甾体类抗炎药物,加秋水仙碱三种药物联合治疗。
反复发作的特发性心包炎是否进展为缩窄性心包炎存在争议,然而,系统性回顾1966—2006年发表的资料,包括230例特发性反复发作的心包炎随访61个月,显示预后良好,并发症罕见。尽管这些患者无数次复发,没有报道缩窄性心包炎,总的风险比特发性急性心包炎低(约1%)。
五、心包穿刺和活检
当出现明显的心包积液时,如果怀疑特异性病因或不能通过其他方法进行诊断的心包炎,必须进行诊断性穿刺;药物治疗难以控制的大量或有症状的心包积液也考虑心包穿刺。可以通过透视或超声心动图引导进行心包穿刺。如果抽出不凝的血性液体,实际上是亚急性和慢性积液的心包内纤溶激活阻止血凝块的发生;然而心包内急性出血,抽出液可能出现血凝块。能在透视下注射造影剂或在超声心动图观察下注射振荡的生理盐水以排除穿刺心腔。超声心动图引导心包穿刺是安全的,除了标准的剑下穿刺部位外,还能引导不同途径的心包穿刺。临床医生能通过超声心动图选择最好的穿刺点,也就是最接近大量心包积液的部位。反复发作的心脏压塞患者,外科引流的过程中可进行心包活检,也被用于疾病持续3周以上而没有明确诊断患者的病因查找。心包镜的靶向活检对诊断肿瘤性心包疾病特别有用。
六、心包剥离、心包开窗和其他干预技术
心包剥离术对频发的、有明显症状的、抵抗药物治疗的复发患者可能是有用的(Class IIa)。其他报道的心包剥离术指征包括反复发作的心脏压塞、以及类固醇毒性证据的患者。不过,对于反复发作的特发性心包炎,一般认为心包剥离术的疗效值得可疑。因为一些患者心包剥离后症状消除,但是也有很多患者的症状无变化或改善或消失一段时间后再现。到目前为止,反复发作的心包炎心包剥离术的指征是基于专家的意见,而不是被证明有效。当然,永久性缩窄性心包炎的心包剥离术利益已获得肯定;然而争论性议题是诊断的心包缩窄后,心包剥离的时机选择问题。据报道9%的急性特发性积液性心包炎患者有暂时的缩窄,在心包积液已经消失或微量时的亚急性阶段记录到缩窄的特征。212例通过药物治疗显示心包炎消退后的2个月至2年,超声心动图显示36例患者(17%)有缩窄性心包炎表现。通过非甾体类抗炎药物、类固醇、抗生素、化疗、血管紧张素转化酶抑制药和利尿药的治疗,5例患者缩窄消失。因此,在缺乏永久性和慢性证据的情况下,血流动力学稳定的患者,在推荐心包剥离术前,能给予试验性保守治疗[非甾体类抗炎药物和(或)皮质类固醇]2~3个月。
肿瘤性心包积液的治疗主要来源于经验,对于反复发作的有症状积液患者选择创伤较小的技术,包括更长时间的导管引流和“心包开窗”技术。心脏压塞或大量心包积液的患者,通过经皮穿刺,有时留置导管能容易获得初步缓解。更长时间的导管引流是一种预防液体再聚集的有效方法,虽然导管引流比液体自身排泄更容易激发炎症和闭塞心包腔。导管引流可能需要几天,直到引流量小于20~30ml/24h前,不应该拔除导管。可替换的方法包括外科心包开窗术,可选择传统的心脏外科或视频辅助的胸腔镜来进行,与心包穿刺引流相比,再发积液的可能性较低。
球囊心包分离术是外科心包窗的一种可替换技术,尤其是为了改善恶性和生命期望值减低的患者生活质量而采用。在透视引导下,从剑突下途径插入的单球囊或双球囊导管进入心包腔。虽然这一技术在超过80%的患者中取得成功,但是扩张心包通常很痛,因此建议适当麻醉;已经报道的并发症包括发热(达到28%)、气胸或胸管引流(达到20%),以及罕见的心包血管出血。
七、小 结
心包炎的最常见病因可能是特发性或病毒性的,心脏压塞是威胁生命的临床综合征;超声心动图是心包积液诊断中最敏感和最准确的工具,然而,一些患者的缩窄性心包炎诊断还有一定的困难,尤其是与限制性心肌病的鉴别诊断;明确病因才能获得靶向治疗;对于常见的特发性或病毒性心包炎的治疗,应该首选阿司匹林或非甾体类抗炎药物。应该限制皮质类固醇的使用,开始时使用低剂量可能与高剂量有同等的或更好的效果,同时副作用减少。秋水仙碱对于预防炎症性心包综合征的复发可能是有用的。心包穿刺是心脏压塞、大量或有症状的药物难治性心包积液患者的指征;永久性慢性缩窄性心包炎患者应该考虑心包剥离术。
(王 强 黄新胜)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















