毛细胞白血病(HCL)是B细胞恶性病,曾称为组织细胞白血病,幼稚型髓性脾组织淋巴细胞增多症、网状细胞白血病、白血病性网状内皮细胞增生症和淋巴样骨髓纤维化,占淋巴白血病中2%。男多于女,男女比值为5∶1,中数发病年龄50岁,可有家族史。
(一)临床表现
1/4以腹部胀满不适,1/4以疲乏、消瘦,1/4以出血或感染及1/4以其他原因为首发,始发现血象异常及脾大。85%有脾大,很少有浅表淋巴结肿大,<10%淋巴结肿大>2cm,可能毛细胞缺乏L-选择素,故侵犯淋巴结者少,CT和尸解发现有75%患者有内部淋巴结肿大。偶有肝大,浸润软组织更为少见。通过α4β1整合素和血管细胞黏附分子(VCAM)-1与内皮细胞相互作用,回归至脾、肝和BM的VCAM丰富区。毛细胞可弥漫性聚集于肝窦和门脉区,但肝大者少见。
HCL可伴有系统性自身免疫性疾病如硬皮病、多肌炎、结节性多动脉炎和皮肤血管炎。偶可以此为首发表现。偶可有溶骨性病变,常见于股骨近端。
(二)临床分型
分两型,临床、血液学及免疫学特征不尽相同,有预后意义。
1.经典型(Ⅰ型) 多为老年人,男女之比为4∶1。以孤立性脾大,全血细胞减少,单核细胞减少,有特征性毛细胞为特点。该细胞比小淋巴细胞大1~2倍,核质比值低,胞质淡蓝可有嗜天青颗粒,细胞边缘不齐呈锯齿状,表面有许多绒毛状突起,核圆、椭圆或肾形或单核样,染色质疏松,核仁不明显。NAP积分高。耐酒石酸酸性磷酸酶(TRAP)阳性。TRAP有诊断意义,HCL 100%阳性。标本采集后趁新鲜立即以细胞化学法不用免疫组化法检查,久置再做易假阴性。因为TRAP在空气干燥后不稳定,也不能用石蜡包埋标本。免疫表型表达全B细胞表面分化抗原:sIg+、CD19+、CD20+、CD22+、CD25+,CD79a+、CD79b-亦可表达早期浆细胞标志:PCA-1。还可表达不常见于正常B细胞(<3%可表达)的其他表面抗原如CD11c(β2整合素α链,也表达于单核细胞和中性粒细胞)、CD103(人黏膜淋巴细胞抗原-1,HML-1,主要表达于上皮内T细胞)。这三种抗原对经典与变异型HCL及与其他B-LPD有鉴别价值,如CD103阳性并有其他全B抗原阳性,强烈支持HCL诊断。CD5、CD23、CD10阴性。BM象增生活跃,10%~20%增生低下。毛细胞可弥漫性或斑片状浸润,可见残留造血细胞,粒系减少较红系和巨核系明显,易见肥大细胞。骨髓活检显示细胞核在半透明浆中,呈荷包蛋样现象为特征性变化。网硬蛋白纤维中度至显著增加,有时网硬蛋白围绕毛细胞。电镜超微结构显示胞质中有核糖体板层复合物。脾病理以红髓受累,假窦形成,白髓萎缩为特点,髓索增宽。2/3患者有克隆性异常,细胞遗传学累及染色体1、2、5、6、11、19、20,可有11q13易位,过度表达周期素D1mRNA,累及5号染色体者约40%,主要为+5、5q13-,可能对HCL发生重要。此型HCL对IFNα治疗有效。
2.变异型(Ⅱ型HCLv或vHCL) 至少有四种,幼淋细胞HCLV、原始细胞HCLV、HCLV和HCL/CLL混合型。临床表现除脾大外,可有淋巴结肿大。白细胞数增高常>50×109/L。不伴中性粒细胞和单核细胞减少。与Ⅰ型比较,细胞毛状突起较少且短,核质比更高,核染色质更为致密,核仁清晰。TRAP弱或阴性。无骨髓纤维化。超微结构无核糖体板层复合物。免疫表型为CD19+、CD20+、CD22+、CD25-、CD103-、CD11c-,κ/λ<0.55。此型可能为HCL和PLL混合中间型,IFNα治疗无效。
Johnson等报道1例不典型HCL,不同于经典HCL亦不同于HCLV、SLVL,可能为HCLV又一亚型。该例毛细胞为典型毛细胞,CD19+、CD20+、CD11c-、CD25-、CD103-、TRAP+、κ/λ为1/4,脾病理显示红髓明显为异常淋巴细胞取代,而白髓无异常。
早在1976年,我院报道了国内首例HCL。患者男性,49岁,于1976年4月因眩晕、耳鸣4个月,双眼视物模糊、复视1个月,言语不清,不能行走10日,以椎-基动脉血栓形成收住脑系内科。后发现肝、脾大,血红蛋白76g/L,白细胞78×109/L,血小板60×109/L,中性粒细胞0.02(2%),淋巴细胞0.15(15%),淋巴样细胞0.83(83%),瑞氏染色下,细胞质灰蓝,不透明,边缘不齐呈锯齿状,伪足状或瘤状突起,质内有的有颗粒,核圆或卵圆,中位或稍偏,染色质粗松,核膜清晰,多无核仁,有的1~2个。BM象增生活跃,以淋巴样细胞为主76%,形态同血象,可见浆细胞。BM活检为一致圆形细胞呈荷包蛋样,网硬蛋白纤维不多,相差显微镜观察活体细胞,显示胞质不齐,有绒毛突起或伪足状,活动变形,诊为HCL。以中药补气养血、开窍化淤,病情好转,出院失访。此例当为HCLV。
(三)分期
Ⅰ期:具备以下情况之一:①Hb>120g/L,脾肋缘下≤10cm;②Hb>85g/L,脾肋缘下<4cm。
Ⅱ期:具备以下情况之一:①Hb>120g/L,脾肋缘下>10cm;②Hb85~120g/L,脾肋缘下4~10cm;③Hb<85g/L,脾肋缘下<4cm。
Ⅲ期:具备以下情况之一:①Hb 85~120g/L,脾肋缘下>10cm;②Hb<85g/L,脾肋缘下>4cm。
(四)诊断与鉴别诊断
诊断HCL主要依据是在PB和或BM中发现毛细胞并有其独特生物学特征。
1.国内诊断标准
(1)临床表现。多有脾大、贫血、可伴有发热。
(2)实验室常规检查有血红蛋白减低,白细胞可明显增高、正常或降低,血小板减少或正常。BM增生活跃,也可“干抽”。
主要依据是在PB和(或)BM见到毛细胞,其特征:光镜下大小不一,胞质中等量,瑞氏染色呈天蓝色,周边不规则,呈锯齿状或伪足突起,有时为细长毛发状。核呈椭圆,可有凹陷,偶见核仁。相差镜下新鲜活体标本中的毛细胞有细长毛发状突起。扫描电镜可有延伸的毛,有交叉现象。透射电镜下在胞质内可见核糖体板层复合物(RLC)。细胞化学PAS+、ACP+、TRAP+、α-NAE+不被氟化钠抑制。免疫表型:sIg+、CD19+、CD20+、CD21-、CD22+、CD11c+、CD25+、CD103+。体外培养对小剂量咐醇酯(TPA)反应极为迅速,24h内细胞完全贴壁,并伴有长枝状突起,幼淋细胞白血病无此反应。BM病理显示增生活跃或减少,毛细胞多呈散在或簇状分布。胞质丰富、透明,胞核间距离宽,呈蜂窝状。核染色质细,呈毛玻璃样,网状纤维轻度或增多。
2.国外诊断标准
(1)临床表现有脾大、消瘦、反复感染,易合并血管炎。
(2)实验室常规检查多有全血细胞减少,也可仅表现为两系或一系细胞减少,BM经常“干抽”。
主要依据为PB中毛细胞形态学特征(如前述),酸性磷酸酶同工酶5阳性,不被酒石酸抑制。免疫表型:sIg(M±D,G或A)阳性,B细胞相关抗原CD19+、CD20+、CD22+、CD79a+、CD11c强阳性,CD25强阳性,CD103和HC2阳性。CD5-、CD10-。BM病理呈弥漫性、间质性浸润,核小、间隙大,网状纤维增多。免疫组化CD103+、annexinA1+(ANXA1+)。
变异型(HCL-v)特点:①发病年龄较高(中位发病年龄70岁);②通常白细胞数>10×109/L;③不典型毛细胞具有幼淋细胞形态特点;④CD25-,有时CD103-,TRAP-;⑤疗效不佳。
3.诊断HCL免疫表型积分 CD11c+、CD25+、CD103+、CD123(IL-3Rα)+四联,各为1分,>90%经典HCL为3~4分。CD11c+亦可见于B-CLL、SMZL/SLVL,但HCL表达CD11c+强度要强30倍。CD25+也可表达于B-CLL、SMZL/SLVL,但HCL表达CD25极其恒定。HCLv、B-CLL、B-PLL、SMZL/SLVL绝不会同时表达CD11c、CD25和CD103,而且CD123阴性,故四联积分仅1~2分。
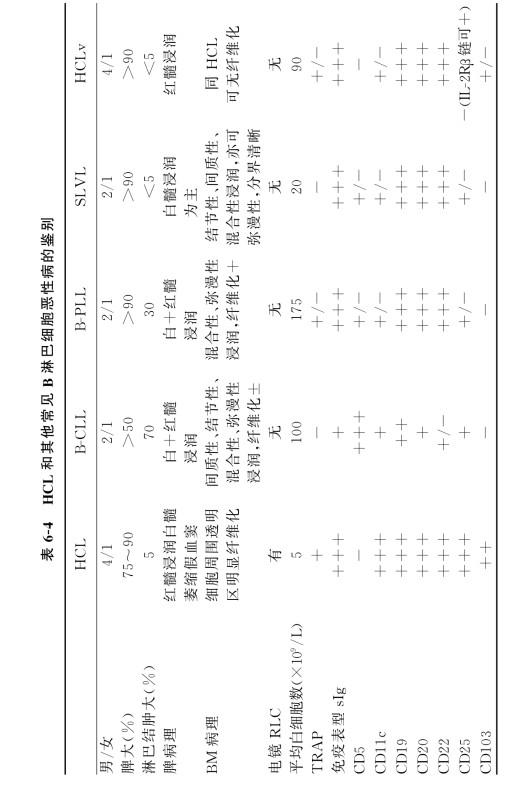
4.鉴别诊断 HCL主要与CLL、PLL、脾边缘区淋巴瘤(SMZL)或有血循绒毛淋巴细胞的脾淋巴瘤(SLVL)区别,见表6-4。
2008年Traverse-Glehen等报道37例伴嗜碱性毛淋巴细胞脾红髓淋巴瘤(splenic red pulp lymphoma with numerous basophilic villous lymphocytes,SRPLBL),与HCL、HCLv、SMZL/SLVL有重叠又不同,建议作为独立病,见表6-5。2008年WHO将SRPLBL和HCLv作为脾淋巴瘤/白血病未分类的暂定亚型。
BM常伴网硬蛋白纤维化,有时致BM增生减少加之全血细胞减少而似再生障碍性贫血。毛细胞浸润被残存的造血细胞所掩盖。CD20免疫组化染色可显露这些隐伏的毛细胞。有时BM浆细胞增多,如浆细胞形成结节或形态不典型,应作Ig轻链检测或CD56、CD28、CD31、CD19、CD20以区别为反应性浆细胞或多发性骨髓瘤。后者有轻链限制,CD56、CD28阳性而CD19、CD20、CD31阴性。


HCLv BM活检标本中毛细胞可呈梭状类似肥大细胞,但B系标志阳性,而且肥大细胞标志溶酶体和类胰蛋白酶阴性可资鉴别。HCL有BM纤维化/脾大也应与慢性特发性骨髓纤维化区别,后者为髓系增殖性疾病,不表达B系抗原,两者鉴别不难。要注意有时HCL与CLL同存。Rosa等报道68岁无症状性双系血细胞减少,无肝、脾、淋巴结肿大,血红蛋白124g/L,白细胞1.8×109/L,血小板83×109/L,形态正常。BM增生减少,53%成熟小淋巴细胞,4.5%毛细胞,BM活检符合HCL。免疫表型有两群成熟B克隆,20%为CD19+、CD20+、CD5+、κ轻链阳性,6%为CD19+、CD20+、CD25+、CD11c+、CD22+、CD23+、CD5-。细胞遗传学正常。以DCF 1mg/m2,4d,其后PB正常,8%成熟淋巴细胞,BM中亦无毛细胞,血液学缓解持续1年,免疫表型未检出毛细胞,B-CLL有2.5%。HCL与CLL同存,临床与血液学表现均与HCL和CLL各自典型临床和血液学表现不同。
(五)治疗
HCL为惰性,进展缓慢,确诊后不一定立即治疗,如有下列指标之一应治疗:①症状性肝、脾大或淋巴结肿大;②血红蛋白<100g/L,或需输血;③血小板<100×109/L,或有出血;④白细胞>20×109/L;⑤中性粒细胞<1×109/L;⑥伴有自身免疫性疾病;⑦反复或严重感染;⑧有发热、疲乏、盗汗等症状;⑨骨病。
脾脏切除、IFNα单作为HCL治疗的主要措施,自嘌呤类药物问世,对HCL有较好疗效,对初治HCL以此药为首选。
1.嘌呤类药物 常用有2-氯脱氧腺苷(2-chlorodeoxyadenosine,cladribine,2CdA,2CDA)、2-脱氧可福霉素(2-deoxycoformycin,pentostatin,DCF)和氟达拉滨(fludarabine,FDR),尤以2-CDA和DCF应用较广。
2-CDA为耐腺苷脱氨酶(ADA)而不抑制之的嘌呤类药物,以三磷酸CDA积集于富含脱氧胞苷激酶的淋巴细胞内干扰RNA合成和DNA修复,导致细胞凋亡。Dearden等以2-CDA 0.1mg/(kg·d),iv,每月用7天,治疗45例,38例(84%)CR,7例(16%)PR。中数23.5个月复发13例。5例复发者再用2-CDA仍有效,4例CR,1例PR。Robak等以0.12mg/(kg·d),iv,2h,每月用5天,治疗Ⅰ型HCL 97例,75例(77.3%)CR,8例(18.6%)PR。Ⅱ型HCL 6例,仅2例PR。复发20例中10例再用2-CDA,7例又CR,3例PR。故一般不发生耐药,初治与复治疗效无差异。Saven等0.087mg/(kg·d)或0.1mg/(kg ·d),持续静脉滴注7天,治疗349例,一个疗程CR者319例(91%),中数30个月复发76例(24%),再治62%CR。发生第二肿瘤27例(8%)。恢复时血小板最先,中性粒细胞次之,血红蛋白最慢。2-CDA亦可皮下注射。如中性粒细胞重度减少0.2 ×109/L,应小剂量0.05mg/(kg·d),脾切除不影响疗效,对其他药物难治者也有效。Tallman等建议对初治HCL用0.1mg/(kg·d),持续静脉滴注7天,一般1个疗程,对用过1个疗程而复发者再用2-CDA,若已用过2个疗程2-CDA复发者则换用DCF(4mg/m2,iv,每2周用1次,3~6个月)或IFNα2MU/m2,每周3次,12~18个月。Robak等以2-CDA 0.12mg/(kg·d),iv,2h,5天或每周1次,6次,分别治疗26例和25例,CR分别为69%和76%。副作用较轻,除BM毒外,可致CD4+T细胞长期减少,引起免疫调节障碍,发生自身免疫现象,如免疫性溶血性贫血,多在2~4疗程或停药后2周内发生。此外,输注血制品时应先照射处理,否则易发生输血相关性GVHD,甚至危及生命。2-CDA已成为治疗HCL的一线标准方案。
DCF不可逆抑制淋巴细胞嘌呤代谢重要的ADA使三磷酸脱氧腺苷积蓄破坏淋巴细胞。一般用量4mg/m2,静脉冲注,每周或每2周1次,2个疗程,可有血液学改善,2个月内可恢复正常。Dearden等以DCF 4mg/m2,1~2周1次治疗165例,132例(82%)CR,25例(15%)PR,中数51.5个月(14.2~105.4个月)40例(24%)复发。8例复发者仍用DCF,5例再次CR,2例PR。有用4mg/m2,每2周1次,87%CR;4mg/m2,每周1次,连用3周后每8周1次,89%CR;也有用5mg/m2,每2周连续用2天,64%CR,20%PR。剂量加大并不能提高CR。对其他治疗无效者亦能奏效。7年无复发存活率可达91%,8年存活率87%±2%,Rosa等用DCF 1mg/m2,4天治疗1例HCL与CLL并存的病例,毛细胞克隆全消失,而B-CLL克隆还有0.025(2.5%),提示剂量减少,用药天数增加也能有效。副作用轻,除BM毒外,可有神经毒、皮疹、结膜炎、肝毒性、可逆性肾功能减退。亦可致CD4+T细胞缺乏。输血可发生输血相关性GVHD,用药期间对所有输用的血制品应照射。由于药物自肾清除,治疗前肌酐清除在50~60ml/min,剂量应减半为2mg/m2。
FDR为单磷酸氟化腺苷衍生物,抗ADA,亦可应用。25mg/m2,iv,30min,每3~4周连用5天。可使复治HCL PB正常,FDR的应用不如2-CDA与DCF广。
嘌呤类药物最突出的问题为免疫抑制,总淋巴细胞数减少,T细胞下降比B细胞与NK细胞为显著,CD4和CD8+T细胞在停用DCF后下降至<0.2×109/L至少可达6个月之久。用DCF或2-CDA CD4+T细胞恢复正常的中数时间分别需要54个月和40个月。若不与皮质激素合用,感染机会并不多见。
2.干扰素(IFN)α 有重度血细胞减少和嘌呤类药物治疗无效者可用,对Ⅰ型疗效较好。IFNα3MU/d或每周5天,或2MU~3MU/m2,每周3次,连用6~12个月,43%可CR,90%可PR。停药后2年内50%可临床复发,复发后再用多数患者仍有效。恢复时血小板为先,血红蛋白和白细胞继之。Pettitt等比较IFNα和嘌呤类药物治疗HCL的疗效,说明前者较后者差,CR少,PR多,长期生存少,发生第二肿瘤机会多(表6-6)。
表6-6 IFNα、2-CDA和DCF疗效比较

于治疗结束患者BM毛细胞>0.30(30%),血小板<100× 109/L易早期复发。变异型及CD5+者对IFNα反应差。IFNα可与其他药物合用,亦可长期维持应用。
3.脾切除 适应证有:①巨脾引起腹部不适;②脾梗死、脾破裂;③脾功能亢进,明显血细胞减少;④输血依赖性;⑤继发于粒细胞减少的反复感染,继发于血小板减少的出血;⑥系统药物治疗无效。切脾后90%患者血象可很快改善,40%~70%三系血细胞可恢复正常,单不能减少BM毛细胞。疗程可维持18个月,5年存活率70%。
4.化疗 可参照治疗B-CLL化疗方案。有用大剂量MTX 2g/m2,iv,1h,四氢叶酸钙25mg/m2,每1/6h,8~12次,每6周1个疗程,6个疗程治疗6例脾切除后复发者,5例有效。由于HCL表达CD20故可于化疗方案中加Rituximab。
复发者用嘌呤类药物及IFNα仍有效。10%HCL为原发性耐药,晚期可获得耐药,治疗困难,可联合治疗和切脾。亦可试用ATO和Rituximab。HCL继发性恶性病发病率2.4%~19%,用IFNα后继发性恶性病多为造血系统肿瘤;嘌呤类药物继发者多为实体瘤。Al-Fiar等以2-CDA 0.09mg/(kg·d),7天,治疗1例HCL,CR 4年后发生AML-M5b,无HCL迹象。继发性肿瘤多发生在治疗后13~114个月。
5.单克隆抗体 HCL高表达全B抗原CD20,故可用利妥昔。标准用法为375mg/m2,每周1次,共4~8次。常先用2-CDA5.6mg/m2,iv,2h,5天,于第28天用标量利妥昔共8次,治疗初治HCL13例,全部CR,除2例外MRD也消失。由于HCL表达CD20有异质性,可用IL-4、G-CSF、GM-CSF以增强其表达再用利妥昔。92%~100%HCL表达CD52,故可用人化抗CD52阿仑单抗(alemtuzumab,campath1H,Alem)剂量可参阅CLL治疗。一般用于2-CDA±利妥昔难治者,尤其是HCLv。此外,HCL和HCLv强表达CD22,亦可考虑用抗CD22单抗epratuzumab。还有抗CD25重组免疫毒素LMB-2或抗CD22免疫重组毒素BL22等可据情选用。
(六)疗效标准
1.国内疗效标准
(1)CR:症状与体征完全消失,血象恢复正常(血红蛋白≥120g/L,中性粒细胞绝对值≥1.5×109/L,血小板≥100×109/L);PB和BM毛细胞消失或BM中毛细胞<0.05(5%);BM活检无HCL,网状纤维恢复正常。
(2)PR:以上各项均有改善,但未恢复正常,血象三系细胞应有两系恢复正常,PB及BM中毛细胞减少≥0.50(50%)。
(3)进步:以上各项指标有进步。血象三系细胞至少一项恢复正常或接近正常;PB及BM中毛细胞减少<0.50(50%)。
(4)NR:以上各项指标均未恢复正常。
2.国外疗效标准
(1)脾切除术:术后2~3个月确定疗效。
①CR:血红蛋白≥110g/L,中性粒细胞>1×109/L,血小板≥100×109/L。
②PR:血象至少有一系上升到以上标准,粒细胞绝对值必须接近正常。
③NR:术后全血细胞短暂上升后下降,需加其他治疗。
(2)药物治疗
①CR:临床上无脏器肿大,血象恢复正常(血红蛋白≥120g/L,中性粒细胞>1.5×109/L,血小板≥100×109/L),不需输血,PB和BM中毛细胞消失,BM活检证实缓解,网状纤维正常。
②PR:血象恢复正常如上,BM涂片或活检毛细胞数较治疗前减少≥50%或<50%。
③进步:血象中任何一系细胞改善或恢复正常。
④NR:以上各项均未达到标准。
3.Ravandi等2006年用利妥昔疗效标准
(1)CR:无器官肿大,BM无毛细胞或BM/PB毛细胞<0.01(1%)。在不用生长因子或不输血支持下,ANC≥1.5× 109/L,Hb≥120g/L(女≥110g/L),血小板≥100×109/L。
(2)CR-RD:同CR,但BM毛细胞0.01~0.05(1%~5%),PB中无,为CR有残留病。
(3)PR:以下二者有一:①PB与CR-RD同,但BM毛细胞>0.05(5%);②至少有1系血细胞改善50%,其他系不减少,肿大器官缩小≥50%,BM/PB中毛细胞减少≥0.50(50%)。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















