慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)为单一性小圆形成熟样CD5+B淋巴细胞增生,可混以少量幼淋细胞,使淋巴组织结构消失,血液和骨髓内淋巴细胞增高,肝、脾淋巴结肿大。CLL在欧美发病率高,占慢性白血病≥50%,全部白血病的25%。我国CLL发病率低,占慢性白血病<10%,全部白血病<4%。90%发病年龄>50岁,30岁以下患者少见,小儿则极罕见。男女比例为2∶1。在非霍奇金淋巴瘤(NHL)中CLL/SLL约占6.7%,所谓SLL为组织形态学和免疫表型与CLL同但不是白血病期。换言之,两者为同一疾病的不同表现。患者在发病时有脏器肿大未累及PB和BM为SLL;而发病时就累及PB和BM[淋巴细胞占有核细胞≥0.40(40%)]为CLL。重点讨论CLL。
(一)临床和血液学特征
多无症状,有的可无脏器肿大偶因其他原因查血常规始发现。也有感疲乏、无力。也有以溶血性贫血为首发表现者。最常见体征为浅表淋巴结肿大,随病程进展,可由少增多,由小变大,肝、脾尤以脾逐渐增大,有个别患者以脾大显著而淋巴结不肿大或轻度肿大,有的可表现为纯红再障、无巨核细胞性血小板减少或再生障碍性贫血和肾病综合征。少见的临床表现有免疫性血细胞减少、副肿瘤天疱疮、渗出性胸膜炎等,并可作为首发表现。
血象最显著表现为白细胞增多,淋巴细胞绝对数增多,可从5×109/L至500×109/L,多>20×109/L,细胞形态和正常小淋巴细胞一样核染色质致密,核仁不明显或无,胞质少,天蓝色透明,无颗粒,涂抹细胞和篮状细胞明显增多。较大带有核仁的幼淋细胞少见为0.02(2%),如>0.10(10%)而<0.55(55%)则为CLL亚型有幼淋细胞增多,诊为CLL/PL。红细胞和血小板数早期正常,后期减少,10%~25%并发自身免疫性贫血或自身免疫性血小板减少时可分别表现溶血性贫血或血小板减少,血片中有小球形红细胞和血小板减少。粒细胞绝对数可正常或减少。
BM增生明显活跃,淋巴细胞明显增多,形态与PB中一致,占0.40(40%)以上。其他系造血细胞在早期均可见到,晚期几乎全为淋巴细胞。原淋巴细胞一般<0.02(2%),幼淋巴细胞<0.10(10%),如>0.10(10%)应为CLL/PL或CLL幼淋变。如转变为弥散性大B细胞淋巴瘤(DLBCL,Richter综合征),则BM可见类似中心母细胞或免疫母细胞样的融合成片的大细胞。BM活检可呈结节性、间质性或弥散性浸润。
免疫表型:CD5+、CD19+、CD20弱、CD22弱、CD79a+、CD23+、CD43+、CD11c弱、CD10-、FMC7-、CD79b-;细胞表面IgM或IgM+IgD弱表达。细胞周期素D1-。有少数有典型CLL形态学但免疫表型远非典型,表现为CD5-、CD23-、FMC7+、CD11c+、sIg强或CD79b+。
80%有异常核型:50%有13q14缺失,20%有+12,20%有11q22-23缺失,10%有17p13(P53位点)缺失,15%有6q21缺失。
免疫球蛋白可降低,但5%患者有单克隆IgM增高。
(二)分期
CLL分期有预后意义,国际上常用有Rai、Binet和国际CLL工作组提出的分期。
1.国内临床分期
Ⅰ期:淋巴细胞增多,可伴有淋巴结肿大。
Ⅱ期:Ⅰ期+肝大或脾大或血小板减少(<100×109/L)。
Ⅲ期:Ⅰ期或Ⅱ期+贫血(血红蛋白<110g/L)。
2.Rai临床分期及其修订分期
0期:仅有淋巴细胞增多(PB淋巴细胞绝对值≥15×109/L, BM淋巴细胞≥0.40(40%),中数生存>120个月,为低危。
Ⅰ期:0期+淋巴结肿大,中数生存95个月,为中危。
Ⅱ期:0期+肝和(或)脾大,有/无淋巴结肿大,中数生存72个月,为中危。
Ⅲ期:0期+贫血(血红蛋白<110g/L),有或无肝、脾、淋巴结肿大,中数生存30个月,为高危。
Ⅳ期:0期+血小板减少(<100×109/L),有或无贫血,肝、脾、淋巴结肿大,为高危,中数生存30个月。
Rai修订分期按危度分低危、中危和高危。0期为低危,Ⅰ、Ⅱ期为中危,Ⅲ、Ⅳ期为高危。
3.Binet等分期 除淋巴细胞增多外,将身体淋巴组织分为5个区域即颈淋巴结区(单侧或双侧,含Waldeyer环)、腋下淋巴结区、腹股沟淋巴结区、脾脏和肝脏。
A期:0~2个淋巴结区肿大,血红蛋白>6.2mmol/L(>100g/L),血小板>100×109/L,中位数生存>120个月。
B期:3~5个淋巴结区肿大,血红蛋白>6.2mmol/L(>100g/L),血小板>100×109/L,中位数生存61个月。
C期:0~5个淋巴结区肿大,血红蛋白<6.2mmol/L(<100g/L),血小板<100×109/L,中位数生存32个月。
4.国际CLL工作组(IWCLL)分期 将Rai和Binet等分期综合。
低危:A(0)。
中危:A(Ⅰ)、A(Ⅱ)、B(Ⅰ)、B(Ⅱ)。
高危:C(Ⅲ)、C(Ⅳ)。
由于Rai和Binet等分期应用方便,故广为临床血液学者们采用。CLL血细胞减少原因有:自身免疫性和CLL骨髓浸润致骨髓衰竭,前者预后较好。上述分期均未提及是何机制使血细胞减少,故有可能分期虽晚属高危,但预后不一定差。
5.BM活检组织病理学分型 Grisler等将BM中CLL细胞浸润分为4型:结节型(N)、浸润呈结节状、分界清晰、结节中无造血细胞,主要分布于骨小梁间中央,少见,主要为A期。
间质型(I):浸润散在,可很轻,脂肪细胞和造血细胞各>15%。
混合型(M):为结节型与间质型混合。
弥漫型(D):重度间质型浸润(HI)有0.05~0.15(5%~15%)的脂肪细胞或造血细胞。
弥漫性聚集者(DP):脂肪细胞与造血细胞<0.05(5%),淋巴细胞≥0.80(80%),主要于B、C期。
(三)诊断标准
1.国内诊断标准
(1)临床表现:①可有疲乏、体力下降、消瘦、低热、贫血或出血表现;②淋巴结(包括头颈部、腋窝、腹股沟)、肝、脾大;③少数人可有结外侵犯,如皮肤、乳腺、眼附属器官。
(2)实验室检查:①PB白细胞>10×109/L,淋巴细胞≥0.50(50%),绝对值≥5×109/L,形态以成熟淋巴细胞为主,可见幼稚淋巴细胞或不典型淋巴细胞;②BM增生明显活跃及以上,成熟淋巴细胞≥0.40(40%)。活检淋巴细胞浸润可分三种类型:结节型、间质型、弥漫型。
PB淋巴细胞持续增高≥3个月并可除外病毒感染、结核、伤寒、传染性单核细胞增多症等其他引起淋巴细胞增多的疾病。
B-CLL典型的免疫表型为sIgM或IgM和IgD呈弱阳性,呈κ或λ单克隆轻链型;CD5+、CD19+、CD79a+、CD23+、CD43+,CD20、CD22、CD11c弱阳性,CD10、FMC7、周期素D1阴性。
(3)形态学分型:根据幼淋细胞及不典型淋巴细胞在淋巴细胞中所占的比例不同分为三种亚型:①典型CLL:≥0.90(90%)为类似成熟的小淋巴细胞;②CLL/PL:为CLL伴幼淋细胞增多>0.10(10%)但<0.54(54%);③混合型:有不同比例的不典型淋巴细胞,该细胞体积较大,核/质比例降低,胞质呈不同程度嗜碱性染色,有少许或无嗜天青颗粒。幼淋细胞<0.10(10%)。
(4)遗传学:>80%患者有下列染色体畸变:13q14·3,11q22~23,6q21,17p13·3缺失;三体12。P53基因表达见于15%B-CLL,多为晚期或临床进展者。
2.IWCLL诊断标准 ①PB淋巴细胞绝对值>5×109/L;②BM淋巴细胞≥0.30(30%);如淋巴细胞<5×109/L,应有单克隆淋巴细胞增生。
3.NBL诊断标准 ①PB淋巴细胞绝对值>10×109/L;②BM淋巴细胞>50%。如PB淋巴细胞>20×109/L,虽无BM检查或淋巴结肿大,亦可诊为CLL。
国外亦将B-CLL根据幼淋细胞和不典型淋巴细胞所占比例分为典型或经典B-CLL,不典型淋巴细胞<0.15(15%),小淋巴细胞>0.85(85%),幼淋细胞<0.10(10%),占CLL中77%。CLL/PL在PB中幼淋细胞>0.10(10%)但<0.55(55%),为CLL和PL的中间型和不典型CLL,PB小淋巴细胞<0.85(85%),不典型淋巴细胞>0.15(15%)但幼淋细胞<0.10(10%)三类。后二类可统称为混合型或不典型CLL占CLL中23%。
4.B-CLL的免疫表型诊断积分 Moreau等以5个膜标志:CD5+、CD23+、CD22弱阳性或阴性、FMC7-、sIg弱阳性各为1分,积分为4~5分者为B-CLL,若<3分则为其他B淋巴细胞增殖性病。其后以CD79b(SN8)阴性以取代CD22,更为可靠,准确率可达96.8%。其他B细胞肿瘤为CD5-(套区细胞淋巴瘤可阳性)、CD23-、CD22/CD79b强阳性、FMC7+、sIg强阳性。
B-CLL100%CD200+,>99%CD160+,故有新免疫表型诊断积分,以CD5+、CD23+和CD160+各为1分,积分为3者为CLL,<3分为其他淋巴增殖病。少数套细胞淋巴瘤(MCL)积分亦可为3,但CD5+CD23+/CD5+CD19+细胞比值≤0.75有别于CLL的≥0.95。还有CD200在MCL为阴性,以CD200取代CD160应更好。
CD5-能否诊为B-CLL,值得进一步探讨。Huang等统计192例CD19+、CD20+的慢性淋巴增殖性病41例(21%)CD5-,均有PB与BM受累,进一步分析仅3例为CLL,但其中2例sIg强阳性,CD23-,而形态学为CLL,此种情况很少见于CLL。另1例除CD5-外,免疫表型如典型的B-CLL,但BM有大细胞转化为Richter综合征,且有非霍奇金淋巴瘤(NHL)常见的t(14;18)。前2例不能除外SLL的白血病期,余下38例分别为毛细胞白血病6例,幼淋细胞白血病2例,淋巴浆细胞淋巴瘤4例,滤泡中心细胞淋巴瘤9例,脾边缘区淋巴瘤6例,小细胞淋巴瘤有骨髓纤维化1例,不能分类的淋巴瘤10例,提示CD5-的B-CLL少见。Shapiro等报道40例CD5--B-LPD,其中CD5-CLL 15例,套区细胞淋巴瘤10例,NHL白血病期5例,血循绒毛淋巴细胞脾淋巴瘤5例,淋巴浆细胞淋巴瘤3例,CLL/PL 2例。CD5-与CD5+-CLL比较有以下特点:①分期较晚,生存期较短;②白细胞数、淋巴细胞绝对值、血红蛋白均较低,淋巴细胞形态学多不典型,幼淋细胞较多,核裂细胞常>25%,有浆细胞样淋巴细胞,幼淋细胞较多;③脾大较明显;④多有NHL的t(14;18)或+12染色体异常;⑤易转化为幼淋细胞白血病。
总之,CD5--CLL少见,应先考虑其他B-LPD包括NHL的白血病期。CD5-、CD13+、CD116+、FMC7+形态学不典型者,有+12者易向幼淋白血病转化。有的B细胞可有脑回状核与套区细胞淋巴瘤白血病期难分,后者常有t(11;14)和过度表达周期素D1。
5.B-CLL活动期的判定 确定CLL有无活动,直接涉及治疗,凡有下列之一,说明病变活动:①有B类症状如近6个月来无明显原因体重减轻10%以上,非感染性发热>38℃(>100.5℉)持续≥2周,盗汗>1个月无感染,疲乏、无力,ECOG体能状态≥2,不能工作,不能坚持日常活动等;②进行性骨髓衰竭出现贫血和血小板减少或原有加重;③有免疫性溶血性贫血和(或)血小板减少,皮质激素或其他标准治疗反应差;④淋巴结肿大(>10cm)、肝、脾(>6cm)或进行性肿大,出现压迫症状;⑤PB淋巴细胞进行性增高,分类>0.80(80%),2个月来增加>50%,倍增时间<6个月,排除其他引起淋巴细胞增高或淋巴结肿大原因;⑥BM活检为弥漫性浸润;⑦明显低丙球蛋白血症或出现单克隆 M蛋白或原有加重;⑧复杂核型异常;⑨可溶性CD23增加(>2 300U/mi)或β2微球蛋白增高(>3mg/dl),应及早治疗;⑩CLL转化。
6.冒烟性CLL和不稳定CLL 无论BM浸润型是何类的A(0)期或浸润为N型的A(Ⅰ)、A(Ⅱ)期为冒烟性CLL,生存期>7年,半数患者无恶化。Montserrat提出冒烟性CLL诊断标准为:①Binet分型A期;②BM浸润为非弥漫型;③血红蛋白≥130g/L;④PB淋巴细胞≤3×109/L,增倍时间<12个月。
不稳定CLL指非N型BM浸润的A(Ⅰ)或A(Ⅱ)期,中数进展期<2年者。
7.低淋巴细胞CLL 下列情况之一,均可诊为低淋巴细胞CLL:①PB淋巴细胞<5×109/L,BM淋巴细胞≥40%,有克隆性增生;②PB淋巴细胞<5×109/L,分类占50%以上,持续≥2个月,BM淋巴细胞>40%,临床上有肝、脾、淋巴结肿大,贫血、血小板减少等,排除引起反应性淋巴细胞增多的疾病,即使无条件作免疫表型或克隆分析亦可诊为CLL。
8.惰性(低危)和侵袭性(高危)CLL 诊断CLL后再区分为惰性或侵袭性对预测转归选择治疗策略有指导意义,见表6-1。
表6-1 惰性CLL与侵袭性CLL的区别

9.单克隆B淋巴细胞增多症(monoclonal B-cell lymphocytosis,MBL)-CLL前期 早在1984年已有人以FCM检查健康人群PB发现有与CLL免疫表型相同的(CD5+CD20dim)克隆性B细胞增多(>0.838×109/L)称为MBL,且随年龄增长而增多。≤40岁发病率0.57%,>65岁发病率6%~8%,>75岁则为8%~10%。献血员的发病率为0.14%。CLL患者家属中MBL发病率可高达13.5%~16%。MBL特点有:①无任何淋巴增殖性临床表现,体检正常;②血象正常,ALC<5×109/L,BM淋巴细胞<0.30(30%);③有IgHV重排;④MBL表型有以下几种:CD5+、CD23+、CD20dim、CD38+/-、sIgdimCLL样者占绝大多数;CD5+、CD23+/-、CD20bright、CD38+/-、sIgmod为不典型CLL样占2%;CD5-、CD23-、CD20+、CD38+、sIg+非CLL样占3%;还有CD5bright、CD23-、CD38+、仅表达sIgD常与CLL样MBL共存。CD5+CD23+CLL样MBL与CLL生物学关系密切,每年有1%~2%进展至CLL而需治疗。CLL患者家属中CD5+MBL发病率较常人高,5年内5%~33%可进展为临床CLL。MBL转归异质性可自行消失,可稳定多年,可进展为临床CLL。提示MBL至少有部分CD5+、CD23+的为CLL前期,作为CLL病谱中最为惰性的一端。
10.难治性CLL 以下情形有一即为难治:①嘌呤核苷类药物治疗无反应;②取得CR/PR后,6个月内复发或进展;③干细胞移植后12个月内复发或进展;④侵袭性CLL。
(四)鉴别诊断
B-CLL应与下列B淋巴增殖性疾病鉴别。
1.意义不明的单克隆B淋巴细胞增多症(B-MLUS) 1993年Garcia等报道一组患者PB淋巴细胞≥4×109/L,有克隆性B细胞,无症状无脏器肿大,无贫血和血小板减少,LDH不高,中数随访68个月,淋巴细胞无明显增高,亦无其他CLL相关症状与体征。为良性增生,与B-CLL恶性克隆有不同的生物学特性。B-MLUS对SAC刺激无反应,不分泌IgM,对CD40+SAC刺激也无反应,CD4+/CD8+细胞比值正常,IL-1生成正常或增高。B-CLL对SAC刺激有反应,DNA合成高,持续分泌IgM,对CD40+SAC刺激增殖活性增强,CD4+/CD8+细胞比值低。正常B细胞于SAC刺激后,DNA合成可增高,但不分泌IgM,CD40+SAC刺激后增殖能力可增强,CD4+/CD8+细胞比值正常。B-MLUS虽是B细胞单克隆增生,但接近正常B细胞的生物学特性,为良性克隆。其本质尚待进一步探讨。B-MLUS易与B-CLL的0期或A期混淆。B-MLUS为CD5-、CD23-、CD19+、CD20+而B-CLL为CD5+、CD23+、CD19+、CD20弱阳性。Byrd发现,随年龄增长,3.5%成人有意义不明的克隆性淋巴细胞增多(CLUS)但有与CLL IgVH基因突变状态,在CLL患者第一级亲属13.5%有CLUS而无CLL的临床表现,可能CLUS和CLL有共同祖细胞有不同的恶性转化过程,也可能CLL代表二种不同B细胞的恶性病,一为有突变VH基因有CLUS期,另一无VH突变的CLL而无CLUS期。可能与MBL的非CLL表型同义。
2.持续性多克隆B淋巴细胞增多症 1982年Gordon等首先报道持续性多克隆B淋巴细胞增多症(PPBL),亦称慢性B淋巴细胞增多症(CBL),为长期PB淋巴细胞绝对值增高[(5~15)×109/L],且多为不典型双核,其间有核间桥相连的淋巴细胞。多克隆IgM增高,IgG和IgA正常或降低。HLA-DR7表型者多。发病以中年女性吸烟者多。经1~2年可自发恢复或戒烟后淋巴细胞及双核淋巴细胞减少,再吸烟又复发。有这些特点不难与B-CLL区别。病因可能与EB病毒感染有关。一般为良性,但有少数于多克隆B细胞增生后出现一主导克隆。Mitterer等报道1例间断发病类似慢性疲劳综合征2年,有反复结节性多形性红斑、瘙痒、关节痛、血沉快,外周血淋巴细胞增高。多克隆B细胞为0.50(50%),免疫表型显示CD19+、CD20+、CD22+、HLA-DR+、CD23弱阳性,CD5-、CD10-,sIg为IgM/IgD,λ和κ轻链表达,高表达淋巴细胞活化抗原CD25和CD54。血清学显示IgM增高并有慢性EBV感染,认为可能为EBV长性刺激使淋巴细胞增生。
Mossafa等报道25例,男3例,女22例,除1例不吸烟外均吸烟。1例肝、脾、淋巴结肿大,2例淋巴结和脾大,4例脾大,1例淋巴结肿大。PB淋巴细胞绝对值3例<4×109/L,22例>4× 109/L。22例有多克隆IgM增高.检测HLA-DR7者20例,19例阳性,淋巴细胞表型为CD19+、CD23-、FMC7+,均表达λ和κ轻链。作染色体分析者22例,17例有+i(3q),1例为+12,而且+i(3q)仅见于非双核的淋巴细胞。15例有多克隆IgH重排。2例于停止吸烟后,染色体异常持续存在。
1988年以来,有系统性多克隆免疫母细胞增生症(SPBP)报道,对皮质激素治疗反应好。Peterson等报道4例有发热、淋巴结、肝、脾大,黄疸、皮疹,PB、BM和淋巴结有免疫母细胞至成熟浆细胞增多,类似浆细胞白血病,2例有14q32异常,1例有单克隆IgMκ。认为SPBP可能为早期B-NHL,由多克隆B细胞增生逐渐向单克隆增生过渡。我们见到1例粒细胞缺乏感染高热患者血象和BM完全符合浆细胞白血病,经抗感染和G-CSF治疗1日后,浆细胞白血病征全消,BM代以粒系增生。
Machii等报道4例毛B淋巴细胞增生症(HBLD),临床表现与血液学特征与毛细胞白血病,日本变异性相似。患者全为女性,但不吸烟,多有脾大,亦可有淋巴结肿大,白细胞中等增高,分类淋巴细胞>0.70(70%),双核淋巴细胞极少,可有贫血或血小板减少。异常淋巴细胞比CLL细胞大,胞质丰富淡染,边缘轻度锯齿状,表面有长绒毛,核圆形、染色质密集、核仁不清,明显核皱褶。抗酒石酸活性低弱,CD5-、CD19+、CD22+、CD10+、CD24-、CD25-、CD110+。IgG明显增高,1例IgM也增高,1例IgM和IgA增高。HTLV-1、HIV抗体阴性。EBV抗体检测提示为既往感染,无急性或持久EBV感染。HLA表型3例为DR4。随访20~48个月者3例,2例无变化,1例脾逐渐增大,出现贫血和血小板减少。认为系分泌IgG的B淋巴细胞异常增生,是否转化为毛细胞白血病尚待观察。
Delage等观察6例PPBL,全有bcl-2/IgH重排使抗凋亡基因bcl-2过度表达,抑制细胞凋亡,5例为多发性重排。随访2~19年,5例稳定,1例发生NHL。有鉴于正常B淋巴细胞50%可有bcl-2/Ig重排,且随年龄增长及吸烟严重程度而增加,EBV也可使bcl-2表达。为此,PPBL为一组异质性B淋巴细胞增生,可能与EBV感染有关。有潜在恶化,对多数PPBL仍应考虑为良性,不应作为NHL的白血病期。其临床、血液学、免疫表型特征足可与B-CLL区别。Mossafa等发现46例PPBL种31例(67%)有克隆性和重现性染色体异常最常见为i(3)(q10),还可有6q-、+8、多倍体等,认为PPBL可能为恶性前期状态。
3.与小淋巴细胞淋巴瘤(SLL)的关系 诊断CLL时,PB淋巴细胞常>4×109/L,淋巴结或脾大;而SLL常有淋巴结肿大,PB淋巴细胞不高,可有孤立性BM受累或脾大,确诊时70%有全身淋巴结肿大,10%~20%有全身症状。15%SLL于病程中PB淋巴细胞增高,形态与CLL相同。BM活检CLL有不同浸润型,结节性浸润约6.5%,间质性浸润34.5%,混合型浸润24%,弥漫性浸润35%,而SLL约1/3有BM浸润,几乎均为结节型。淋巴结活检CLL和SLL相同,仅做淋巴结活检而不查血象时,CLL常诊为SLL;CLL时偶可见较大细胞有假滤泡形成,SLL有滤泡和滤泡间区,两者均可有少许浆细胞,常无肥大细胞。B-CLL与SLL细胞常表达全B标志CD19、CD20,B-CLL 90%CD5+、sIg弱阳性(常为IgM±IgD,60%~70%为κ型轻链)。75%~90%有活化抗原CD23+、25%~70%CD25+,约40%CD22+、<20%为FMC7+、5%CD79b+、38%有低亮度CD11a/CD18;而SLL,sIg亦弱(IgM±IgD,κ轻链),73%CD5+、93%强亮度CD11a/CD18。B-CLL在诊断时8%有低丙球蛋白血症,15%有高丙球蛋白血症,单克隆IgM增高多见,亦可为IgG和IgA增高,10%~20%有抗人球蛋白试验阳性溶血性贫血,2%有自身免疫性血小板减少。SLL少有低白球蛋白血症,可有单克隆IgM或IgG增高,少有自身免疫性溶血性贫血。40%B-CLL有异常核型,多为+12、13q-、11q-,85%高表达bcl-2,低表达bax、高表达周期素D2,50%高表达MDM2。SLL亦可有+12,少有13q-,11q-较为特异,可有6q-。综上所述,B-CLL与SLL无论临床、形态学、免疫学和细胞遗传学均极为相似,为同一疾病不同表现。REAL和WHO关于B细胞肿瘤分类中均作为CLL/SLL一类。如患者就诊时有淋巴结肿大或脾大,PB白细胞数增高,淋巴细胞绝对值>5× 109/L,BM象淋巴细胞>0.40(40%),则为CLL。如患者就诊时仅淋巴结肿大,活检为NHL,PB及BM淋巴细胞不增多,则为SLL。如实在不能区分可诊为SLLⅣ期或白血病期。
4.与套区细胞淋巴瘤(MCL)白血病期鉴别也很困难 但MCL细胞明显大,大小不一,核形态不规则,分叶或核裂,核染色质更疏松,常有t(11;14)和周期素D1高表达等有助于鉴别。还有CD200-以及免疫表型CD5+CD23+CD160+三联积分<3,可与CLL的CD200+及三联免疫表型积分为3区别。MCL高表达CD148有别于CLL低表达CD148。
5.与毛细胞白血病的鉴别 毛细胞白血病无论典型或变异型特征性细胞形态有毛状突起,不难与CLL区别。Rosa等报道1例HCL与CLL同存的病例,该例为68岁男性,表现为无症状性双系血细胞(白细胞和血小板)减少,亦无淋巴结、肝、脾大,BM涂片增生减少,0.53(53%)为成熟小淋巴细胞,0.045(4.5%)为毛细胞,BM活检符合毛细胞白血病(HCL),免疫表型显示有两群成熟B细胞克隆,20%为CD19+、CD20+、CD5+、κ轻链阳性(CLL),6%为CD19+、CD20+、CD25+、CD11c+、CD22+、CD23+、CD5-(HCL)。细胞遗传学正常。治以2-脱氧可福霉素而缓解,持续一年,免疫表型检查无HCL克隆,B-CLL尚有2.5%。
6.与T淋巴细胞CLL区别 借助B-CLL表达B系抗原而无T细胞标志可资区别。T-CLL极少见。
7.与t(14;19)小B细胞白血病鉴别 此易位使14q32上IGH与19q13上BCL3基因并列,但细胞形态与免疫表型和CLL不尽相同。2006年Soma等以及2007年Huh等认为此型B细胞白血病应作为新的淋巴增殖病实体,不应诊为CLL。其以下特点有别于CLL:①发病年龄中位数48岁(33~62岁),较CLL年轻(>90%年龄>50岁);②病程侵袭进展多需治疗;③淋巴结肿大,亦可脾大;④PB中白细胞增高,淋巴细胞绝对值(ALC)增高[(11.4~208)×109/L),Hb正常或轻度贫血,血小板数正常;⑤细胞形态不典型,大小不一,核凹陷,胞质可有空泡,高核质比,幼淋细胞不增多;⑥免疫表型:CD5+、CD23-、CD22+、FMC7+、sIgbright、周期素D1-;⑦遗传学有t(14;19)(q32;q13)无t(11;14)(q13;q32);⑧可进展为大B细胞淋巴瘤类似Richter综合征。
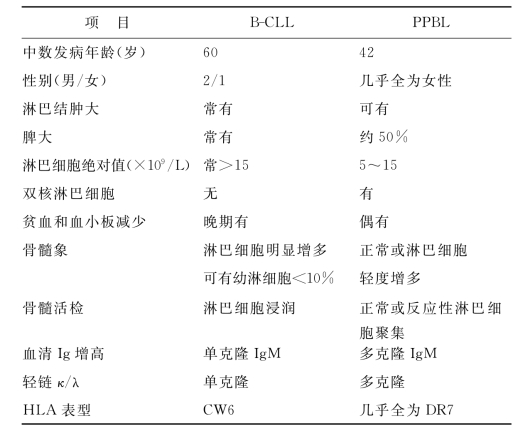
表6-2显示B-CLL与PPBL的鉴别,表6-3显示免疫表型鉴别B-CLL和其他B细胞恶性病及T细胞恶性病。
表6-2 B-CLL与PPBL临床与实验室检查的异同

(五)预后因素
下列为预后不良因素:
(1)临床上有肝、脾、淋巴结肿大,尤以纵隔淋巴结肿大明显,一般情况差,年龄较高。
(2)血液学有贫血、血小板减少,大和不典型淋巴细胞多,BM弥漫性浸润。
(3)实验室检查有低白蛋白血症,血钙增高,血清LDH高,TNFα高,脂蛋白增高。高β2-M,CD38+、ZAP-70+、IGVH无突变等。
(4)细胞遗传学有复杂多发染色体异常和17p-、11q-、+12。
(5)免疫学上显有低丙球蛋白血症,免疫表型异常和sIg强阳性,CD5-、CD23-、血清可溶性CD25受体增加,可溶性CD23受体增加。
(6)淋巴细胞倍增时间快,对治疗反应差。Benet等提出:①淋巴结肿大;②淋巴细胞数>30×109/L;③不典型淋巴细胞≥0.30(30%);④CD38+细胞>0.20(20%);⑤BM为弥漫性浸润;⑥淋巴细胞倍增时间<1年,6项中有3项提示预后不良。
(六)B-CLL的变异
B-CLL和CML一样最终有的发生变异急变,有以下几种。
1.Richter综合征和真性组织细胞淋巴瘤(THL) CLL终末期可转化为弥漫性大细胞淋巴瘤表现为Richter综合征或THL,发病率3%~15%。向Richter综合征转化过程中出现发热、消瘦、淋巴结和脾进行性肿大或其他部位肿瘤,淋巴细胞减少,异常蛋白血症。淋巴结或肿物活检为大细胞浸润。可累及PB与BM而呈白血病样,亦可局灶性分布与CLL细胞混存或取代CLL。免疫表型与CLL一样提示为同一克隆增殖转化。极少数可为2个不同克隆。Tsang发现B-CLL有散在大细胞呈Reed-Stemberg细胞样,免疫表型与CLL细胞一样为活化的肿瘤性B细胞,预后比Richter综合征好,称为霍奇金病变异型Richter综合征。我院28例CLL中1例于3年后转化为此综合征。Cohen等观察到50例中有9例于用氟达拉滨和(或)rituximab治疗数周后9例转化为Richter综合征,有的为原有克隆恶化,有的为新发生的。
Wetzler等报道1例并复习文献9例CLL转为THL。转变过程中有发热及淋巴结、脾大,并可有结外病变。CLL至THL中数间隔25.5个月,常无促发因素。该例B-CLL于2年后转为THL,颈淋巴结活检显示多形性大细胞窦性浸润,细胞胞质丰富,核仁清晰,并有中性粒、嗜酸粒和嗜碱粒细胞。溶酶体酶和NSE阳性,可被氟化钠抑制,ACP、5′-N亦阳性。免疫表型:CD22-、CD3-、CD45-、CD30-(Ki-1),但单核-巨噬细胞CD11b、CD13、CD14为阳性,S-100蛋白强阳性。该例于确诊B-CLL时有+12,发生THL后,细胞仍有+12提示为CLL克隆转化,还有t(5;14)、t(8;21)以及21号染色体畸变。有JH和JK重排,代表残留的CLL。该例CLL细胞可能来自淋巴细胞与组织细胞共同的前体细胞,有t(5;14)的细胞从淋巴细胞转变为组织细胞形态。转化后治疗反应差,中数生存仅33天(10天至5个月)。
THL与Richter综合征,淋巴结病理比较,后者细胞浸润整个淋巴结,溶酶体酶阴性,与B或T系单克隆抗体有反应,sIg阳性。在CLL早期可根据一些变数预测发生Richter综合征的可能性,Rossi等认为淋巴结≥3cm、CD38+、无del13q14及IGHV4-39利用发生Richter综合征的危险性高,应加强观察。
2.幼淋变 CLL转为PLL 3%~10%。确诊CLL时BM中幼淋细胞≤0.10(10%),经10~192个月可转化,幼淋细胞逐渐增多≥0.15(15%)可为幼淋变。转化时有进行性淋巴结、脾大,血中淋巴细胞增多,贫血加重等。CLL幼淋变有CLL病史,血中有两种表型相同的淋巴细胞和幼淋细胞,sIg弱阳性,M玫瑰花结形成,病程相对稳定,可与PLL相区别。我院28例CLL,3例(10.7%)分别于1年、3年和7年幼淋变。
3.急淋变 CLL急淋变极少见<1%。转化几乎为同一细胞系,用放疗/化疗治疗者易转化。Demirojlu等报道1例BCLL(CD19+、CD20+、HLA-DR-、CD3+、CD4+、CD5+、TCR重排)。2年后急淋变,95%原淋细胞CD19-、CD20-、HLADR-、CD3+、CD5+、CD4+、TCR重排支持原有B细胞克隆消失转化为T-ALL。
4.其他B系细胞恶性病 CLL细胞形态虽似成熟小淋巴细胞,实质为中度分化,未完全达到终末阶段,病程中可向更为成熟的浆细胞,毛细胞分化而转化为多发性骨髓瘤、浆细胞白血病或毛细胞白血病等。
5.髓系细胞变 CLL亦可向髓系细胞转变。Brocey等有1例CLL经MDS期转化为AML-M4。Teichmann等与Schaeiber等各报道1例CLL,分别于6年和8年后转化为Ph+-CML,有可能系CLL治疗引起髓系异常克隆增生的治疗相关性白血病。但Hushimi及Wallis等各报告1例CLL未经任何治疗分别于4年和5年转为CML,提示CLL可自发向髓系变异。也有转化为M6或真性红细胞增多症者。
6.成纤维细胞样转化 Isham等报道1例B-CLL转化表现奇特不符合大细胞NHL(Richter综合征)也不符合幼淋变,该例54岁,女性,1998年诊为Rai 0期CLL,无症状,未进行治疗,2002年4月,白细胞增至115×109/L,70%为淋巴前体细胞,0.20~0.30(20%~30%)淋巴样细胞核大,染色质细致,1~2个明显核仁,胞质多,不像典型幼淋细胞,BM活检为弥漫性小淋巴细胞浸润,很少大细胞,bcl-1-,CD23-,在体外培养分化成大、圆成纤维细胞样的黏附细胞,可被IFNβ及维A酸抑制。
(七)治疗
CLL进展缓慢,Binet A期患者是否需要立即治疗,Dighiero等资料作了明确的回答。他们比较了每日用瘤可宁(CLB)301例和不用CLB的308例,7年存活率分别为66%和62%,不进展至B期或C期分别为77%和65%;另一组间断用CLB和泼尼松460例和不用者466例7年存活率分别为69%和61%,无进展分别为83%和78%,均无明显差异,说明在A期治疗不能延长生存期。为此,一般的意见是:晚期及活动期者应立即治疗,而非活动期的A(0)、A(Ⅰ)、A(Ⅱ)期可暂不治疗,一旦有病情活动应治疗。治疗也应个体化。
治疗以化疗尤以烷化剂瘤可宁和环磷酰胺为单药首选。经治疗CR者仍有约50%可检出残留病变如CD5+/CD19+异常细胞>0.05(5%)或IgH基因重排,应维持治疗,真正CR应为形态学、免疫学和分子水平的缓解。
1.瘤可宁(CLB) 亦称苯丁酸氮芥,为芳香族氮芥类衍生物,治疗CLL的首选药物,常用量为0.1~0.2mg/(kg·d),淋巴细胞下降0.50(50%),改半量直至10×109/L,给维持量(2mg/d)。亦可0.4~0.6mg/kg每2~4周1次。Jaksic等用CLB 15mg/d直至CR,然后以5~15mg每周2次维持18个月,治疗116例,89.5%缓解,5年存活率61%。Catovsky等以CLB 10mg/m2,每28天用6天,至少6个月治疗208例,15例CR,113例PR,5年存活率5%。也有用小剂量0.07mg/(kg· d),每周或每2周查血象,据此调节剂量,也有用大剂量(0.7mg/kg)间歇治疗(每隔3~4周),可根据患者情况选用。
氨茶碱可抑制单磷酸环腺苷磷酸二酯酶增加细胞内cAMP浓度,增强CLB作用,促使细胞凋亡。笔者曾用CLB 4mg/d,氨茶碱0.1g/d,每月连用7~10天作维持治疗1例CLL,2年来血象正常,但分类淋巴细胞仍高0.50~0.60(50%~60%)。副作用有恶心、呕吐、黏膜炎及BM抑制。
CLB虽是治疗CLB有效药物,但CR率低,多为PR,有被疗效更好的嘌呤类药物取代之势。
2.环磷酰胺(CTX) 可口服或静脉滴注,也可小剂量维持给药(50~100mg/d)或间歇给药(1 000~1 200mg,每2~4周),疗效与CLB相似,无交叉耐药性,对CLB耐药者对CTX有反应,反之亦然,副作用中值得注意为大剂量易致出血性膀胱炎,可水化或同时给mesna。
其他烷化剂如美法仑、氮芥等虽也有效,但少用。
3.嘌呤类药物 有氟达拉滨(fludarabine,FDR)、2-氯脱氧腺苷(2-chlorodeoxyadenosine,cladri bine,2-CDA)和2-脱氧可福霉素(2-deoxycoformycin,pentostatin,DCF),疗效优于CLB。
FDR用量为25~30mg/(m2·d),静脉滴注30min,连用5天。间隔3~4周,6个疗程,疗效与分期和治疗与否相关。初治者CR+PR可达79%,复治难治者为52%。Rai 0~Ⅱ期为64%,Ⅲ期为58%,Ⅳ期为50%。Sapriano等以FDR 25mg/(m2·d),iv,30min,每4周用5天治疗60例,47%CR,23% PR。Clavio等用同法治疗16例,5例(31%)CR,11例(69%)PR,3例复发。分子水平检查6例CLL和3例NHL,7例组织学和免疫表型均CR者仍有克隆性重排。Zachee等以5FDR 12.5mg/m2,第1~5天,每28天1个疗程,6个疗程治疗2例CLL相关性肾病均CR。Rossi等以口服FDR 40mg/m2,5天,每28天1个疗程,6~8个疗程治疗81例初治CLL,37%CR,35%PR。Robak等以2-CDA 0.12mg/kg,iv,2h,5天治疗75例,总有效率62.7%,17.3%CR。又以2-CDA同样剂量3天,和环磷酰胺650mg/m2,iv,第1天治疗86例,CR27.9%,总有效86%。Elliott等以FDR 30mg/(m2·d),5天治疗1例BCLL有症状性CNS浸润而成功,副作用主要为BM抑制和感染、消化道反应、末梢神经炎等。一般在2~4疗程或停药后2周可发生抗人球蛋白试验阳性的自身免疫性溶血性贫血,可能与药物长期抑制CD4+T细胞有关,如已有免疫性溶血性贫血者更易发生。
2-CDA常用于治疗难治病例,一般用量为0.12mg/(kg· d),iv,2h,每28天用5天,3~6个疗程。综合174例,CR10%~47%,PR56%~85%。Tallman等以0.4mg/(kg· d),iv,2h,每28天用5天,3~6个疗程治疗54例,26%CR。Bosanquet等以0.12mg/(kg·d),iv,5天,间歇28天,治疗34例经CLB、FDR及蒽环类治疗无效或复发B-CLL,事先用DISC检测药物敏感性,28例药物敏感者7例(21%)CR,19例(56%)PR,6例药物不敏感者仅2例淋巴细胞稍有减少。按分期计疗效为:Binet A期8例,CR与PR各4例;B期13例,CR2例,PR 8例;C期13例,CR 1例,PR 7例。Robak等以2-CDA 0.12mg/kg,iv,2h,5天,治疗75例,17.3%CR,总有效率62.7%,又以同样剂量2-CDA和CTX 650mg/m2,iv,第1天,治疗86例,CR27.9%,总有效率86%。副作用轻,除骨髓毒性外,亦可致CD4+T细胞缺乏引起免疫调节障碍发生自身免疫现象。输血时可发生输血相关性GVHD。用药期间所有输用的血制品应照射。
DCF亦用于治疗难治者,用量为4mg/m2,iv,每1~2周1次。一组初治CLL 13例,6例(46%)PR,另一组23例难治复发者7例(30%)缓解。Handing等以DCF 4mg/m2,1周1次,3次,然后每2~4周1次,治疗15例。14例CR,1例PR,中数CR期186个月(132~210个月)。副作用轻,除BM毒外,有神经毒、皮疹、结膜炎、肝毒性、可逆性肾功能减退。亦可致CD4+T细胞缺乏,产生自身免疫现象。输血时可发生输血相关性GVHD甚至危及生命。用药期间所有输用的血制品应照射。由于药物自肾清除,治疗前肌酐清除在50~60ml/min,剂量应减半为2mg/m2。
4.肾上腺皮质激素 由于肾上腺皮质激素有明显溶解淋巴细胞作用,可单用亦可与其他药物联合,用药初期肿大的淋巴结、脾可能缩小,将其中滞留的淋巴细胞挤压入血使PB淋巴细胞进一步增高,但随治疗数日后则明显下降。尤其适用于CLL并发自身免疫性溶血性贫血和血小板减少。常用量为泼尼松40~80mg/d,每月连用5~7天,若有持续性慢性溶血可5~15mg/d或一周2次。CLL患者多为老年,应用激素易引起高血糖、骨质疏松、精神反应、感染(含原愈合的结核病变复活)等。己烯雌酚也有降淋巴细胞作用。雄激素对某些CLL的贫血有效。
5.联合化疗 多用于治疗难治及晚期病例,可延长缓解期,但不能延长中数生存期。
(1)CP方案:苯丁酸氮芥(CLB)0.08mg/(kg·d),泼尼松(P)0.8mg/(kg·d),直至缓解。有用CLB 30mg/m2,第1~15天,P 40mg/m2,第1~19天,每4周重复治疗55例,31例(56%)CR。我院以CLB 6mg/d,泼尼松40mg/d直至缓解,治疗9例,2例于治疗50天CR,7例继续治疗10天后又2例CR,全稳定。
(2)COP方案:环磷酰胺(CTX)200mg/d,7天,长春新碱(VCR)2mg,第1天,P 60mg/d,7天,每月1个疗程。药物可随白细胞和血小板减少程度而调整。
(3)CHOP方案:CTX 300mg/m2,第1~5天,多柔比星(ADR)25mg/m2,第1天,VCR 1mg/m2,第1天,P 40mg/d,7天,每月1疗程,缓解后每3个月1个疗程维持。Jaksic等治疗112例,75%有效,5年存活率36%。
(4)VCD(A)P方案:VCR 2mg第1天,CTX 200mg,第1~7天,柔红霉素(DNR)40mg,第1~3天或阿糖胞苷(Ara-C)200mg,第1~7天,P 40mg/d,第1~14天,逐渐减量,间隔14~21天为1个疗程。我院以此治疗17例,均有效,7例(41%)CR,4例(24%)PR,6例(35%)稳定。
(5)VAD方案:VCR 0.4mg,第1~4,ADR 10mg/m2,第1~4天,地塞米松(DEX)40mg,第1~4天,治疗1例CP方案无效,且有溶骨,单克隆IgA增高伴高黏综合征B-CLL而缓解。
(6)CE方案:CLB 10mg/m2,第2~7天,表柔比星(E)50mg/m2,第1天,每28天1个疗程,6个疗程。Catovsky等治疗210例,27例CR,110例PR,5年存活率49%。
(7)FDR为基础的方案:FA方案:FDR 25~30mg/m2,5天,ADR 50mg/m2,第1天,每月1个疗程,有效率55%。FM方案:FDR 30mg/m2,第1~3天,米托蒽醌(MIT)10mg,第1天,每28天1个疗程,有效率77%。FC方案:FDR 25mg/m2,5天,CTX 300mg/m2,5天,每28天1个疗程,最多6个疗程,治疗难治复发CLL 6例,CR和PR各3例;或FDR 25mg/m2,3天,CTX 250mg/m2,iv,30min,3天,每4周1疗程治疗晚期CLL 7例,有效率71%。FMCD方案:FDR 25mg/m2,第1天,CTX 600mg/m2,第1天,MIT 10mg/m2,第1天,DEX 40mg,第1~4天,每28天为1个疗程,4疗程治疗7例全部CR。近年来,多以FDR为基础作为一线治疗方案。
(8)Schutz等用抗CD20单克隆抗体rituximab 375mg/(m2·d),第57、85、113、151天,FDR 25mg/(m2·d),第1~5天,29~33天,57~61天,85~89天,治疗初治CLL 20例,5例CR,12例PR,治疗复发CLL 11例,5例CR,6例PR。
(9)FMD-R方案用于治疗难治复发性病例。FDR 25mg/m2,第2~4天,MIT 10mg/m2,第2天,DEX 20mg/d,第1~5天,R(rituximab)375mg/m2,第1天,每28天1个疗程,治疗21例,12例(57%)CR,7例(33%)PR,1例稳定。
(10)FCD-R方案治疗初发治CLL,FDR 25mg/m2,第1~3天,CTX 250mg/m2,第1~3天,DEX 20mg/m2,第1~5天,R 375mg/m2于前药用后48~72h,每3~4周1个疗程,治疗14例,10例CR,3例PR,1例无效。
6.其他治疗
(1)IFNα能调节:CLL的免疫状态并有抗增殖活性,用于治疗CLL有一定效果,用量为1.5MU/d,65%有效,用于缓解后治疗,可延长缓解期,一般不单用,最好用于早期,并于其他药物联合。
(2)白细胞单采术:适用于白细胞数特高(>500×109/L)有高黏滞综合征及白细胞淤滞者,可快速下降白细胞数,然后给联合化疗可减轻或避免发生因化疗大量杀伤白血病细胞所致的急性肿瘤溶解综合征。
(3)Russo等以GM-CSF 2.5μg/(kg·d),Epo 150U/(kg·d)连用14天对4例晚期对多种治疗无效的B-CLL作姑息治疗,以同样剂量交替隔日1次维持,PB和BM淋巴细胞下降>0.50(50%),淋巴结和脾较前缩小50%,中性粒细胞和血红蛋白均上升,达PR,维持稳定4~12个月。
(4)脾切除:适用于:①巨脾对化疗无反应;②脾亢使贫血与血小板减少加重;③自身免疫性溶血性贫血和血小板减少对皮质激素治疗反应差;④脾型CLL。Vidovic等24例(RaiⅡ期5例,Ⅲ期4例,Ⅳ期15例)行脾切除术,17例血小板减少有所改善,3年存活率84%。脾切除有效可持续数月至数年。最好于术前给肺炎球菌疫苗。
(5)单克隆抗体:B-CLL表达CD20,可用抗CD20单克隆抗体Rituximab(Rituxan,利妥昔,美罗华)375mg/m2,iv,每周1次,共4次。单用疗效短暂,多联合化疗应用。Volkova等以FCR方案治疗22例,14例(63%)CR,6例(27%)PR,疗效明显优于单用氟达拉滨(F)和CTX(CR分别为23%和29%)。方案组成为Rituxan(R)375mg/m2,iv,第1天,F 25mg/m2,iv,第1~3天,CTX 300mg/m2,iv,第1~3天,每月1个疗程,6~8个疗程。而且CD38+的CLL只有用FCR方案才取得CR。Weiss等以F(25mg/m2,5天,每28天1个疗程,6个疗程),CTX(3g/m2,每21天1个疗程,3个疗程)及R(375mg/m2,每周1次,4次)序贯治疗,治疗13例,7例CR,3例PR,1例淋巴结消失,2例无效。Mauro等以R 375mg/m2,每周1次,4次,作缓解后治疗,可使83%患者残留病变进一步减少。R的副作用有寒战、发热、恶心、荨麻疹、支气管痉挛、低血压等多短暂能耐受。Ahmed等以RCD方案治疗1例B-CLL,R 375mg/m2,第1天,CTX 750mg/m2,第2天,DEX 12mg/d,第1~7天,于输R后8h后出现肉眼血尿,消失后输CTX无发作,1个月后再用R,6h后又出现血尿,说明R可引发血尿,机制不清。B-CLL的自身免疫现象可致纯红系再生障碍、无巨核系血小板减少症,甚至再生障碍性贫血。Bharwani等病例均以R 375mg/m2,每周1次,4次而治愈。Savage等发现以R治疗后13例CD20转阴,可能用R后CD20+克隆消失而CD20-克隆生长。为此,再用R最好再检查CD20表达情况。B细胞和T细胞均表达CD52。也有用抗CD52单克隆抗体阿仑单抗(Alemtuzumab,Alem,Campath-1H),首次3mg/d,iv或sc均可,能耐受者增至10mg/d,最终增至30mg/d,每周3次,12周。Mahe等治疗12例难治B-CLL,CR和PR各6例,5例于4~14个月复发。Saba等治疗5例难治病例,1例CR,4例PR。也可用10~30mg,sc,每周3次,6~12周治疗7例FDR治疗无效复发CLL,1例CR,4例PR。Rai等以氟达拉滨25mg/m2,iv,第1~5天,每月1个疗程,4个疗程后用Alem,先3mg,iv,第1天,能耐受,第3天,10mg,第5天,30mg,以后30mg/d,1周3次,治疗36例,15例CR,18例PR。Rai等还单用Alem 3mg,iv,2h,第1天,增量至第5天30mg,第2周起30mg,每周3次,12周治疗152例难治性B-CLL,7例CR,57例PR。Flter等以FDR 30mg/(m2· d),iv,Alem 30mg,iv,第1~3天,每28天1个疗程,4个疗程,治疗14例难治复发CLL,8例CR,1例PR,1例稳定。有人以R 375mg/m2,每8周1次作维持治疗可消灭微小残留病变,减少复发,甚至减少干细胞移植后的复发。Faderl以抗CD20和抗CD52抗体合用治疗难治复发病例32例,总有效率63%,其中2例CR,1例NPR。
要注意用R后,血中CLL细胞很快减少或消失,淋巴结和脾大可缩小,但BM中CLL细胞减少慢且不明显。因为①CLL细胞有CD20分子少(1 455~28 994个/细胞)其他BLPD约为10万个/细胞;②血中有游离CD20。静脉输入R后先与血中CLL细胞上CD20结合,又与游离CD20结合,到达BM中R量很少之故。为此,R应与化疗同时或其后用。Alem高表达于恶性B/T淋巴细胞,约40万个分子/细胞。粒系、红系、血小板不表达,CD34+干祖细胞不表达,故Alem对造血祖细胞和血细胞影响不大。静脉滴注与皮下注射疗效相似,还可消灭MRD,优于R。
高表达抗凋亡bcl-2家族成员Mcl-1,尤以Mcl-1/bax比值高的CLL对化学免疫治疗效果差,可加抗Mcl-1药物flavopiridol 30~40mg/m2静脉注射30min,每周1次或silvestrol。
(6)砷剂:Akao等观察到砷剂能引起B细胞白血病系KOCL44和LyH7细胞凋亡,可能通过IL-1β转换酶家族蛋白酶caspase 1和3发挥作用。在LyH7系中还有抗凋亡bcl-2的下调。另外,有11q23累及MLL的B淋巴白血病系对砷剂抑制生长也很敏感。为此,亚砷酸(三氧化二砷,ATO)可用于难治的恶性B-LPD。我院有一例B-CLL经多种药物联合治疗,白细胞不降,一直徘徊在150×109/L左右,改用ATO 10mg/d,iv,2周后白细胞下降至60×109/L,加CLB 6mg/d,2周后白细胞降至7×109/L,停ATO,间断用CLB维持已2年,血象正常,淋巴分类仍在0.50(50%)左右。
(7)下调抗凋亡基因bcl-2,促发凋亡:B-CLL高表达bcl-2比对照高1.5~25倍,下调bcl-2,激活caspase 3,有助于提高疗效。Cabrelle等发现地塞米松和环孢素A(CsA)可激活caspase-3引起凋亡,而bcl-2无下调。但也有发现皮质激素、IL-10可下调bcl-2,上调促凋亡基因bax。抗微管药紫杉醇可磷酸化灭活bcl-2,反义寡核苷酸,ATRA等均可下调bcl-2可用于B-CLL的综合治疗。有人单用bcl-2反义寡核苷酸Genasense 3mg/(kg·d),iv,每3~4周用5~7天,治疗19例难治复发CLL,有2例PR,9例稳定。
(8)抗血管生成药物:Kini等首先发现B-CLL BM活检血管新生增强。D′Arena等检测35例B-CLL,促血管生成因子VEGF、肝细胞生长因子(HGF)、TNFα、上皮生长因子(EGF)都较对照明显增高,bFGF虽也高但与对照无差异。抗血管生长因子endostatin虽也增加,与对照亦无差异。而且VEGF与TNFα与BM浸润、PB淋巴细胞增多及淋巴结增大有关。已证实抗血管生长药物沙利度胺在多发性骨髓瘤中的治疗作用。为此,沙利度胺亦可用于B-CLL的综合治疗。一般用量50~100mg/d,用1周,无明显副作用增量至100~200mg。
(9)蛋白激酶C抑制药:有人以蛋白激酶C抑制药CGP41251 25~225mg/d,14天为1个疗程治疗9例,淋巴细胞下降>40%,以150mg/d为好,并可增强治疗CLL药物FDR、2-CDA、CLB和DNR的作用逆转多药耐药Pgp。副作用有剂量相关性胃肠道反应、头痛、嗜睡、淀粉酶和转氨酶升高,停药后可复发。可作为CLL的辅助药。
(10)拓扑酶Ⅱ抑制药:拓扑酶Ⅱ(TopoⅡ)有α和β两型。B-CLL高表达TopoⅡβ,可被MIT抑制,TopoⅡα则否。MIT可致B-CLL凋亡,并可加强嘌呤类药物FDR的作用。如能治疗前测定TopoⅡ的类型,进一步探索最佳给药方法和剂量,当可提高疗效。
(11)IL-10抑制药:B-CLL细胞可自分泌IL-10为B细胞生长分化调节因子。大豆异黄酮Genistein可使细胞阻滞在G2/M期,介导凋亡,抑制IL-10的生成与分泌。可与化疗药物合用,增加疗效。Henze等以烷化剂Bendamustine(苯达莫司丁,宾达氮芥)100mg/m2,iv,每4周用2天,6疗程治疗25例,56%有效。
(12)CLL合并PRCA常规治疗无效,每周可用利妥昔375mg/m2,4次有良效。
(八)疗效标准
1.国内疗效标准
(1)完全缓解(CR)临床症状消失,受累淋巴结和肝、脾回缩至正常,外周血白细胞≤10×109/L,淋巴细胞绝对值<4×109/L,血红蛋白和血小板正常。BM中淋巴细胞<0.40(40%)。
(2)部分缓解(PR)症状减轻,累及淋巴结、肝、脾的区域数和(或)肿大体积比治疗前减少50%以上,且无新的累及区域出现。PB白细胞、淋巴细胞绝对值和BM中淋巴细胞比例降至治疗前50%以下。血红蛋白和血小板正常或较治疗前增加50%以上。
(3)无效(NR)临床及实验室检查未达到上述PR标准或反而恶化。
2.IWCLL(慢性淋巴细胞白血病国际工作组)标准
(1)CR:没有疾病证据(临床或CLL克隆消除)。
(2)PR:由B期转为A期或由C期转为A或B期。
(3)无变化:原有分期未变。
(4)恶化:从A期转为B期或C期,从B期转为C期。
3.NCI(美国国家肿瘤研究所)标准
(1)CR:无临床症状和淋巴结、肝、脾大。血象正常,中性粒细胞≥1.5×109/L,淋巴细胞≤4×109/L,血红蛋白>110g/L,血小板>100×109/L;BM增生正常,淋巴细胞<0.30(30%)。
(2)PR:淋巴结和(或)肝、脾缩小≥50%。血象:中性粒细胞≥1.5×109/L,或较治疗前增加50%以上,淋巴细胞绝对值较治疗前减少≥50%,血红蛋白>110g/L,或较治疗前增加50%以上。血小板>100×109/L或较治疗前增加50%以上。
(3)稳定(SD):未达到治疗前PR标准。
(4)恶化:至少有以下一种:①至少2个淋巴结较治疗前增大50%以上,或有新的淋巴结肿大;②肝或脾较治疗前增大50%以上;③淋巴细胞绝对值增加50%以上;④转为幼淋白血病或非霍奇金淋巴瘤(Richter综合征)。
此外,有的国外文献CLL疗效标准除CR、PR、SD及NR外有NPR,即达CR标准,但BM活检仍有淋巴细胞聚集灶可见。
前已提及最好取得微小残留病(MRD)甚至遗传学阴性的CR。常用FCM来监测MRD,至少用常规二色(CD5+/CD19+)FCM,CD5+/CD19+B细胞<1%或CD5+/CD160+细胞<2%,κ/λ比值正常为MRD阴性。四色FCM(CD5/CD19/CD20/CD79b)敏感性较高<0.01%为MRD阴性。FCM显示MRD阴性如以PCR(特别是等位基因特异性寡核苷酸-PCR,ASO-PCR)检测22%MRD阳性,故最好取得PCR阴性(无IgH重排)。据最近资料,伦利度胺和丙戊酸钠对消灭CLL的MRD有助。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














