一、实验目的
1.了解电导率的含义。
2.掌握电导率测定水质的意义及其测定方法。
二、实验原理
电导率是以数字表示溶液传导电流的能力。纯水的电导率很小,当水中含有无机酸、碱、盐或有机带电胶体时,电导率就增加。电导率常用于间接推测水中带电荷物质的总浓度。水溶液的电导率取决于带电荷物质的性质和浓度、溶液的温度和黏度等。
电导率的标准单位是S/m(即西门子/米),一般实际使用单位为mS/m,常用单位为μS/cm(微西门子/厘米)。
单位间的互换
1 mS/m=0.01 mS/cm=10μS/cm
新蒸馏水的电导率为0.05~0.2 mS/m,存放一段时间后,由于空气中的二氧化碳或氨的溶入,电导率可上升至0.2~0.4 mS/m;饮用水的电导率为5~150 mS/m;海水的电导率大约为3 000 mS/m;清洁河水的电导率为10 mS/m。电导率随温度变化而变化,温度每升高1℃,电导率增加约2%,通常规定25℃为测定电导率的标准温度。
由于电导率是电阻率的倒数,因此,把两个电极(通常为铂电极或铂黑电极)插入溶液中,可以测出两电极间的电阻R。根据欧姆定律,温度一定时,这个电阻值与电极的间距L(cm)成正比,与电极截面积A(cm2)成反比,即
R=ρ×L/A
由于电极面积A与间距L都是固定不变的,故L/A是一个常数,称为电导池常数(以Q表示)。
比例常数ρ叫作电阻率。其倒数1/ρ称为电导率,以κ表示。
κ=1/ρ=1/R×(L/A)=Q/R
已知电导池常数,并测出电阻后,即可求出电导率。
三、仪器与试剂
1.仪器
电导率仪
温度计
恒温水浴锅
2.试剂
纯水(电导率小于0.1 mS/m)
0.001 mol/L HCl溶液
氯化钾标准溶液:0.010 0 mg/L(称取0.745 6 g于105℃干燥2 h并冷却的氯化钾,溶于纯水中,于25℃下定容至1 000 mL,此溶液在于25℃时的电导率为141.3 mS/m)
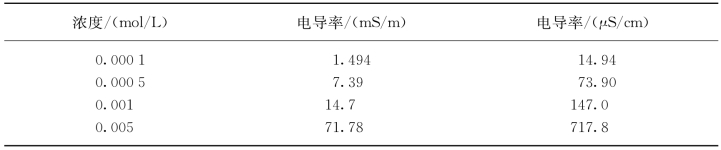
必要时可适当稀释,各种浓度氯化钾溶液的电导率(25℃)见表12-1。
表12-1 不同浓度氯化钾的电导率(25℃)
四、实验步骤
1.测定25℃纯水的电导率。
2.测定30℃、35℃、40℃、45℃、50℃、60℃水温下纯水的电导率。
3.测定25℃0.001 mol/L HCl溶液的电导率。
4.测定30℃、35℃、40℃、45℃、50℃、60℃0.001 mol/L HCl溶液的电导率。
五、数据处理
1.恒温25℃下测定水样的电导率,仪器的读数即为水样的电导率(25℃),以μS/cm单位表示。
2.在任意水温下测定,必须记录水样温度,样品测定结果按下式计算
κ25=κt/[1+a(t-25)]
式中,κ25为水样在25℃时的电导率,μS/cm;κt为水样在t℃时的电导率,μS/cm;a为各种离子电导率的平均温度系数,取值0.022;t为测定时水样品的温度,℃。
六、思考题
1.电导池常数怎样计算?
2.电导率与温度有什么关系?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















