【摘要】:在溶液中,蛋白质的氨基等基团可结合H+而带正电荷,羧基等基团可释放出H+而带负电荷。若在某一pH时蛋白质解离成正、负离子的趋势相同,所带正、负电荷数相等,成为兼性离子,净电荷为零。此时溶液的pH称为该蛋白质的等电点,用pI表示。人体血浆蛋白质的等电点大多接近5.0,血浆pH为7.4,所以血浆蛋白质处在碱性环境中以负离子形式存在。
蛋白质的两性电离_生物化学基础
一、蛋白质的两性电离
蛋白质多肽链的两端以及侧链上,有自由的氨基和羧基等基团。在溶液中,蛋白质的氨基等基团可结合H+而带正电荷,羧基等基团可释放出H+而带负电荷。因此,蛋白质是两性电解质。
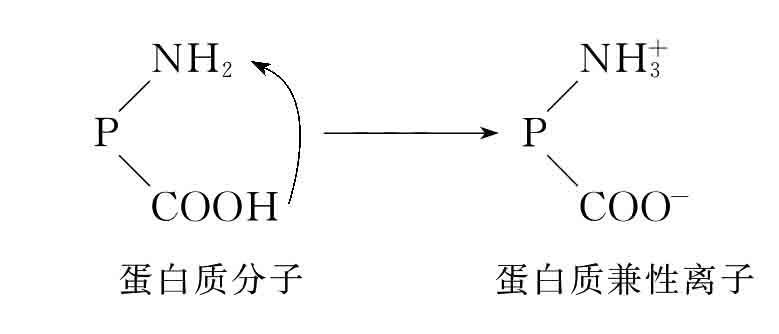
蛋白质在溶液中的电离情况,可受溶液pH的影响。在酸性溶液中,H+抑制羧基释放H+,而使氨基结合H+生成—NH+3,蛋白质为正离子。在碱性溶液中OH-与羧基释放的H+结合成水,有利于羧基电离成—COO-,蛋白质为负离子。若在某一pH时蛋白质解离成正、负离子的趋势相同,所带正、负电荷数相等,成为兼性离子,净电荷为零。此时溶液的pH称为该蛋白质的等电点,用pI表示。
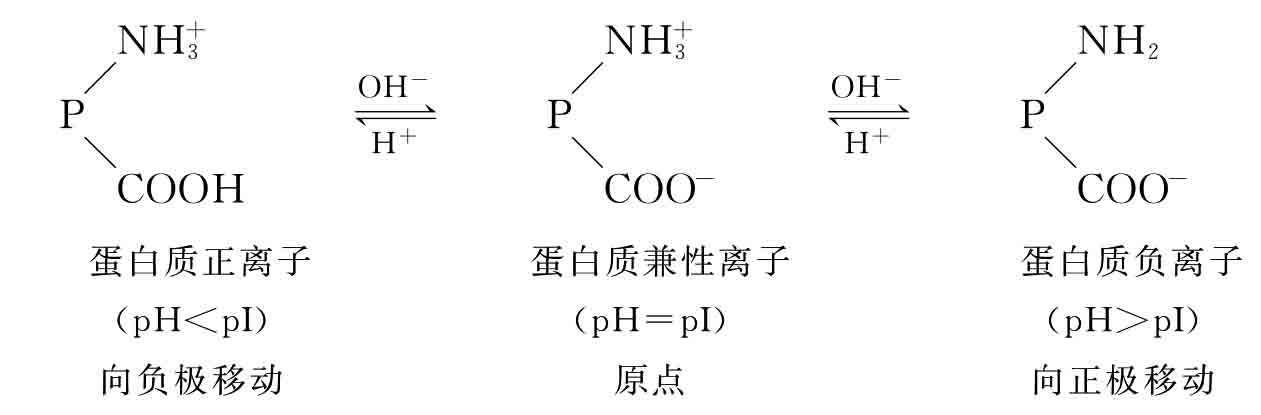
人体血浆蛋白质的等电点大多接近5.0,血浆pH为7.4,所以血浆蛋白质处在碱性环境中以负离子形式存在。
溶液中带电离子在电场中向电性相反的电极移动的现象称为电泳。在同一pH溶液中,不同的蛋白质分子因所带电荷多少、分子大小等不同,电泳的速度也不同。分子量相对较小,所带电荷较多的,电泳速度就快;反之则慢。利用蛋白质这一特性,可通过电泳法将人体血清蛋白分为五个不同的组分:清蛋白、α1-球蛋白、α2-球蛋白、β-球蛋白、γ-球蛋白等(图2-9)。

图2-9 血清蛋白电泳图谱
临床上常用血清蛋白电泳帮助诊断疾病、观察病情变化。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















