第六章 免疫应答
学 习 目 标
1.简述免疫应答的概念、分型。
2.免疫应答的基本过程是什么?
3.抗体产生的一般规律有哪些?
免疫应答是机体对抗原异物所发生的一系列排异性生理反应。
体内存在两种免疫应答类型:即固有性免疫应答和适应性免疫应答。
1.固有性免疫应答 又称非特异性免疫应答。是生物体在长期种系发育和进化过程中逐渐形成的天然防御功能。如皮肤、黏膜及附属物的机械阻挡作用和分泌杀菌、抑菌物质;吞噬细胞的吞噬作用;NK细胞对靶细胞的杀伤作用;补体的抗菌作用和干扰素的抗病毒作用等。其特点有:①与生俱来,受遗传控制;②作用广泛、迅速;③无特异性;④无记忆性。
2.适应性免疫应答 指抗原呈递细胞(APC)加工、处理和呈递抗原,T、B淋巴细胞特异性识别抗原后自身活化、增殖、分化,产生免疫效应的过程,又称特异性免疫应答。由于是在非特异性免疫应答基础上建立的,也可称为获得性免疫应答。在防止再感染中发挥关键作用。其特点有:①后天获得;②具有明显的个体差异;③具有明显的针对性;④具有记忆性。
第一节 非特异性免疫
非特异性免疫主要由三部分组成:屏障结构、参与非特异性免疫的免疫细胞、体液中的非特异免疫分子。
一、屏障结构
1.皮肤黏膜屏障 皮肤、黏膜及附属物构成了机体的外部屏障,它们通过以下三种方式抵御病原体的感染。①机械阻挡作用:皮肤表面覆盖多层鳞状上皮细胞,鼻黏膜上的鼻毛、呼吸道黏膜表面纤毛的定向运动,可将分泌物及附着于表面的微生物排出体外。②分泌杀菌和抑菌物质:皮肤及黏膜附属的腺体可分泌多种抑菌和杀菌物质,如汗腺分泌的乳酸和皮脂腺分泌的脂肪酸可抑制细菌与真菌的生长。此外,广泛存在于唾液、泪液、乳汁中的溶菌酶也能溶解革兰阳性菌。③正常菌群的拮抗作用:寄居在人体皮肤、口腔、肠道和阴道中的正常菌群能通过营养竞争及其代谢产物而拮抗病原菌的生长,如肠道中的大肠埃希菌能够分解糖类产酸而抑制志贺菌、金黄色葡萄球菌和白假丝酵母菌等病原菌的生长。
2.血-脑脊液屏障 由软脑膜、脉络丛的脑毛细血管壁和壁外的星状胶质细胞组成。它通过致密的结构阻挡血液中的病原微生物及其毒性产物进入脑组织及脑室,从而保护中枢神经系统。婴幼儿期此屏障发育不完善,较成人易发生脑膜炎、脑炎等中枢神经系统疾病。
3.胎盘屏障 由母体子宫内膜的基蜕膜和胎儿的绒毛膜滋养层细胞共同构成。正常情况下,它可以阻止母体感染的病原体及其有害产物进入胎儿体内,保护胎儿免受感染。妊娠早期(3个月内)此屏障发育尚未完善,若孕妇在此期间发生弓形虫、风疹病毒、巨细胞病毒、单纯疱疹病毒等感染,可引起胎儿畸形、流产或死胎。药物影响亦然。
二、参与非特异性免疫的免疫细胞
1.吞噬细胞 病原体穿过机体的屏障结构后,向机体内部入侵、扩散、蔓延。此时吞噬细胞即可发挥强大的吞噬杀伤作用。
(1)吞噬细胞的种类 吞噬细胞包括大吞噬细胞和小吞噬细胞两种。小吞噬细胞是指血液中的中性粒细胞,大吞噬细胞是指单核巨噬细胞系统,包括血液中的单核细胞和分布在多种组织器官中的巨噬细胞。
(2)吞噬细胞杀菌过程 ①趋化和接触:吞噬细胞在趋化因子的作用下定向运动并聚集到病原体周围并与之接触。②调理与吞入:吞噬细胞接触病原体后,细胞膜内陷或伸出伪足包裹病原体,形成吞噬体,即吞噬。对于病毒等较小的物质,则其附着处的吞噬细胞膜内陷形成吞饮小泡,即胞饮。体液中的抗体或补体可起调理作用。③杀菌和消化:吞噬体与溶酶体融合形成吞噬溶酶体,在溶酶体内的各种水解酶及髓过氧化物酶等参与下对病原体消化降解,未被消化的残渣排出体外(图6-2)。
(3)吞噬结果 病原体被吞噬后彻底消化即为完全吞噬,多见于化脓性细菌感染。一些胞内寄生菌(如结核分枝杆菌、麻风分枝杆菌、伤寒沙门菌等)和病毒被吞噬后却不能被有效杀死,即为不完全吞噬。不完全吞噬可保护病原体免受抗菌物质或药物的杀灭,甚至在胞内增殖,或随游走的吞噬细胞扩散全身。
2.NK细胞 NK细胞的杀伤作用不需要抗原诱导,也无须特异性抗体或补体的参与,没有MHC限制性。它在特异性免疫应答产生以前即已发挥防御作用,可通过不同途径杀死病原体感染的靶细胞,如病毒感染的细胞和肿瘤细胞等。
除NK细胞外,嗜酸性粒细胞和血小板对寄生虫感染也具有杀伤作用。
三、体液中的非特异性免疫分子
1.补体系统 补体系统是机体非特异性免疫的一个重要组成部分,在机体早期抗感染免疫过程中具有十分重要的意义(详见第四章)。
2.干扰素 干扰素是由干扰素诱生剂刺激机体多种细胞产生的一组特殊蛋白,具有抗病毒、抗肿瘤和免疫调节作用。
3.溶菌酶 溶菌酶是一种不耐热碱性蛋白质,主要来源于巨噬细胞,广泛存在于泪液、唾液、乳汁、肠液、尿液、血清以及吞噬细胞的溶酶体颗粒中。溶菌酶对革兰阳性细菌具有溶解作用。
4.乙型溶素 乙型溶素是血清中一种对热较稳定的碱性多肽。血小板中含量丰富,可破坏革兰阳性细菌细胞膜,而对革兰阴性细菌无效。
5.C反应蛋白 C反应蛋白是一种具有代表性的急性期蛋白。在感染早期,多种细胞因子刺激肝细胞大量合成,血清中含量急剧升高,感染控制时迅速降至正常水平。C反应蛋白能与多种细菌结合,通过激活补体系统而杀伤病原体。
第二节 特异性免疫
一、概 述
(一)特异性免疫应答的类型
特异性免疫应答是T、B细胞在抗原刺激后,活化、增殖、分化,形成效应细胞和产生效应分子,产生生物学效应的全过程。根据其免疫结果,可分为正应答(免疫应答)和负应答(免疫耐受);根据其免疫机制可分为T细胞介导的细胞免疫应答和B细胞介导的体液免疫应答。
在正常情况下,机体通过免疫应答清除抗原并对自身物质耐受,以维持自身生理功能稳定。在异常情况下,则导致机体病理损伤,引起超敏反应或其他免疫性疾病。
(二)特异性免疫应答的场所
淋巴结、脾脏及黏膜相关淋巴组织等外周免疫器官是特异性免疫应答的场所。免疫应答发生时,常伴有局部淋巴结肿大,这是由于在抗原刺激下,淋巴细胞增殖、细胞因子产生、炎细胞浸润等多因素作用所致。随着免疫应答的逐渐减弱,肿大的淋巴结将恢复正常。
(三)特异性免疫应答的基本过程
免疫应答过程可分为三个阶段(图6-1):
1.抗原呈递和识别阶段 是APC对抗原的摄取、处理、呈递和T、B细胞通过受体TcR和BCR识别特异性抗原的过程。
(1)对外源性抗原的加工处理和呈递 外源性抗原指细胞外感染的微生物或其他蛋白质抗原。当外源性抗原进入机体,被APC通过吞噬、胞饮等方式摄入细胞内形成吞噬小体,与溶酶体融合形成吞噬溶酶体,在酸性环境中,被蛋白酶等水解为抗原多肽片段。在吞噬溶酶体中,抗原肽与新合成的MHC-Ⅱ类分子结合,形成抗原肽-MHC-Ⅱ类分子复合物,转运至APC表面,供CD4+ T细胞识别(图6-2)。

图6-1 免疫应答的基本过程

图6-2 APC对外源性抗原的加工和处理
(2)对内源性抗原的加工处理和呈递 内源性抗原指机体细胞内合成的抗原,如病毒感染的细胞合成的病毒蛋白,肿瘤细胞合成的蛋白抗原等。内源性抗原在细胞内受聚合蛋白酶体(LMP)的作用而被降解成具有8~10个氨基酸残基的抗原肽,再由转运体(TAP)转运到内质网中,与新合成的MHC-Ⅰ类分子结合成抗原肽-MHC-Ⅰ类分子复合物,转运至细胞表面,供CD8+ T细胞识别。体内所有能表达MHC-Ⅰ类分子的细胞都具有将抗原肽结合到MHC-Ⅰ类分子上,并表达于细胞表面。
两类MHC分子可被看作是抗原多肽的载体,外源性抗原主要通过MHC-Ⅱ分子呈递,内源性抗原主要通过MHC-Ⅰ分子呈递。但现已证实,二者间存在交叉呈递现象,但这种交叉呈递并非抗原呈递的主要方式。
2.活化、增殖和分化阶段 T细胞和B细胞识别抗原后,在细胞间多种协同刺激分子和细胞因子作用下,发生活化和增殖,并分化为效应细胞(效应性T细胞和浆细胞),产生效应分子(细胞因子和抗体)。有部分细胞中途停止分化形成记忆性细胞(Tm和Bm),记忆性细胞再次接触相同抗原后,可迅速增殖分化为效应细胞,发挥效应作用。若T细胞和B细胞识别抗原后不能有效活化,则诱导抗原特异性细胞的凋亡或克隆无能,形成耐受。
3.效应阶段 效应细胞和效应分子共同发挥作用,产生细胞免疫效应和体液免疫效应。清除抗原性异物,从而维持机体正常生理状态。病理情况下也可引发免疫相关性疾病。
二、体液免疫应答
体液免疫应答又称B细胞介导的免疫应答,是指B细胞接受特异性抗原刺激后,活化、增殖、分化为浆细胞,浆细胞分泌抗体,发挥特异性免疫效应的过程。B细胞表面的抗原受体(BCR)可识别游离抗原或被APC捕获的抗原。抗体是存在于体液中的主要的效应分子,故将抗体参与的免疫应答称为体液免疫应答。
诱导B细胞应答的抗原是TD抗原和TI抗原。TD抗原引起的体液免疫应答必须有抗原呈递细胞和CD4+ Th细胞的参与;TI抗原引起的体液免疫应答无需抗原呈递细胞和CD4+ Th细胞参与。
(一)B细胞对TD抗原的免疫应答
1.Th细胞的活化、增殖和分化 初次进入机体的TD抗原,APC多为巨噬细胞,再次应答发生时,APC则主要是已扩增的B细胞克隆,B细胞的BCR可直接识别游离抗原,B细胞通过胞饮或BCR介导的内化作用摄入抗原。经APC加工处理成抗原肽-MHC-Ⅱ类复合物表达于APC表面,供CD4+ Th细胞识别。Th识别抗原后由静止状态转变为活化的Th才能辅助B细胞产生抗体。Th细胞识别抗原肽-MHC-Ⅱ类复合物而活化需要双信号(图6-3)。
第一信号为双识别:由静止的CD4+ Th细胞表面的TcR-CD3复合物与APC表面的抗原肽-MHC-Ⅱ类分子复合物的抗原肽部分特异性结合,CD4分子与MHC-Ⅱ类分子Ig样区结合,相互作用,诱导产生CD4+ Th细胞活化的第一信号。
第二信号为协同刺激信号:APC上表达的多个协同刺激分子与Th细胞表面表达的相应受体配对结合,相互作用。在各种协同刺激分子中,最重要的是CD28与B7-1(CD80)和B7-2 (CD86)的结合,其他还有VCAM-1与VLA-4、ICAM-1与LFA-1、LFA-3(CD58)LFA-2 (CD2)等均为第二信号。

图6-3 CD4+ Th细胞活化双信号
在双信号刺激下,Th细胞被活化,表达多种细胞因子受体及分泌多种细胞因子,并与受体结合。活化的Th细胞在与以IL-4为主的细胞因子作用下可增殖分化为CD4+ Th2细胞,形成细胞克隆,分泌更多的细胞因子,如IL-2、4、5、6,TNF、IFN等,促进B细胞的增殖分化。在此过程中部分Th细胞停止分化,保留对特异性抗原的长期记忆,成为Tm细胞。当再次接受相同抗原刺激时,不经上述诱导过程可直接活化,产生效应。如果只有第一活化信号,则Th细胞被诱导进入特异性免疫无应答状态,即免疫耐受状态。
2.B细胞的活化、增殖和分化 B细胞的活化、增殖和分化也需要双信号刺激和细胞因子的参与(图6-4)。
B细胞活化的第一信号:B细胞的BCR识别抗原是B细胞活化的第一信号,并由Igα/Igβ将信号传入B细胞内。同时,B细胞作为APC加工处理TD抗原以抗原肽-MHC-Ⅱ类分子复合物形式呈递给Th,称为Th细胞活化的第一信号。
B细胞活化的第二信号:由Th细胞与B细胞间相互作用的多对分子结合构成的协同刺激信号,其中最重要的是T细胞表面的CD40L与B细胞表面的CD40结合。
在双信号刺激下,B细胞活化,活化的B细胞可表达多种细胞因子受体,在不同细胞因子作用下发生类别转换,增殖分化为分泌不同类别Ig的浆细胞。在此过程中部分B细胞分化成保留对特异性抗原的长期记忆的Bm细胞。当再次接受相同抗原刺激时,不经上述诱导过程可迅速增殖分化为浆细胞,合成分泌更多抗体,扩大免疫效应。
3.浆细胞分泌抗体发挥免疫效应 抗体的生物学作用有:①中和作用;②激活补体;③免疫调理作用;④介导ADCC作用;⑤参与超敏反应和某些自身免疫病。
图6-4 B细胞与Th细胞间的相互作用
(二)B细胞对TI抗原的免疫应答
细菌多糖、多聚鞭毛蛋白、脂多糖等属TI抗原,能直接激活初始CD5+ B1细胞而无需APC和Th细胞辅助,不受MHC限制。TI抗原诱导所产生的抗体均为IgM类,不能诱导记忆性B细胞的形成,无再次应答反应。TI抗原分为TI-1和TI-2。
1.TI-1抗原 高剂量TI-1抗原(如LPS)可非特异激活多克隆B细胞,故称其为B细胞丝裂原。低剂量TI-1抗原只能激活其BCR能结合TI-1抗原的特异性B细胞,B细胞针对低剂量TI-1抗原产生的免疫应答在细菌感染的早期发挥抗感染作用。
2.TI-2抗原 此类抗原(如细菌的荚膜多糖)具有高度重复的抗原表位,能与成熟的特异性B细胞BCR广泛交联而激活B细胞,但高剂量TI-2抗原过度交联可使成熟B细胞产生耐受性。B细胞针对TI-2抗原所产生的抗体,可发挥调理作用,促进吞噬细胞对病原体的吞噬。
(三)抗体产生的一般规律
1.初次应答 初次应答是机体初次接触抗原发生的免疫应答。抗体产生的特点为:①潜伏期较长,经1~2周血清中才出现抗体;②抗体效价低;③在体内维持时间短;④以IgM抗体为主;⑤低亲和力抗体。
2.再次应答 再次应答是指机体再次接触相同抗原所发生的免疫应答。抗体产生的特点为:①潜伏期明显缩短,一般经1~2 d;②抗体效价高;③在体内维持时间长;④以IgG抗体为主;⑤高亲和力抗体(图6-5)。
抗体产生的规律在医学实践上有重要意义:①用于加强免疫,提高免疫效果;②检测IgM作为病原体感染的早期诊断和子宫内感染的诊断;③根据抗体水平的动态变化了解患者病程及评估疾病转归。

图6-5 初次和再次免疫应答抗体产生的一般规律
三、细胞免疫应答
细胞免疫应答又称T细胞介导的免疫应答,是指T细胞接受特异性抗原刺激后,转化为效应T细胞(致敏Th1细胞和致敏Tc细胞),发挥特异性免疫效应的过程。通常由TD抗原诱发,与B细胞介导的体液免疫应答相似。参与细胞免疫应答的细胞主要包括APC、CD4+ Th细胞和CD8+ Tc细胞。此外,巨噬细胞、NK细胞等也参与细胞免疫的效应过程。
1.CD4+ T(Th1)细胞的激活与作用 初始的CD4+ T细胞的TcR与APC表面的抗原肽-MHC-Ⅱ类分子复合物结合产生特异信号,即第一信号,经CD3转导至细胞内(图6 -3);APC与CD4+ T细胞表面有多对分子结合产生协同刺激信号,即第二信号,如B7与CD28、LFA-3与CD2、ICAM-1与LFA-1等,其中B7与CD28最重要。在双信号刺激下CD4+ T细胞活化并产生细胞因子;活化的T细胞分泌IL-1、IL-12、IL-2、IL-6等细胞因子,在细胞因子的作用下初始的CD4+ T细胞进一步活化,并迅速的分裂而大量增殖,分化为效应性T细胞,即Th1细胞和Th2细胞。
效应Th1细胞当再次和相同抗原相遇后,释放IL-2、INF-γ、TNF-β细胞因子等多种细胞因子,作用于单核巨噬细胞、淋巴细胞、粒细胞和血管内皮细胞,使局部产生以淋巴细胞和单核巨噬细胞浸润为主的慢性炎症反应和迟发型超敏反应。
Th1细胞以分泌为主介导细胞免疫效应,Th2细胞以分泌IL-4、IL-5、IL-6、IL-10细胞因子为主增强体液免疫应答。
2.CD8+ Tc细胞的激活与作用 CD8+ Tc细胞的活化要在Th细胞协同作用下才能分化发育成效应Tc细胞,也需要双信号刺激(图6-6)和细胞因子的作用。
第一信号来自于TcR与靶细胞上的抗原肽-MHC-Ⅰ类分子复合物特异性地结合产生的特异信号;第二信号来自于CD8+ Tc细胞和靶细胞表面的CD28与B7等分子结合而产生的协同刺激信号;同时CD8+ Tc细胞需要在活化的CD4+ Th1细胞产生的IL-2、IFN-γ等细胞因子的作用下活化、分化为效应Tc细胞。
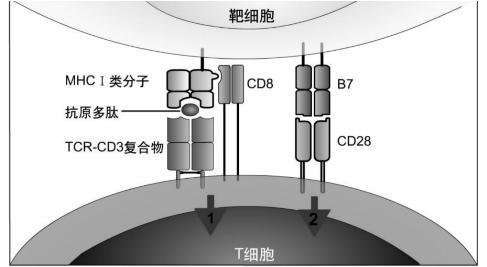
图6-6 CD8+ Th细胞活化双信号
效应Tc细胞的TcR特异性结合靶细胞表面的抗原肽-MHC-Ⅰ类分子复合物,以及两细胞间CD28与B7等辅助分子结合,触发Tc细胞释放穿孔素和颗粒酶(丝氨酸蛋白酶),穿孔素单体可迅速嵌入靶细胞膜,在Ca2+存在下,聚合形成孔道,导致靶细胞溶解;颗粒酶经穿孔素在靶细胞膜形成的孔道进入,激活细胞凋亡相关的酶系统而导致靶细胞凋亡,并可分泌肿瘤坏死因子(TNF)和表达受体Fas的配体(FasL),这些效应分子与靶细胞上TNF受体和Fas结合介导靶细胞凋亡,从而选择性杀伤所接触的靶细胞,而不影响邻近正常的细胞(图6-7)。
效应Tc细胞对靶细胞的杀伤作用特点是:①特异性杀伤作用;②杀伤作用受MHC-Ⅰ类分子的限制;③可连续杀伤靶细胞。
3.细胞免疫的生物学效应 ①抗细胞内寄生病原体(病毒、某些细胞内寄生菌)的感染。②抗肿瘤。③介导迟发型超敏反应、移植排斥反应和参与某些自身免疫病的发生。
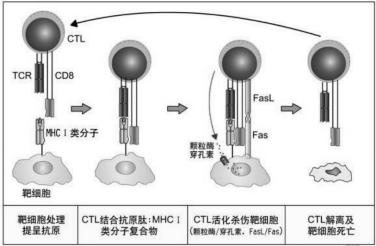
图6-7 Tc杀伤靶细胞的过程
第三节 免疫耐受
免疫耐受是指T细胞和B细胞识别抗原后,不能被激活,发生抗原特异性细胞的凋亡或克隆无能,表现出特异性无应答状态,又称负免疫应答。免疫耐受的作用与正免疫应答相反,但两者均是免疫系统的重要功能组成。诱导耐受形成的抗原称为耐受原。
免疫耐受与免疫缺陷或药物引起的免疫抑制不同,前者具有免疫特异性,只对特定的抗原不应答,对其他抗原仍能进行正常的应答;而后者则无免疫特异性,对各种抗原均不应答及对免疫系统有普遍的抑制作用。
1.胚胎期及新生期接触抗原所致的免疫耐受 在胚胎发育期及新生期,不成熟的T细胞和B细胞接触抗原,不论是自身抗原或是外来抗原,都会形成对所接触抗原的免疫耐受,以后再遭遇相同抗原,不予应答。这种免疫耐受长期持续,不会轻易被打破。
(1)天然免疫耐受现象 Owen(1945)观察到异卵双生小牛由于胚胎期胎盘血管融合而导致血液交流,出生后双方成为含有两种不同血型红细胞的嵌合体,相互间进行皮肤移植而不发生移植排斥反应。
(2)人工诱导的免疫耐受 Medawar等(1953)将CBA黑鼠的脾细胞注入A系白鼠的胚胎或新生鼠体内,A系鼠成长后可接受CBA系的皮肤移植,不被排斥。此实验不仅证实了Owen的观察,且揭示了当机体内免疫细胞处于早期发育阶段时,可人工诱导其对“非己”抗原产生耐受。
2.后天接触抗原导致的免疫耐受 在后天过程中,原本对抗原应答的T细胞和B细胞克隆,受多种因素影响,发生耐受,这类耐受能持续一段时间,部分耐受可随诱导因素的消失,耐受随之解除,重新恢复对相应抗原的免疫应答能力。抗原因素与免疫耐受的关系主要有以下几种。
(1)抗原类型 可溶性的、分子结构小而简单的抗原,蛋白质单体分子抗原,易诱导免疫耐受;颗粒性抗原、蛋白质聚体分子抗原为良好的免疫原。
(2)抗原剂量 适当的抗原剂量免疫机体易诱导免疫应答,而过低或过高剂量抗原刺激均可能诱导免疫耐受。低剂量可诱导T细胞低带耐受;高剂量可诱导T及B细胞高带耐受;TI抗原可诱导B细胞高带耐受;低、高剂量TD抗原均易诱导耐受。
(3)抗原免疫途径 经口服和静脉注射抗原易诱导免疫耐受;皮下及肌内注射易诱导免疫应答。口服抗原诱导耐受的机制是:①胃肠道消化作用使抗原大分子降解而降低其免疫原性;②口服抗原,经胃肠道诱导派氏集合淋巴结及小肠固有层B细胞,产生分泌型IgA(SIgA),形成局部黏膜免疫,但却致全身的免疫耐受。
(4)抗原变异 易突变病毒,如人类免疫缺陷病毒(HIV)、丙型肝类病毒(HCV),在感染过程中,会因基因突变产生模拟抗原,它们能与MHC结合,虽可被TCR识别结合,却产生不完全活化信号,使细胞处于免疫耐受状态,失去免疫防御作用。
小 结
B细胞对TD抗原的应答需BCR结合抗原的第一信号、T细胞及其分泌细胞因子所提供的第二信号(辅助刺激信号)。B细胞对TD抗原的再次应答具所需抗原量少、抗体生成潜伏期短、抗体产量高、在体内维持时间长、抗体亲和力高等特点。B细胞对TI抗原应答的特点是:不需T细胞辅助,无类别转换,无亲和成熟,不产生记忆细胞。其意义在于可在感染早期发挥作用。黏膜免疫应答是一类特殊的免疫应答,起主要作用的是分泌型IgA。B细胞介导的体液免疫表现在:参与抗感染、抗肿瘤,介导超敏反应和某些自身免疫病。
T细胞识别双信号包括TCR识别APC上的抗原肽和MHC分子的复合物为第一信号;辅助刺激分子与其配基结合提供的第二信号。特异性细胞免疫的效应细胞主要是Th1型CD4+ T细胞和CD8+ CTL细胞,前者经活化Mφ而诱生炎症性迟发型超敏反应;后者藉分泌细胞毒素及诱导细胞凋亡以及杀死带抗原的靶细胞。特异的细胞免疫应答的表现为:在清除胞内病原感染、清除病毒感染细胞、抗肿瘤免疫反应、排斥异体移植物中起重要作用和介导迟发型超敏反应。
(丁 丽)
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















