第二章 白细胞疾病
一、白细胞减少症
【诊断标准】
根据国内有关文献拟定如下白细胞减少症(leukopenia)的诊断标准。有各种病因导致成人外周血白细胞数低于4.0×109 /L时,称为白细胞减少症。儿童参考不同年龄正常值的低线。10~12岁低于4.5×109 /L;<10岁低于5.0×109 /L时,考虑为白细胞减少症。
二、中性粒细胞减少和粒细胞缺乏症
【诊断标准】
参考以上“白细胞减少症”的国内外文献拟定诊断标准如下:
当外周血中性粒细胞绝对值,成人低于2.0×109 /L时为中性粒细胞减少症。当粒细胞严重减少,低于0.5×109 /L,为粒细胞缺乏症。儿童10-12岁低于1.8×109 /L〈10岁低于1.5×109 /L,为中性粒细胞减少症。粒细胞缺乏症的诊断标准同成人标准。
三、急性白血病
白血病是因造血干细胞于分化过程的不同阶段发生分化阻滞,凋亡障碍和恶性增殖而引起的一组异质性的造血系统恶性肿瘤。急性白血病阻滞发生在较早阶段。按照白血病细胞的系列又分为急性髓系白血病和急性淋巴细胞白血病两大类。
【诊断标准】
(WHO标准)
(1)血或骨髓原始粒(或单核)细胞≥20%,可诊断为AML。
(2)当患者被证实有克隆性重现性细胞遗传异常t(8;21)(q22;q22)、inv(16)(p13;q 22)或t(16;16) p13;q 22)以及t(15;17)(q22;q12)时,即使是原始细胞<20%,也可诊断为AML.
(3)伴有多细胞系病态造血的AML以及治疗相关性AML和MDS,分别单独划分为独立亚型。
(4)骨髓中幼稚淋巴细胞>25%时诊断急性淋巴细胞白血病。
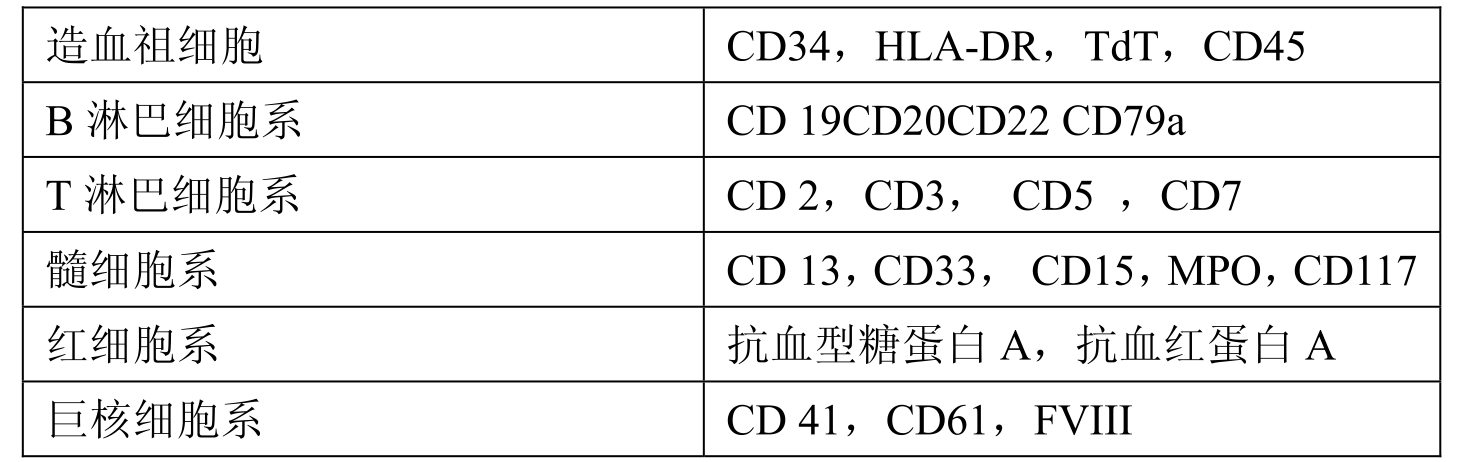
急性白血病分类常用的单克隆抗体
四、急性髓系白血病
【分型诊断标准】
1980年9月和1986年9月,分别在我国苏州市和天津市召开了全国白血病分类分型讨论会。两次会议在讨论FAB分类的基础上,提出国内AML的形态学分型诊断标准如下。
1.原粒细胞按形态分为两型
Ⅰ型:典型原粒细胞,胞浆中无颗粒。
Ⅱ型:有原粒细胞特征,胞浆量较少,有少量细小颗粒。
原单核细胞和原淋巴细胞也分为Ⅰ和Ⅱ型,分型标准与原粒细胞相似。
2.AML分类
(1)急性粒细胞白血病未分化型(M1)骨髓中原粒细胞大于等于90%(NEC),早幼粒细胞很少,中幼粒细胞以下阶段不见或罕见。
(2)急性粒细胞白血病部分分化型(M2):分为以下两种亚型。
M2a:骨髓中原粒细胞为30%-<90%(NEC),单核细胞小于20%,早幼粒细胞以下阶段>10%
M2b:骨髓中原粒细胞及早幼粒细胞明显增多,以异常的中性中幼粒细胞为主,其胞核常有核仁,有明显的盒浆发育不平衡,此类细胞>30%。
(3)急性早幼粒细胞白血病(M3):骨髓中以颗粒增多的异常早幼粒细胞增生为主,>30%(NEC),其胞核大小不一,胞浆中有大小不等的颗粒。
分为两种亚型。
1)M3a(粗颗粒型):是苯胺蓝颗粒粗大,密集甚或融合。
2)M3b:(细颗粒型):是苯胺蓝颗粒密集而细小。
(4)急性粒单核细胞白血病(M4):按粒细胞和单核细胞形态不同,分为下列四种亚型。
1)M4a:原粒和早幼粒细胞增生为主,原幼单核和单核细胞≥20%(NEC)。
2)M4b:原幼单核细胞增生为主,原粒细胞和早幼粒细胞>20%(NEC)。
3)M4c:原始细胞既具粒细胞系,又具单核细胞系形态特征者>30%(NEC)
4)M4E0:除上述特点外,还有粗大而圆的嗜酸颗粒及着色较深的嗜酸颗粒,占5%-30%(NEC)。
(5)急性单核细胞白血病(M5):分为以下两种亚型。
1)M5a(未分化型):骨髓中原单核细胞I+II型(NEC)≥80%。
2)M5b(部分未分化型):骨髓中原始+幼稚单核细胞(NEC)>30%,原单核细胞I+II型<80%。
(6)红白血病(M6):骨髓中红细胞系>50%,且有形态学异常,骨髓原粒细胞(NEC)或原始+幼稚单核性细胞(NEC)I+II型;若血片中原粒细胞或单核细胞>5%,骨髓原粒细胞或原始+幼稚单核细胞>20%(NEC)。
(7)急性巨核细胞白血病(M7):外周血中有巨核细胞;骨髓中原巨核细胞≥30%,该原巨核细胞应有电镜或单克隆抗体证实;骨髓细胞少,往往干抽,活检有原始或巨核细胞增多,网状纤维增加。
五、急性淋巴细胞白血病
【分型诊断标准】
1980年9月,在江苏省苏州市召开了全国白血病分类分型的讨论会,对急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)的分型标准提出建议如下。
1.第一型(L1)原始和幼稚淋巴细胞以小细胞(直径<12μm)为主;核圆形,偶有凹陷和折叠,染色质较粗,结构较一致,核仁少而小,不清楚;胞浆量少,轻中度嗜碱。过氧化物酶或苏丹黑色阳性的原始细胞一般不超过3%。
2.第二型(L2)原始和幼稚淋巴细胞以大细胞(直径可大于正常小淋巴细胞2倍以上,>12μm为主;核型不规则,核型和折叠可见。染色质较疏松,结构较一致,核仁较清楚,一个或多个;胞浆量常较多,轻中度嗜碱,有些细胞较深染。
3.第三型(L3)似Burkitt型,原始和幼稚淋巴细胞大小较一致,一大细胞为主;核型较规则,染色质呈均匀细点状,核仁明显,一个或多个,呈小泡状;胞浆量较多,深蓝色,空泡较为明显,呈蜂窝状。
六、低增生性急性白血病
【诊断标准】
综合国内文献,将低增生性急性白血病(hypocellular leukemia,HL)的诊断条件归纳如下。
1.临床表现 肝、脾、淋巴结一般不肿大。
2.实验室检查
(1)外周血常呈全血细胞减少,偶见原始细胞或幼稚细胞。
(2)两次以上不同部位骨髓检查呈增生减低,有核细胞少,但原始细胞在30%以上。
(3)骨髓活体组织检查为本病。
七、成人T淋巴细胞白血病
【诊断标准】
1984年9月,在天津召开了全国部分省市成人T淋巴细胞白血病(adult T-cell leukemia,ATL)协作会议制定了国内的诊断标准。
1.白血病的临床表现
(1)发病于成年人。
(2)有浅表淋巴结肿大,无纵膈或胸腺肿瘤。
2.实验室检查 外周血白细胞数常增高,多形和淋巴细胞(花细胞)占10%以上,属T细胞,有成熟T细胞表面标志;血清抗HTLV-I抗体阳性。
八、浆细胞白血病
【诊断标准】
1.临床上呈现白血病的临床表现或多发性骨髓瘤的表现。
2.外周血白细胞分类中浆细胞>20%或绝对值≥2.0×109/L。
3.骨髓中浆细胞明显增生,原始及幼稚浆细胞明显增多,伴形态异常。
九、肥大细胞白血病
【诊断标准】
综合国内外资料,提出肥大细胞白血病(mast cell leukemia,MCL)的诊断条件。
1.临床上除有白血病的临床表现外,还有肥大细胞增多症的表现。
(1)淋巴结 肝 脾肿大。
(2)肥大细胞释放组胺和其他物质引起的局部和全身变化。
1)皮肤潮红 色素性荨麻疹、皮肤瘙痒等。
2)发作性支气管痉挛、呼吸困难、心悸、低血压、晕厥、休克等症状。
3)肝素释放过多引起出血倾向。
2.外周血中有肥大细胞(组织嗜碱细胞)。
3.骨髓中肥大细胞明显增多,占有核细胞的50%以上。
4尿内组胺增高。
5.骨髓干抽或有皮肤浸润时需做活体组织检查确诊。
十、嗜酸性粒细胞白血病
【诊断标准】
1患者有白血病的临床表现。
2.外周血嗜酸粒细胞明显持续增多,并常有幼稚嗜酸粒细胞。
3.骨髓嗜酸粒细胞增多,有形态异常、核左移,可见各阶段幼稚石酸粒细胞,甚至早幼粒细胞可有粗大的嗜酸颗粒,原粒细胞>5%。
4.脏器又是酸粒细胞浸润。
5.能除外其他原因所致的嗜酸粒细胞增多。
十一、中枢神经系统白血病
【诊断标准】
1978年10月,在广西南宁召开的全国白血病防治研究协作会议制定的中枢神经系统白血病(CNSL)的诊断标准如下。
1.有中枢神经系统症状和体征(尤其是颅内压增高的症状和体征)。
2.有脑脊液的改变
(1)压力增高(>0.02kpa或200mmH2O),或滴速大于60滴/分。
(2)白细胞数>0.01×109/L。
(3)涂片见到白血病细胞。
(4)蛋白>450mg/L,或潘氏试验阳性。
3.排除其他原因造成的中枢神经系统或脑脊液的相似改变。
十二、急性白血病
【疗效标准】
1987年11月,在江苏省苏州市召开了全国白血病化学治疗讨论会,提出了如下急性白血病疗效标准。
1.缓解标准
(1)完全缓解(CR)
1)临床无白血病细胞浸润所指的症状和体征,生活正常或接近正常。
2)血象:Hb≥100g/L(男),或≥90g/L(女及儿童),中性粒细胞绝对值≥1.5×109/L,血小板≥100×109/L。外周血白细胞分类中无白血病细胞。
3)骨髓象:原粒细胞I型+II型(原始单核+幼稚单核细胞或原始淋巴+幼稚淋巴细胞)≤5%,红细胞及巨核细胞系正常。
M2b型:原粒细胞I型+II型≤5%,中性中幼粒细胞比例在正常范围。
M3型:原粒细胞+早幼粒细胞≤5%。
M4型:原粒细胞I、II型+原始单核及幼稚单核细胞≤5%。
M5型:原始单核细胞I型+II型及幼稚单核细胞≤5%。
M6型:原粒细胞I型+II型≤5%,原始红细胞及幼红细胞比例基本正常。
M7型:粒细胞、红细胞二系比例正常,原始巨核细胞+幼稚巨核细胞基本消失。
急性淋巴细胞白血病:原始淋巴细胞+幼稚淋巴细胞≤5%。
(2)部分缓解(PR):骨髓原粒细胞I型+II型(原始单核+幼稚单核细胞或原始淋巴+幼稚淋巴细胞)>5%而≤20%;或临床、血象中有一项未达完全缓解标准者。
2.白血病复发 经治疗获CR后出现下列三者之一,即成为复发。
(1)骨髓原粒细胞I型+II型(原始单型+幼稚单核细胞或原始淋巴细胞+幼稚淋巴细胞)>5%而≤20%;或临床、血象中有一项未达到完全缓解标准者。
(2)骨髓原粒细胞I型+II型(原始单核+幼稚单核细胞或原始淋巴+幼稚单核细胞)>20%者。
(3)骨髓外白血病细胞浸润。
3.持续完全缓解(CCR)指从治疗后完全缓解之日起计算,期间无白血病复发达3-5年以上者。
4.长期存活 急性白血病自确诊之日起,存活时间(包括无病或带病生存)达5年或5年以上者。
5.临床治愈 指停止化疗5年或无病生存(disease free survival,DFS)达10年者。
说明:同级生存率时应包括诱导治疗不足一疗程者;诱导治疗满一个疗程以上的病例应归入疗效统计范围。
十三、慢性粒细胞白血病
【诊断标准】
1989年,第二届全国白血病治疗讨论会制定的慢性粒细胞性白血病(CML)的分歧诊断标准如下:
1.慢性期
(1)临床表现:无症状;或有低热、乏力、多汗、体重减轻等症状。
(2)血象:白细胞数增高,主要为中性中晚幼和杆状粒细胞,原始细胞(I型+II型)<5%-10%,嗜酸粒细胞和嗜碱粒细胞增多,可有少量有核红细胞。
(3)骨髓象:增生明显至极度活跃,以粒系增生为主,中晚幼粒细胞和杆状核粒细胞增多。原始细胞(I型+II型)<10%
(4)有Ph染色体。
(5)CFU-GM培养:集落或集簇较为正常明显增加。
2.加速期具有下列之二者,考虑为本期。
(1)不明原因的发热、贫血、出血加重和(或)骨骼疼痛。
(2)脾脏进行性肿大。
(3)非药物引起的血小板进行性降低或增高。
(4)原始细胞(I型+II型)在血和(或)骨髓中>10%。
(5)外周血嗜碱粒细胞>20%。
(6)骨骼中有显著地胶原纤维增生。
(7)出现Ph以外的其他染色体异常。
(8)对传统的抗CML药物治疗无效。
(9)CFU-GM增生和分化缺陷,集簇增多,集簇与集落比值增高。
3.急变期 具有下列之一者可诊断为本期。
(1)原始细胞(I型+II型)或原淋巴细胞+幼淋巴细胞或原单+幼单在外周血或骨髓中>20%。
(2)外周血中原始细胞+早幼粒细胞>
30%。
(3)骨髓中原始粒细胞+早幼粒细胞>
50%。
(4)有髓外浸润。
此期临床症状、体征比加速期更为恶化,CFU-GM培养呈小簇生长或不生长。
十四、慢性淋巴细胞白血病
【诊断标准】
综合近二十年内报告并参考国内外文献,拟定国内慢性淋巴细胞白血病(chronic lymphocytic leukemia,CLL)的诊断标准。
1.诊断条件
(1)临床表现
1)可有疲乏、体力下降、消瘦、低热、贫血或出血表现。
2)淋巴结(包括头颈部、腋窝、腹股沟)、肝、辟肿大。
3)少数人可有结外侵犯,如皮肤、乳腺、眼附属器官。
(2)实验室检查
1)外周血:WBC>10×109/L,淋巴细胞比例≥50%,绝对值≥5×109/L,形态以成熟淋巴细胞为主,可见幼稚淋巴细胞或不典型淋巴细胞。
2)骨髓象:增生明显活跃及以上,成熟淋巴细胞≥40%,活检淋巴细胞浸润情况可分3种类型:结节型、间质型、弥漫型。
3)免疫分型:B-CLL:SigM或IgM和IgD呈现弱阳性,呈k或x单克隆轻链型;CD5、CD19、CD79a、CD23、CD43阳性,CD20、CD22、CD11c弱阳性;CD10,CyclinD1阴性。
T-CLL:CD2、CD3、CD7阳性。TdT和CDla阴性。膜CD3表达弱阳性。60%CD4+/CD8-,25%CD4+/CD8+,15%CD4-/CD8+。
4)遗传学:B-CLL:>80%有染色体畸变:13q14.3,11q22-23,6q21,17p13.3缺失;三体12。P53基因表达见于15%CLL,多为晚期或临床进展病人。
T-CLL:大多有14q11~32键断裂倒位。t
(11;14)(q11;q32);idic(8p11),t(8;8)(P11~12;q12)、三体8,12p13缺失,少数人TCLL、TCL1b、ATM基因突变。
患者具备实验室检查第1)项+第2)项或第3)项中一项即可确定为CLL。遗传学改变作为重要参考条件。
2.形态学分型
(1)根据幼淋巴细胞及不典型淋巴细胞在淋巴细胞中所占的不同比例可将B细胞型慢性淋巴细胞白血病(B-CLL)分为三种亚型:
1)典型CLL:90%以上为类似成熟的小淋巴细胞。
2)CLL伴随幼淋巴细胞增多(CLL/PL):幼稚淋巴细胞>10%,但<54%。
3)混合细胞型:有不同比例的不典型淋巴细胞,但幼淋巴细胞小于10%。幼淋巴细胞体积大、核/浆比例减低,胞浆呈不同程度是碱性染色,有(或)嗜天青颗粒。
(2)T-CLL细胞形态分为以下四种:
1)大淋巴细胞型:多见、细胞体积较大、胞浆为淡蓝色,内有细或粗的嗜天青颗粒,胞核为圆形或卵圆形,长偏向一侧,染色质聚集成块,核仁罕见。
2)幼稚T细胞型:胞核嗜碱性增强、无颗粒、核仁明显。
3)呈脑回样细胞核的小或大淋巴细胞。
4)细胞形态多样,胞核多有分叶。
3.临床表现
(1)I期:淋巴细胞增多,可伴有淋巴结肿大。
(2)II期:I期+肝大或脾大或血小板减少(<100×109/L)。
(3)III期:I期/或II期+贫血(Hb<
110g/L)。
十五、多毛细胞白血病
【诊断标准】
1.临床表现 多有脾大、贫血、可伴有发热。
2.血常规检查 血红蛋白下降;白细胞可明显降低,正常或增高;血小板减少或正常。
3.骨髓检查 常呈“干抽”,也可增生活跃。
在骨髓和(或)外周血中见到多毛细胞,此为诊断本病的依据。多毛细胞特征如下。
(1)形态学:光镜下,直径10~15μm,大小不一,胞浆中等量,瑞氏染色呈蓝色,周边不规则,呈锯齿状或伪足突起,有时为细长毛发状。核呈椭圆,可有凹陷,偶见核仁。相差镜下。新鲜活体标本中的多毛细胞有细长毛状的胞浆突起。扫描电镜可正是上述发现,延伸的“毛”有交叉现象。透射电镜下,在胞浆内可见到核糖体-板层复合物(RLC)。
(2)细胞化学染色:酸性磷酸酶(ACP)阳性,不被酒石酸抑制(TRAP);糖原(PAS)阳性。
(3)免疫表现:sIg+,GD19+,CD20+,CD21-,CD22+,CD11c+,CD25+,CD103+。
(4)咐醇酯(TPA)反应:在体外培养下对小剂量TPA反应极为迅速,24小时内细胞可完全贴壁,并伴有长枝状突起。幼淋细胞白血病无此反应。
4.骨髓病理 增生活跃或低下,多毛细胞多呈散在或簇状分布。胞浆丰富、透明,胞核间距离宽,成“蜂窝”状。核染色质细,呈毛玻璃样。网状纤维轻度或增多。
十六、幼淋细胞白血病
【诊断标准】
1.临床表现 发现病龄多在50岁以上。起病缓慢,脾中、重度肿大,常有肝大。
2.实验室检查
(1)血象:轻至中度贫血。白细胞增高,也可正常。血小板减少。血涂片中,可见大量幼淋细胞(多少不一,2/3病人幼淋占60%)。
(2)骨髓象:增生明显活跃,以淋巴细胞为主。有核仁的幼淋巴细胞占17%-80%。
3.外周血和骨髓中出现大量幼淋巴细胞是确诊本病的必要条件。幼淋巴细胞的特点如下。
(1)形态学:光镜下胞体较大、圆形,胞浆较丰富。核染色质浓集成块状或粗细不等,尤其在核膜周边密集分布。大而明显的核仁,是幼淋细胞的突出特点,核质与核仁发育不同步。扫描电镜下,幼淋细胞有长0.7-2.5μm的毛状小突起,透射电镜下无核糖体——板层复合物(RCL)。
(2)细胞化学染色:80%糖原染色(PAS)阳性;酸性磷酸酶(ACP)阳性,酸性磷酸酶耐酒石酸实验(TRAP)阴性;其他如:过氧化物酶(POX)、各种酯酶均为阴性。
(3)免疫表现:多数B细胞表型。
十七、大颗粒淋巴细胞白血病
大颗粒淋巴细胞(LGL)占外周血单个核细胞的10%-15%,其中CD3+大颗粒淋巴细胞为激活的细胞毒T细胞,而CD3-者为NK细胞。大颗粒淋巴细胞白血病分为T细胞型和NK细胞型。
【诊断标准】
1.临床表现
(1)T-LGL型:反复感染,脾脏轻度肿大,可有全身B症状,部分患者症状类似风湿关节炎。
(2)NK-LGL型:B症状明显,肝脾肿大,淋巴结及胃肠道易受累。
2.实验室检查
(1)血象:白细胞计数中度升高,中性粒细胞明显减少。淋巴细胞数>5×109/L,其中大颗粒淋巴细胞占50%至90%,持续6个月以上。
(2)骨髓象:可见红系细胞增生低下,髓系细胞成熟障碍,大颗粒淋巴细胞呈间质性浸润,散在成团。
大颗粒淋巴细胞的形态学特点:胞浆丰富,浅蓝色,含有数个或粗或细的嗜天青颗粒。核圆或椭圆,染色质呈块状,核仁不易见到。酸性磷酸酶(ACP)染色强阳性,特异性酯酶(CE)阳性,非特异性酯酶(ANAE)染色弱阳性或阴性。
(3)免疫表型:可分为两类。
1)T-LGL:CD3+,CD8+,CD16+,CD57+,HLA-DR+,TCR阳性;CD4-,CD56-。
2)NK-LGL:CD2+,CD10+,CD56+;CD3-,CD4-,CD57-。
当患者反复感染带有外周血淋巴细胞持续升高、中性粒细胞明显减少时,应考虑本病。若细胞形态学特点及免疫表型符合上述标准,可作出诊断。
十八、类白血病反应
类白血病(lekemoid reaction)指并非由白血病引起的外周血白细胞计数增多、显著增多和(或)出现幼稚的血细胞,与某些白血病相类似,但随后病程或尸检证实没有白血病。在小儿,由于骨髓造血功能尚未成熟,易受各种病理因素刺激,因而较易发生类白血病反应,须注意鉴别。
【诊断标准】
综合国内外文献报告的类白血病反应,归纳如下。
1.有明确的病因 入眼中的感染、中毒、恶性肿瘤、大出血、急性溶血、过敏性休克、巨幼细胞贫血、服药史等。
2.实验室检查
(1)红细胞与血红蛋白测定值一般正常,血小板计数正常。
(2)粒细胞型类白血病反应:白细胞计数可多达30×109/L,以上,或外周血出现幼稚粒细胞;血象中成熟中性粒细胞胞浆中往往出现中毒性颗粒和空泡,骨髓象除了有增生、左移及中毒性改变外,没有白血病细胞的形态畸形等,没有染色体异常或BCR/abl融合基因阳性、成熟中性粒细胞碱性磷酸酶则明显增高。
(3)淋巴细胞型类白血病反应:白细胞计数轻度或明显增加,分类中成熟淋巴细胞占到40%以上,并可有幼稚淋巴细胞出现。
(4)单核细胞型类白血病反应:白细胞计数在30×109/L以上,单核细胞大于30%,并可有幼稚单核细胞出现。
(5)嗜酸粒细胞性类白血病反应:血象中嗜酸粒细胞明显增加,以成熟型细胞为主,骨髓象原始细胞不增多,也无嗜酸粒细胞形态异常以及Ph染色体等。
(6)浆细胞型类白血病反应:白细胞增高,外周血中的浆细分类计数增高,常>5%,同时可见幼稚浆细,但与之同时有中性粒细胞左移,单核细胞相应增多,骨髓象显示浆细胞系统增生活跃,但一般<20%,可减少量的幼浆细胞,甚至原浆细胞。
(7)红白血病型类白血病反应:外周血中有幼红及幼粒细胞,骨髓象除红细胞系增生外,尚有粒细胞系增生,但无红白血病中的细胞畸形。此外,还需排除其他骨髓疾病(如结合、纤维化、恶性肿瘤转移等)所致的幼粒幼红细胞增多症(leucoerythro-blastosis)。
(8)白细胞不增多型类白血病反应:白细胞计数不增多,但血象中出现幼稚细胞。
3.治疗结果 原发病经治疗去除后,血象变化随之恢复正常。
十九、传染性单核细胞增多症
【诊断标准】
传染性单核细胞增多症(infections mononucleosis)的诊断标准如下。
1.临床表现
(1)发热:热型不定,持续1~4周或更长后骤退或渐退。
(2)咽峡炎:常有咽痛、眼部充血。
(3)淋巴结肿大:常见,全身淋巴结均可累及,颈后三角区最常受累。
(4)肝脾肿大:30%~60%病例有肝大,多数半肝功能损害。24%~65%有脾大,肝脾肿大多数在肋下3cm以内。
(5)皮疹:10%~20%病例有皮疹,多数为斑疹或丘疹。
2.实验室检查
(1)血象:病程中不同阶段白细胞数可增多、正常或减少。淋巴细胞比例增高吗,异性淋巴细胞超过10%。
(2)嗜异性凝集试验:本病阳性率第一周为40%,第2~3周60%~80%,恢复期下降,体内持续时间为2~5个月。阳性时需做牛红细胞及豚鼠肾吸附实验,本病血清中存在嗜异性凝集抗体可被牛红细胞吸附而不被豚鼠肾吸附。少数正常人、结核病、淋巴瘤、白血病等嗜异性凝集试验也可呈阳性,但效价均较低,而且可被豚鼠肾完全吸收。血清病嗜异性凝集试验也呈阳性,但可被豚鼠肾和牛红细胞完全吸附。
(3)抗EB病毒抗体检查:抗病毒壳抗原(viral capsid antigen,VCA)VCA-IgM抗体出现早,阳性率高,是急性期重要的诊断指标,但持续时间仅为4-8周。VCA-IgG阳性出现在临床症状开始时,并持续终身。
3.除外传染性单核细胞增多综合征 由其他病毒(如巨细胞病毒、人类免疫缺陷病毒、单纯疱疹病毒、风疹病毒、腺病毒、肝炎病毒等)、某些细菌、原虫等感染以及某些药物引起,外周血中出现异型淋巴细胞,但嗜异性凝集试验和VCA-IgM抗体一般阴性。
具备上述第一项中任何三条,第二项中任何两条。再加上第三项,可诊断为传染性单核细胞增多症。
二十、特发性嗜酸粒细胞增多综合征
嗜酸粒细胞增多综合征,为一组石酸粒细胞持续升高,并伴有器官损害的疾病。最早在1968年由Hardy等描述。由于其原因不明,故又称特发性(ldiopathic)嗜酸粒细胞增多综合征。
【诊断标准】
1975年,Chusid等提出嗜酸粒细胞增多综合征(hypereosinophilic syndrome,HES)的诊断标准,沿用至今。
(1)外周血嗜酸粒细胞>1.5×109/L,并持续6个月以上,或出现临床症状后,于6个月内死亡。
(2)有器官受累的症状或体征。
(3)未发现导致嗜酸性粒细胞增多的原因。
【疗效标准】
本病目前尚无公认的疗效标准,现参考有关文献拟定如下:
(1)完全缓解:外周血嗜酸粒细胞计数正常(<0.45×109/L);受累器官的症状与体征完全消失,功能恢复正常;持续4周以上。
(2)部分缓解:外周血嗜酸粒细胞计数<1.5×109/L或较治疗前减少50%以上;症状及器官受累情况减轻。
(3)稳定:未达到部分缓解标准,但病情无进展。
(4)无效:外周血嗜酸粒细胞计数较治疗前升高,器官受累持续存在或加重。
二十一、骨髓增生异常综合征
骨髓增生异常综合征(Myelodysplastic Syndromes,MDS)是一组异质性克隆性造血干细胞疾病,其生物学特征是髓系细胞(粒系、红系、巨核系)一系或多系发育异常(或称病态造血,disordered maturation or myelo-dysplasia)和无效造血,可以伴有原始细胞增多。临床和血液学特征是外周血细胞一系或多系减少,骨髓有核细胞增多且形态异常,可伴有原始细胞增多,转化为急性髓系白血病的危险性明显增加。
【诊断标准】
1.诊断条件
(1)临床表现常以贫血为主,可兼有发热或出血。初期可无症状。
(2)外周血一系或多系减少。
(3)骨髓有核细胞增多,髓系细胞一系或多系呈发育异常的病态造血形态学表现。
(4)能除外叶酸或维生素B12缺乏、重金属中毒、微小病毒B19或HIV病毒感染、应用粒细胞集落刺激因子等引起的非克隆性血细胞发育异常。
(5)以下实验室检查结果有助于诊断本病。①骨髓组织切片显示造血细胞空间定位紊乱,或ALIP(+)(详见后文)。②有非随机性-5/5q-、-7/7q-、+8、20q-等MDS常见的核型异常。③血细胞克隆性分析提示单克隆造血。④姊妹染色单体分化(SCD)试验延迟,或有其他造血细胞,细胞周期延长的证据。⑤造血细胞有ras或fms等MDS可有的癌基因异常。
2.血细胞发育异常(病态造血)的形态学表现 红细胞发育异常(dyserythropoiesis,dysE)外周血中大红细胞增多,红细胞大小不均,可见到巨大红细胞(直径>2个红细胞)、异型红细胞、点彩红细胞,可出现有核红细胞。骨髓中幼红细胞巨幼样变,幼红细胞可有多核、核型不规则、核分叶、核出牙、核碎裂、核间桥、Howell-Jolly小体,早期细胞胞浆可有小突起,可出现环状铁粒幼细胞。成熟红细胞形态改变同外周血。
(1)粒细胞发育异常(dysgranulopiesis,dysG):外周血中中性粒细胞颗粒减少或缺失,胞浆持续偏于嗜碱,个体小,分叶少,假性Pelger-Huet样核异常,或核分叶多(hrperseg mentation)。骨髓中出现异型原粒细胞(I型,II型),幼粒细胞核浆发育不平行,嗜天青颗粒粗大,消退延迟,中型颗粒减少或缺如;幼粒细胞巨型变,可见环形核幼粒细胞。成熟里细胞形态改变同外周血。异型原粒细胞形态特征如下:I型的形态特征与正常原粒细胞基本相同,但大小可有较大差异,核型可稍不规则,核仁明显,胞浆中无颗粒。II型的形态特征同I型,但胞浆中有少数(<20个)嗜天青颗粒。
(2)巨核细胞发育异常(dysmegakaryocytopoiesis,dysMK):外周血中可见到巨大血小板。骨髓中出现小巨核细胞(细胞面积<800μm2),包括淋巴细胞样小巨核细胞,小圆核(1~3个核)小巨核细胞,或有多个小核的大巨核细胞。一般的巨核细胞也常有核分叶明显和包教颗粒减少的给便。淋巴细胞样小巨核细胞形态特征如下:类圆形,直径5~8μm,核浆较大,核染色质浓聚,结构不清,无核仁,胞浆极少,强嗜碱性,常有不规则的毛状或小泡状突起,无颗粒或颗粒极少。
3.骨髓组织切片所见
(1)造血组织面积增大(>50%)或正常(30%~50%)。
(2)造血细胞定位紊乱:红系细胞和巨核细胞不分布在中央窦周围,而分布在骨小梁旁区或小梁表面;粒系细胞不分布于骨小梁表面,而分布在小梁间中心区,并有聚集成簇的现象。
(3)(粒系)不成熟前体细胞异常定位(abnormal localization of immature precursors,ALIP)现象:原粒细胞和早幼粒细胞在小梁间中心区形成集丛(3~5个细胞)或集簇(>5个细胞)。每张骨髓切片上都能看到至少3个集丛和(或)集簇为ALIP(+)。
(4)基质改变:血窦壁变性、破裂、间质水肿,骨改建活动增强,表现为骨吸收,小强中有破骨细胞及骨样组织表面排列着成骨细胞,网状纤维增多等。
4.治疗相关或疾病相关MDS 过去(常为4~6年前)曾接受细胞毒药物化疗或放射治疗而发生的MDS,可诊断为治疗相关MDS(therapy-relatedMDS,t-MDS)。可有以下特点:①多系血细胞发育异常;②骨髓增生减低的现象相对多见;③染色体核型异常发生率高,且多为复杂核型异常;④常持续进展,转化为AML。
某些疾病如自身免疫性疾病伴发的MDS称疾病相关性MDS。
5.分型标准
(1)FAB协作组的MDS分型:1982年法、美、英(FAB)协作组将MDS分为5个亚行,即难治性贫血(RA)、难治性贫血伴有环状铁粒幼细胞(RARS)、难治性贫血伴有原始细胞过多(RAEB)、转化中的RAEB(RAEB-t)和慢性粒单核细胞白血病(CMML)。
(2)世界卫生组织(WHO)的MDS分型:2001年WHO的“造血组织和淋巴组织肿瘤”分类中,将MDS分型在FAB分型基础上修订如下:
1)重申只有骨髓红系一系发育异常即可诊断为RA或RARS。
2)增加一个“难治性血细胞减少伴有多系发育异常(refactory cytopenia with multilineage dysplasia,RCMD)”新亚型。
3)将5q-综合征纳入MDS作为一个亚型。
4)将RAEB再分为RAEB-I和RAEB-II两个亚型。
5)将MDS与急性髓系白血病(AML)的骨髓原始细胞分界线降低为20%,取消RAEB-t亚型。
6)将CMML归入一个新的骨髓增生异常/骨髓增殖综合征(MDS/MPD)大类,不再作为MDS的一个亚型。
7)增设MDS不能分类亚型。
8)有t(8;21),t(15;17),inv(16)/t(16;16)核型异常者,即使骨髓原始细胞<20%亦不诊断为MDS相应亚型,而直径诊断为AML。
(3)儿童MDS:成年儿童MDS的表现与成人基本相同,但婴幼儿的MDS则有一些不同的特点:1在FAB亚型方面以幼年型粒单核细胞白血病(juvenil myelomonocytic leukemia,JMML)最多,其次为RAEB/RAEB-t,而RARS罕见。WHO髓系肿瘤分类中已将JMML归入MDS/MPD大类之中。2可合并其他先天性异常。3个别患儿可自发缓解。
(4)MDS合并骨髓增生低下:诊断所谓的“增生低下型MDS”必须有骨髓切片的组织学证据,即骨髓组织切片中造血阻滞面积缩小((60岁以下患者造血阻滞面积<30%,60岁以上患者<20%)此外,有以下各种发现有助于“MDS合并骨髓增生低下”的诊断:①血片中能见到发育异常的中性粒细胞或I/II型原始细胞。②骨髓涂片中能见到发育异常的粒、红、巨核系细胞,能见到I,II型原始细胞,特别是小巨核细胞。③骨髓切片中能见到小巨核细胞,早期粒系细胞相对多见或ALIP(+),网状纤维增加。④骨髓细胞有MDS常见的克隆性染色体异常。⑤能证明单克隆造血。
6.MDS的预后评估 1997年,国际MDS危险分析专题研习会提出一个MDS预后积分系统(International Prognostic Scoring System,IPPSS):选定了3个预后参数,给予相应积分,根据积分将MDS分为低危、中危I、中危II、高危4个危度。
二十二、骨髓增生异常/骨髓增殖性疾病
骨髓增生异常/骨髓增殖性疾病(MDS/MPD)是一组克隆性造血组织肿瘤性疾病,在就诊时既有一些临床、实验室或形态学表现符合MDS,又有另一些表现符合慢性骨髓增殖性疾病。其临床和血液学特点是骨髓髓系有核细胞增多,其中一系或多系是有效增殖,导致外周血中该系细胞增多,而另一系或多系是无效增殖,导致外周血该系细胞减少。同时,髓系各系细胞可有发育异常的形态学表现或功能异常。
2001年WHO髓系肿瘤分类中将之新设为一类,包括:
(1)慢性粒单核细胞白血病(chronic myelomonocytic leukemia ,CMML).
(2)不典型慢性髓系白血病(atypical chronic myeloid leukemia,aCML).
(3)幼年型粒单核细胞白血病(juvenile myelomoncytic leukemia,JMML)。
(4)MDS/MPD,不能分类(MDS/MPD,U)。
【诊断标准】
1.CMML的诊断标准
(1)持续性PB单核细胞增多,>1×109/L。
(2)Ph(-),BCR/ABL(-)。
(3)PB或BM原始细胞<20%。
(4)髓系中1个或1个以上细胞系别有发育异常;如无发育异常或极微,但其他条件符合,且有以下表现者,仍可诊断为CMML:骨髓细胞有获得性克隆性细胞遗传学异常,或单核细胞增多已持续至少三个月,而且除外可引起单核细胞增多的其他原因。
(5)原始细胞PB中<5%,和BM中<10%者,诊断为CMML-1原始细胞PB中5%-19%,或BM中10%-19%者,诊断为CMML-2。
(6)符合以上诊断标准且PB嗜酸粒细胞≥1.5×109/L者,诊断为CMML-I或CMML-II伴有嗜酸粒细胞增多。
注:诊断CMML是,原始细胞包括原始粒细胞、原始和幼稚单核细胞。
2.aCML的诊断标准
(1)PB中WBC增多,主要由于成熟和不成熟中性粒细胞增多。
(2)显著的粒系细胞发育异常。
(3)Ph(-),BCR/ABL(-)。
(4)幼稚中性粒细胞(早幼-晚幼)≥10%WBC。
(5)无绝对性嗜碱粒细胞增多,或极微;时间粒细胞<2%WBC。
(6)无绝对性单核细胞增多,或极微;单核细胞<10%WBC。
(7)BM组织切片有核细胞增多,粒系增多且有发育异常,伴有或不伴有红系和巨核系发育异常。
(8)PB或BM中原始细胞<20%。
3.JMML的诊断标准
(1)PB单核细胞增多>1×109/L。
(2)原始细胞(包括原、幼单核细胞)少于外周血白细胞或BM有核细胞的20%。
(3)Ph(-),BCR/ABL(-)。
(4)外加下列三项中的任何两项:
1)HbF高于年龄应有值。
2)PB中有不成熟粒细胞。
3)WBC>10×109/L,克隆性染色体异常(常为7单体)。
(5)粒单系祖细胞在体外培养中对GM-CSF高度敏感。
4.MDS/MPD,U的诊断标准
(1)临床、实验室和形态学特征符合MDS的任何一个亚型,PB和BM中原始细胞<20%。
(2)具有显著的MPD特征,如PLT≥600×109/L伴有巨核系增殖,或WBC≥13×109/L,伴有或不伴有脾脏肿大。
(3)无先期MDS或CMPD,近期未接受细胞毒药物或造血生长因子治疗,Ph`(-),BCR/ABL(-),无5q-、t(3;3)(q21;q26)或inv(3)(q21;q26),或具有混合型MPD和MDS特征而不能归入任何一个MDS、CMPD或MDS/MPD亚型。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















