基因治疗的基本原理原则是把目的基因物质转移到个体内,在分子水平改变其细胞结构或功能从而达到治疗目的。基因改变后最终合成治疗性蛋白质并分泌到周围环境从而发挥治疗作用。该蛋白质在细胞膜表面表达或者作为信号分子来影响细胞或者组织的行为。因此,基因治疗技术即通过合成蛋白质来治疗甚至治愈急慢性疾病。基因治疗有两种常用的方式。一种是直接方式,即把治疗基因直接转移到活体内的目标体细胞内;另一种是非直接方式,即是获取患者的细胞,进行基因修饰之后再回输到患者体内。这两种方式中,直接治疗方式操作简单,在临床上的应用潜力更大。体外技术可能更加复杂,但是相对来说比较安全。在选择合适的方法时,必须考虑疾病的种类、治疗疾病的目的基因以及所需要的载体等因素。
把目的基因信息转移到细胞核内并产生蛋白质的过程称为转染,其有两种作用方式(图11-1)。病毒是进行转染的理想载体,但是对该方法的要求较高,且产生病毒相关疾病的风险增高。但是这些风险通常由于病毒有效转染细胞的能力而被忽略不计,而且在向宿主转移DNA的过程中病毒载体也不会激发宿主的免疫反应。
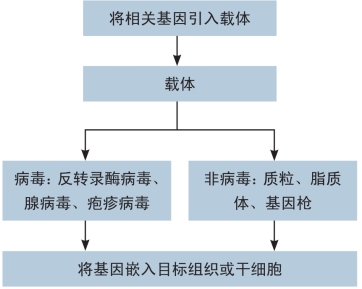
图11-1 基因疗法的原则和不同的载体
反转录病毒是最常用的基因治疗工具。它不会感染不发生分裂的细胞。腺病毒、疱疹病毒和腺相关病毒都可以用于活体直接转染和体外间接转染。反转录病毒是RNA病毒,能把病毒基因反转录形成双链DNA嵌合到宿主DNA上,从而允许宿主细胞器产生病毒组件。由于病毒基因嵌入到宿主DNA,来自感染细胞的基因都会传递给子细胞。
目前,最常用的反转录病毒来源于小鼠白血病病毒。大多数的临床试验应用都是基于小鼠白血病病毒的载体。小鼠白血病病毒自身的特性使人们喜欢将其用来作为基因疗法的载体。人们之所以认为这一病毒是非常安全的选择,是因为小鼠白血病病毒对于人类来说是不致病的。此外,由于它很少与人类反转录病毒同源,载体和人类固有的病毒间重组的风险很低。
和反转录病毒相比,腺病毒在感染宿主细胞后不是将其基因组整合到宿主的基因组里面,而是作为一个附加成分留存在细胞核内。所有的腺病毒载体均具有易于纯化和浓缩,感染宿主细胞有效率高的优点。这些优点使病毒载体非常适合用于活体直接基因转移。单纯疱疹病毒的优点在于其体积大,具有宽频活动性及持续表达基因,然而单纯疱疹病毒也有它的局限性,包括低感染率、存在野生型、基因组过大等,这使其比其他病毒载体更加难以操控。
非病毒载体可分为三类,由各种与细胞整合的遗传物质组成。包括可以注射的裸相DNA(通常是质粒)、脂质体或粒子介导的基因转移(基因枪)。为了促进靶组织摄取DNA,遗传物质可以被放入脂质体或包被到微小注射物(如金、钨)中。这些微粒可以通过基因枪的氦气压力或者高压放电而加速运动,从而携带足够的能量去穿透细胞膜。非病毒载体非常便宜,可以大批量生产。这些载体具有有限的免疫原性,可以重复应用,而且它们不可能重组,不会形成一个完整的病毒从而导致疾病的发生,所以被认为是更加安全的选择。然而,与病毒载体相比,它们的基因转移率较低。
非病毒基因转移的最新技术是将cDNA加载到多孔生物材料支架上,直接将后者包扎到创面上,随后将基因转入到向患处迁移的内源性细胞内。这种技术被称作基因活化基质(gene-activated matrix,GAM),是生产组织工程用的生物降解聚合物的扩展研究。
基因疗法在治疗疗效和安全性上有其局限性。其可能作为严重疾病如癌症、囊性纤维化等的最后治疗手段,但是在选择性重建术中其副作用的风险可能令人难以接受。此外,将病毒载体整合进宿主的基因组时可能伴有插入性基因突变的风险。不可控制的细胞生长、生长因子和细胞因子长期过度表达产生的慢性毒性,理论上可能产生恶性肿瘤,但还尚未有相关病例报道。然而,目前还无法保障嵌合的DNA序列不会引起多年后的突变或恶性肿瘤。大多数的基因疗法临床试验是使用体外培养的方法,因此病毒是不能直接进入患者身体细胞的,这些细胞需要通过大量的检验后才能够用于移植。
转移的基因在几周后失去表达是一种常见的现象,其机制不明。然而,短暂的和自限性的基因表达可用于肌肉骨骼损伤的治疗,这种短暂高水平的生长因子可以促进伤口愈合。目前的研究还致力于开发在基因转录表达和调节过程中需要的与功能性基因相邻的特定可诱导DNA序列。
细胞治疗已成为再生医学的一个重要的战略手段。组织工程细胞成分间的相互作用是修复受损或患病组织的核心问题。临床治疗的先决条件是需要能够提供多能细胞的可靠来源,获取细胞时造成的致病率低,这些细胞可以被精确调控、塑型以及整合入组织。由此看来,成体干细胞非常适合这一角色。不过前提是需要创建一个适合不同类型细胞存活的培养环境。
基因工程可能掌握着识别和调控细胞发育和分化决定基因的关键。尽管目前还没有已经批准的可用于临床的治疗技术,不过基因工程在未来肌肉骨骼损伤治疗中的应用潜力相当巨大。目前,只有几个有效的软骨重建基因治疗技术在人体关节上得到了验证。许多研究已经成功地验证了这些技术的可行性,即基因可以传递到不同的骨骼肌肉系统组织。除此之外,初步实验研究表明在体外和体内转导基因(特别是骨形态发生蛋白-2,胰岛素样生长因子-1、转化生长因子β)均可以出现阳性效应。目前我们遇到的主要障碍似乎是怎样得到携带有效基因的载体,以及病毒载体的安全性等问题。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















