实验技术六 乙醚的制备
【实验目的】
(1)掌握实验室制备乙醚的原理和方法。
(2)初步掌握低沸点易燃液体的操作要点。
【实验原理】
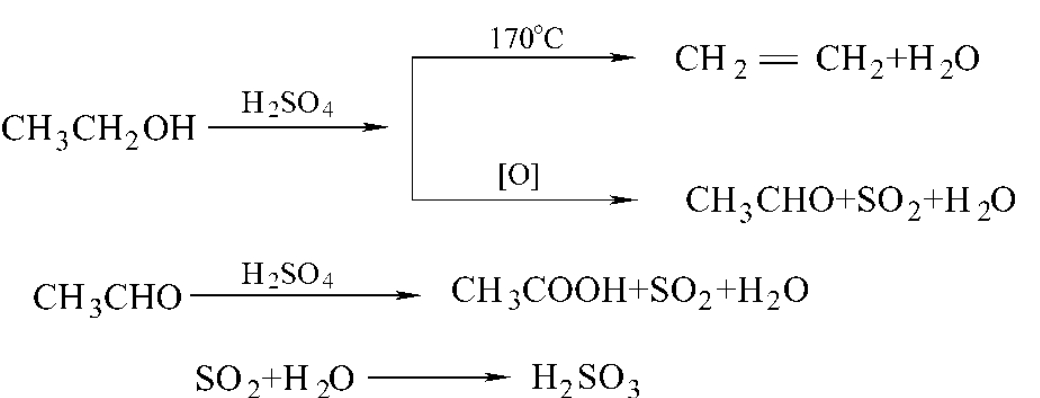
主反应:

总反应式:

副反应:
【仪器及药品】
1.仪器
电热套、水浴锅、三角烧瓶、滴液漏斗、温度计、冷凝管、接收器、折射仪。
2.药品
乙醇、浓H2SO4、5%NaOH溶液、饱和NaCl溶液、CaCl2(饱和溶液)、无水CaCl2。

图5-5 乙醚制备实验装置
【实验步骤】
1.乙醚的粗制
(1)在干燥的三角烧瓶中加入12mL乙醇,缓缓加入12mL浓H2SO4,混合均匀。
(2)滴液漏斗中加入25mL乙醇。
(3)按图5-5连接好装置。
(4)用电热套加热,使反应温度比较迅速地升到140℃。开始由滴液漏斗慢慢滴加乙醇。
(5)控制滴入速度与馏出液速度大致相等(每秒1滴)。
(6)维持反应温度在135~145℃内,30~45min滴完,再继续加热10min,直到温度升到160℃,停止反应。
2.乙醚的精制
(1)将馏出液转至分液漏斗中,依次用8mL 5%NaOH,8mL饱和NaCl溶液洗涤,最后用8mL饱和CaCl2溶液洗涤两次。
(2)分出醚层,用无水CaCl2干燥。
(3)分出醚,蒸馏收集33~38℃馏液。
(4)计算产率。
【注意事项】
(1)在反应装置中,滴液漏斗末端和温度计水银球必须浸入液面以下,接收器必须浸入冰水浴中,尾接管支管接橡皮管通入下水道或室外。
(2)控制好滴加乙醇的速度(每秒1滴)和反应温度(135~145℃)。
(3)乙醚是低沸点易燃的液体,仪器装置连接处必须严密。在洗涤过程中必须远离火源。
【问题讨论】
(1)本实验中,把混在粗制乙醚里的杂质一一除去,需采用哪些措施?
(2)反应温度过高或过低对反应有什么影响?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。

















