第七节 仪器工作条件的选择
一、分析线
原子吸收强度直接正比于谱线振子强度和处于基态的原子数。从灵敏度的观点出发,通常选择由基态向第一激发态跃迁的共振吸收线做分析线,这是因为由基态向第一激发态跃迁的共振线具有最大的振子强度,而且,在3000℃以下,处于基态的原子数近似地等于总原子数,这也就是说,由基态向第一激发态跃迁的共振线一般说来也就是最灵敏的吸收线。
在选择分析线时,还要考虑其他谱线的干扰,在分析线附近不得有其他非吸收线存在。例如镍共振线Ni 232nm附近有几条非吸收或吸收很差的原子线Ni 231.98nm和Ni 232.14nm及离子线Ni 231.6nm,使用很窄的光谱通带也难于将它们完全分辨开,因此,人们宁愿选用吸收系数稍低的Ni 341.48nm做分析线。
分析线的选择还受到背景吸收的限制。在200nm以下,大气、火焰气和光学元件相当明显地吸收来自光源的共振辐射,对于As、Se、Hg等,其共振吸收线位于远紫外区,背景吸收强烈,这时就不宜选择这些元素的共振线做分析线,可以考虑选择波长较长的次灵敏线。
即使灵敏线不受干扰,在实际工作中,也未必都要选用灵敏线,灵敏线往往用于测定痕量元素,在分析高浓度试样时,有时选取灵敏度较低的次灵敏线,以便得到适度的吸光度值,改善校正曲线的线性范围,减少不必要的稀释操作。最适宜的分析线,应视具体情况由实验来决定。实验的方法是:首先扫描空心阴极灯光源的发射光谱,了解有哪几条可供选用的谱线,然后喷入适当浓度的分析元素标准溶液,查看这些谱线的吸收情况,应当选用不受干扰而且吸光度值适当的谱线为分析线。最强的吸收线是最适宜于测定痕量元素的。
一个元素若有多条分析线,通常采用灵敏线,但也要根据样品中被测元素的含量来选择。例如测定钴时,为了得到最高灵敏度,应使用240.7nm谱线,但要得到较高精度,而且钴的含量较高时,最好使用352.7nm谱线。有时还要考虑干扰问题,如测定铷时,为了消除钾、钠的电离干扰,可用798.4nm代替780.0nm。测定铅时,为了克服短波区域的背景吸收和噪声,不使用217.0nm灵敏线而用283.3nm次灵敏线。
二、光谱通带
它是指单色器出口狭缝包含波长的范围。光谱通带的宽度直接影响测定的灵敏度和标准曲线的线性范围,作为一般原则来讲,应该这样来决定狭缝的宽度,即在不减小吸光度值的条件下,在能将邻近分析线的其他谱线分开的情况下,尽可能使用较宽的狭缝。这样可以增加光强,使用小的增益以降低检测器的噪声,从而提高信噪比与改善检出限,对测定有利。对于有复杂谱线的元素如铁、钴、镍等来说,要求选择较窄的通带,否则会带来光谱干扰,使分析灵敏度下降和工作曲线弯曲。因为吸收线的数目比发射线的数目少得多,所以谱线重叠的几率也会少得多,因此在原子吸收光谱分析时,允许使用较宽的狭缝。
合适的狭缝宽度可用实验方法确定,其方法为将分析元素的标准溶液喷入火焰中,调节狭缝宽度,测定不同狭缝宽度时的吸光度。当狭缝增宽到一定程度,其他谱线或非吸收谱线出现在光谱通带内,吸收度值就立即开始减小。不引起吸收值减小的最大狭缝宽度,就是应当选用的最合适的狭缝宽度。
三、灯电流
在保证稳定放电和合适的光强输出的前提条件下,尽可能选用较低的工作电流。灯电流过高,可导致热变宽和压力变宽,并增加自吸收,反而使辐射的光强度降低,结果是灵敏度下降,校正曲线下弯(弯向浓度轴),灯寿命缩短。寻找最佳工作电流的方法是固定其他测量条件,吸喷某一固定浓度的溶液,改变灯电流和负高压数值,测量吸光度值,然后绘制吸光度—灯电流关系曲线,从中选择灵敏度高,负高压在300~800V之间的灯电流值为工作电流。为了使空心阴极灯发射强度稳定,一般需预热10~30min,对大多数元素而言,应采用额定电流的40%~60%。较小的灯电流可提高测定灵敏度和延长灯的使用寿命。
四、对光
在调节燃烧头时,使其缝口正好在光束的中央,升高或降低燃烧器,使光束正好在缝口上方。点燃火焰,吸入一个标准溶液,对燃烧器再进行调节,直到获得最大吸光度值。
五、火焰的选择
不同的元素可选择不同种类的火焰,原则是使待测元素获得最大原子化效率。易原子化的元素用低温火焰,反之就需要高温火焰。当火焰选定后,要选择合适的燃助比,对于难原子化的元素,易选用富燃火焰,易原子化的元素选用贫燃火焰或化学计量焰,调节时,吸入一个标准溶液,固定助燃气的流量,逐步改变燃气的流量,得到最大的吸光度值和稳定的火焰。
六、燃烧器的高度和角度
调节火焰燃烧器高度的目的,是使来自空心阴极灯的辐射从自由原子浓度最大的火焰区域通过,以获得最大灵敏度。首先从灵敏度和稳定性来考虑,选择适宜的高度;遇到干扰时,再改变其高度以设法避免干扰。若干扰仍然存在,应考虑采用其他消除干扰的方法。其调节方法是在其他测试条件不变的情况下,吸喷待测元素的标准溶液,改变燃烧器高度,测定其吸光度值,绘制吸光度对燃烧器高度的关系曲线,找出最佳燃烧器高度。
通常情况下,燃烧器的角度为0°,即燃烧器缝口与光轴方向一致。在测定高浓度样品时,可选择一定的角度,当角度为90°时,灵敏度仅为0°的1/20。
【相关链接】
一、朗伯—比尔定律
1852年,比尔(Beer A)对朗伯(Lambert)定律作了详细的验证,二者结合起来称为朗伯—比尔定律,也称为光的吸收定律。
![]()
式中,A为吸光度,K为比例常数。
上式是朗伯—比尔定律的数学表达式。它表明:当一束单色光通过含有吸光物质的溶液后,溶液的吸光度A与吸光物质的浓度C及吸收层厚度成正比。因此可以方便地用标准系列做出工作曲线后,从待测物的吸光度大小,求得其含量。这是进行定量分析的理论基础。式中比例常数K与吸光物质的性质、入射光波长及温度等因素有关。
实践证明,溶液对光的吸收程度,与溶液浓度、液层厚度及入射光波长等因素有关。如果保持入射光波长不变,则溶液对光的吸收程度只与溶液浓度和液层厚度有关。
对固定频率的光,原子蒸气对它的吸收是与单位体积中原子的浓度成正比并符合朗伯—比尔定律。在原子吸收光谱法中,原子池中激发态的原子和离子数很少,因此蒸气中的基态原子数目实际上接近于被测元素总的原子数目,与试样中被测元素的浓度c成正比。因此吸光度A与试样中被测元素浓度c的关系如下:
![]()
式中,K为吸收系数。
二、灵敏度、检出限、精密度、准确度
在所有光谱化学分析中,都涉及被测元素浓度c和测量值A。所谓“分析函数”(Ana-lytical function),就是表征测量值A与元素浓度c之间的函数关系,即
![]()
采用坐标轴绘制分析函数的图形曲线,称作分析曲线(Analytical curve)。对火焰原子化方式而言,通常宜配制8份吸光度在0.05~1.0范围内的标准溶液来绘制标准曲线。当然,对具有干扰效应的系统,元素i的测定值Ai,不仅取决于元素i的浓度ci,也取决于其他共存元素的浓度。因此分析曲线可表示为,
![]()
评定一个分析方法,可以用其灵敏度、检出限、精密度和准确度来衡量。
1.灵敏度
在光谱化学分析中,灵敏度S被定义为:
![]()
可见,灵敏度S的物理意义是浓度c的变化(dc),引起测量值x的改变程度(dx)。显然,灵敏度S就是分析工作曲线的斜率,斜率大,则灵敏度高。即元素浓度c的微小变化(dc),将引起测量值较大的改变(dx)。
在原子吸收光谱分析中,常采用“特征浓度”(Characteristic concentration),来表示灵敏度。
特征浓度就是能产生1%吸收(即吸光度为0.0044A)信号时所对应的待测元素浓度。假定C是待测溶液浓度,A是待测溶液的吸光度,那么:C∶A=S*∶0.0044。从而得到1%吸收灵敏度(特征浓度)的计算公式:
![]()
显然,S*(特征浓度)越小,S就越大,则分析灵敏度越高。
对于石墨炉原子吸收光谱分析法,往往采用绝对灵敏度的概念。绝对灵敏度就是能产生1%吸收(0.0044A)信号时所对应的待测元素量,用pg/0.0044A或g/0.0044A表示,计算公式为:
![]()
式中,C是待测溶液浓度,单位为微克/毫升;
l是待测溶液体积,单位用微升;
A是待测溶液的吸光度。
计算时要注意单位换算,用pg/0.0044A或g/0.0044A表示。由此可见,所谓灵敏度高,表示S的数值大,分析工作曲线斜率也大,而相应的“特征浓度”S*的数值则是小的。
2.检出限CL
检出限通常用CL表示。其含义是指在给定的分析条件下,能被合理检测出的最小测定值XL,表示为:
![]()
式中,xb1是空白溶液测定的平均值(吸光度值);Sb1是空白溶液吸光度值测定的标准偏差。空白溶液是指组成与样品相同的不含被测元素的溶液;K是置信因子。
显然,xL是一个被检测到的确定值(信号),其大小取决于空白测定值的大小及其重现性。检出限浓度CL则可由此最小值xL导出。这里差值xL-xb1=KSb1表示被合理检测出的“净测量值”。显然,它对应的浓度值即为CL。我们假定一个浓度为c的试验溶液的吸光度为A。那么,与“净测量值”KSb1相比较则得:
![]()
所以,检出限为
![]()
式中,A是试验溶液(浓度为C)多次测定的平均吸光度。规定C的浓度要很小,一般为CL的2至5倍,对有限次(通常是10次或20次)测定而言,空白溶液吸光度测定值的标准偏差Sb1,可用σ代替。
![]()
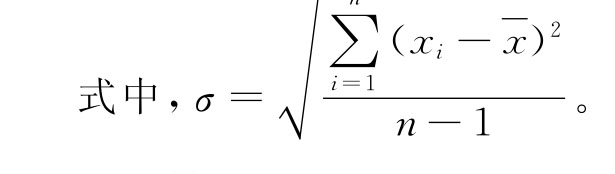
早期,在原子吸收光谱测定法中,人们选择K=2。但是对极低浓度测量而言,误差分布曲线可能是非高斯型的。另一方面,空白标准偏差实际是通过有限次数测量来计算的。因此,就实际意义而言,K=3相应的实际置信水平只有90%,K=2就更小了。因此,1975年,国际纯化学和应用化学联盟(IUPAC)通过规定,强调并建议置信因子取K=3。那么,检测限浓度计算公式为:
![]()
单位用μg/mL表示。由此可见,检出限浓度CL可定义为3倍噪声电平所对应的元素浓度。噪声电平由空白溶液吸光度值的标准偏差求出。
3.精密度
精密度(亦称再现性),它反映的是一组测量结果的波动性,即同一试样多次测定结果的再现性。精密度高也就是再现性好。在分析化学中,有时还使用重复性(Repeatabili-ty)和再现性(Reproducibility)来表征精密度。重复性系指在同一条件下同一操作者多次测定结果数值的接近程度。而再现性则指不同实验室,不同操作者各自独立测定结果数值的接近程度。标准偏差能较好地反映测量过程的精密度。因此,在原子吸收光谱测定法中,精密度习惯用相对标准偏差来表示。
显然,精密度取决于偶然误差的大小。表示精密度应指明测定次数和相应的含量范围。最好是列出各次测定的数值。
4.准确度
“准确度”意味着测定结果与“真值”之间的符合程度。它取决于偶然误差和系统误差。准确度用绝对误差或相对误差表示。
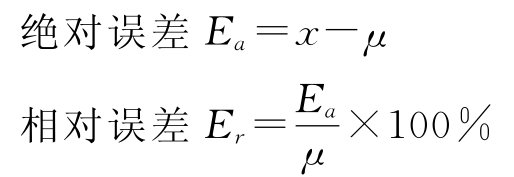
式中,x是测量值,μ是“真值”。我们知道,“真值”是不可知的。但可以在没有系统误差时,通过多次测定的算术平均值T来接近“真值”μ,即:

在实际分析中,人们往往取国家标准样品或“管理样”作“真值”来考察所制定方法的准确度。
5.准确度和精密度的关系
我们以A、B、C三人分别“射箭”的结果来说明。如图6-4所示。
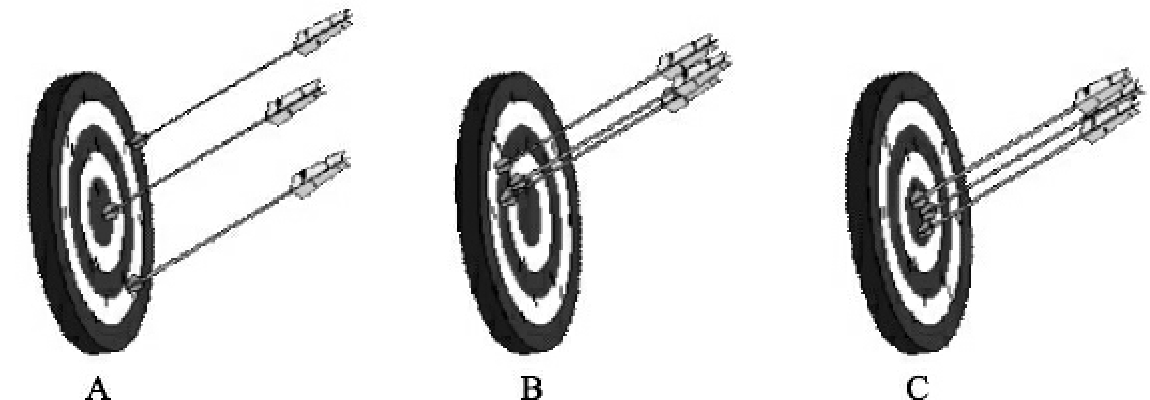
图6-4 准确度和精密度的关系
A表明“精密度”和“准确度”都差;B表明“精密度”高,但“准确度”差;C表明“精密度”和“准确度”都好。
6.试样的污染及预防措施
原子吸收分光光度分析通常用来测定微量元素,同其他微量分析一样,要严防污染。一般认为周围的气氛、容器、水、试剂等都是影响测定结果的主要因素。
(1)气氛污染。实验室空气中的有害气体、气溶胶、尘埃等,均能造成污染。这种污染很难校正,应尽量设法予以避免。
(2)容器污染。容器污染相当严重。容器的材质不同,污染程度也不相同,因此要特别注意容器的选择、清洗及贮藏,以减少污染。同时还必须注意容器表面吸附所造成的损失。
容器必须洗净,用铬酸清洗不好。通常可根据待测元素的种类、容器的使用经历等情况选择适宜的清洗方法,这一点是很重要的。原子吸收光谱分析,常使用20%硝酸浸泡实验器皿24h,然后用去离子水冲洗干净。
(3)试剂污染。分解试样或酸化溶液用的酸类也能造成污染。硝酸中杂质较多,陈旧试剂更为严重。通常可用蒸馏共沸混合物的方法予以精制。精制时要使用石英冷凝器,不然残存杂质较多。盐酸中金属杂质也不少,往往含铅较多,可用二次蒸馏的方法予以精制。必要时可用溶剂萃取法精制所用的盐类。将8-羟基喹啉的氯仿溶液与盐类的中性溶液充分混合,即可萃取除去其中的杂质。
试剂在贮存过程中有污染的可能。试剂溶液即使贮存在耐腐蚀容器中,其浓度也往往会发生变化,所以不应使用长期搁置的试剂。试剂应贮存在清洁、低温和阴暗的地方。
有机试剂有时也含有金属杂质,因此必须蒸馏精制。水必须是高纯的(一般使用实验室二级用水)。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















