一、目的及要求
1.了解和熟悉紫外分光光度计。
2.掌握紫外分光光度法测定苯甲酸的方法和原理。
3.学习用一元线性回归法作标准曲线的方法。
二、实验原理
为防止食品在贮存、运输过程中发生腐败、变质,常在食品中添加少量防腐剂。防腐剂使用的品种和用量在食品卫生标准中都有严格的规定,苯甲酸及其钠盐、钾盐是食品卫生标准允许使用的主要防腐剂之一,其使用量一般在0.1%左右。苯甲酸具有芳香结构,在波长225 nm和272 nm处有K吸收带和B吸收带。
由于食品中苯甲酸用量很少,同时食品中其他成分也可能产生干扰,因此一般需要预先将苯甲酸与其他成分分离。从食品中分离防腐剂常用的方法有蒸馏法和溶剂萃取法等。本实验采用蒸馏法,将样品中苯甲酸在酸性(H3PO4)溶液中随水蒸气蒸馏出来,与样品中非挥发性成分分离,然后用K2Cr2O7溶液和H2SO4溶液进行氧化,使得除苯甲酸以外的其他有机物氧化分解,将此氧化后的溶液再次蒸馏,用碱液(NaOH)吸收苯甲酸,第二次所得蒸馏液中除苯甲酸以外,基本不含其他杂质。根据苯甲酸(钠)在225 nm处有最大吸收,测得其吸光度即可用标准曲线法求出样品中苯甲酸的含量。
三、仪器及试剂
1.仪器
紫外分光光度计(任一型号)
蒸馏装置
2.试剂
无水Na2SO4(分析纯)
85%H3PO4
0.1 mol·L-1NaOH
0.01 mol·L-1NaOH
0.033 mol·L-1K2Cr2O7
2 mol·L-1H2SO4
0.10 mg·mL-1苯甲酸标准溶液:称取100 mg苯甲酸(A.R.,预先经105℃干燥),加入100 mL 0.1 mo1·L-1NaOH溶液,溶解后用水稀释至1 000 mL
四、操作步骤
1.样品测定
准确称取10.0 g均匀的样品,置于250 mL蒸馏瓶中,加1 mL H3PO4、20 g无水Na2SO4、70 mL水、3粒玻璃珠进行第一次蒸馏。用预先加有5 mL 0.1 mol·L-1NaOH的50 mL容量瓶接收馏出液,当蒸馏液收集到45 mL时,停止蒸馏,用少量水洗涤冷凝器,最后用水稀释到刻度。
吸取上述蒸馏液25 mL,置于另一只250 mL蒸馏瓶中,加入25 mL 0.033 mol·L-1K2Cr2O7溶液,6.5 mL 2 mol·L-1H2SO4溶液,连接冷凝装置,水浴加热10 min,冷却,取下蒸馏瓶,加入1 mL H3PO4、20 g无水Na2SO4、40 mL水、3粒玻璃珠进行第二次蒸馏,用预先加有5 mL 0.1 mol·L-1NaOH的50 mL容量瓶接收蒸馏液,当蒸馏液收集到45 mL左右时,停止蒸馏,用少量水洗涤冷凝器,最后用水稀释到刻度。
根据样品中苯甲酸含量,取第二次蒸馏液5~20 mL,置于50 mL容量瓶中,用0.01 mol·L-1NaOH定容,以0.01 mol·L-1NaOH作为对照液,于紫外分光光度计225 nm处测定吸光度。
2.空白试验
准确称取10.0 g均匀的样品,按上述样品测定方法操作,但第一次蒸馏时用5 mL 0.1 mol·L-1NaOH代替1 mL H3PO4。测定空白溶液的吸光度A0。
若测定试样中无干扰组分,则无需分离,可直接测定。以雪碧为例,吸取一定体积试样在50 mL容量瓶中用蒸馏水稀释定容,即可供紫外光谱测定。标准溶液也不需蒸馏,直接配制测定即可。
3.标准溶液的测定
取苯甲酸标准溶液50 mL,置于250 mL蒸馏瓶中,然后按样品测定方法进行第一次蒸馏。将全部蒸馏液50 mL置于250 mL蒸馏瓶中,然后按样品测定方法进行第二次蒸馏。取第二次蒸馏液2.00 mL、4.00 mL、6.00 mL、8.00 mL、10.00 mL,分别置于50 mL容量瓶中,用0.01 mol·L-1NaOH溶液稀释至刻度。以0.01 mol·L-1NaOH为对照液,测定其中一种标准溶液的紫外-可见吸收光谱(测定波长范围为200~350 nm),找出λmax,然后在λmax处测定5种标准溶液的吸光度Ai,按下面介绍的一元线性回归法绘制标准曲线。
五、数据处理
1.记录数据
将标准溶液的质量浓度ρ和扣除A0的吸光度A数据填入表5-2中。
表5-2 苯甲酸标准溶液浓度及吸光度测定数据
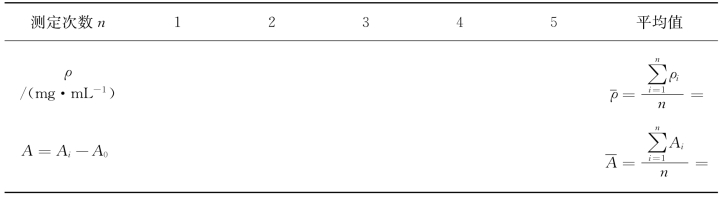
2.(一元线性回归法)绘制标准曲线
(1)一元线性回归方程 由于存在随机(偶然)误差,即使在线性范围内,浓度分别为ρ1,ρ2,ρ3,ρ4,ρ5,…的标准系列,其相应的响应信号的测量值(吸光度)A1,A2,A3,A4,A5,…也不一定都在一条直线上。因此,用简单的方法很难绘制出比较准确反映A与ρ之间关系的标准曲线。这里介绍一种比较常用可靠的方法——一元线性回归法绘制标准曲线,它给出A与ρ的关系式(即一元线性回归方程)
A=bρ+a
式中,b为回归系数,即回归直线的斜率;a为截距,a=A-bρ。
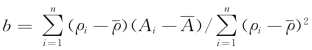
依次计算b和a,数据填入表5-3中。
表5-3 计算数据

将计算的a,b值代入方程A=bρ+a中,即得本次实验数据组的一元线性回归方程。
(2)绘制标准曲线 由(1)可知,当ρ=0时,A=a;当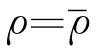 时,A=
时,A= 。因此,以ρ为横坐标,A为纵坐标过(0,a)和
。因此,以ρ为横坐标,A为纵坐标过(0,a)和 )两点在ρ的浓度范围内作直线,此直线即本实验给定的数据组(ρi,Ai)所确定的一条最可靠的标准曲线。
)两点在ρ的浓度范围内作直线,此直线即本实验给定的数据组(ρi,Ai)所确定的一条最可靠的标准曲线。
(3)计算样品中苯甲酸含量 将实验测得(扣除空白A0)的样品吸光度(Ax)从曲线上找出相应的苯甲酸浓度ρx,按下列公式计算样品中苯甲酸含量。也可将测得的Ax值代入一元线性回归方程中求得苯甲酸的浓度和样品中苯甲酸的含量,以此比较。

式中,m为样品的质量,mg;V为样品测定时所取的第二次蒸馏液体积,mL;ρx为从标准曲线上查得样品溶液中苯甲酸钠的质量浓度,mg·mL-1。
六、思考题
1.如何利用一元线性回归法绘制标准曲线及计算样品中苯甲酸含量?
2.怎样安装蒸馏装置?
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。
















